Οι αντιδράσεις αλογόνωσης είναι ένας τύπος αντίδρασης οργανικής υποκατάστασης, δηλαδή εκείνων στις οποίες a άτομο ή ομάδες ατόμων αντικαθίστανται από άτομα ή ομάδες ατόμων άλλου μορίου οργανικός.
Γενικά, αυτός ο τύπος αντίδρασης λαμβάνει χώρα με αλκάνια και αρωματικούς υδρογονάνθρακες (βενζόλιο και τα παράγωγά του).
Η αλογόνωση ονομάζεται έτσι επειδή συμβαίνει με τις απλές ουσίες των αλογόνων: F2, Cl2, αδερφέ2 Γεια2. Ωστόσο, το πιο κοινό μεταξύ αυτών είναι η χλωρίωση (Cl2) και βρωμίωση (Br2), καθώς το φθόριο είναι πολύ αντιδραστικό και οι αντιδράσεις του είναι εκρηκτικές και δύσκολο να ελεγχθούν, καταστρέφοντας ακόμη και την οργανική ύλη:
Χ.Χ.4 (ζ) + 2 F2 (ζ) → Γ(μικρό) + 4HF(σολ)
Οι αντιδράσεις με το ιώδιο είναι εξαιρετικά αργές.
Ακολουθούν οι κύριοι τύποι αλογόνωσης και μερικά παραδείγματα:
1. Αλογόνωση με αλκάνια: Δεδομένου ότι τα αλκάνια είναι ελάχιστα αντιδραστικά, οι αντιδράσεις αλογόνωσής τους λαμβάνουν χώρα μόνο παρουσία ηλιακού φωτός (λ), υπεριώδους φωτός ή έντονης θέρμανσης. Αυτός ο τύπος αντίδρασης γίνεται για να ληφθεί ένα αλκυλαλογονίδιο.
Παράδειγμα: μονοχλωρίωση μεθανίου:
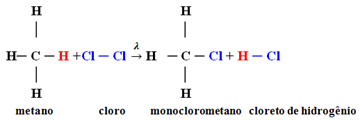
Στην περίπτωση αυτή προήλθε από άτομο υδρογόνου μεθανίου (CH4) να αντικατασταθεί από ένα άτομο χλωρίου, δίνοντας μονοχλωρομεθάνιο. Εάν υπήρχε πάρα πολύ χλώριο, αυτή η αντίδραση θα μπορούσε να συνεχίσει να επεξεργάζεται, αντικαθιστώντας όλα τα υδρογόνα στο μεθάνιο.
1.1. Αλογόνωση σε αλκάνια με περισσότερους από 3 άνθρακες: Εάν το αλκάνιο που θα αντιδράσει έχει τουλάχιστον 3 άτομα άνθρακα, καταλήγουμε με ένα μείγμα διαφορετικών υποκατεστημένων ενώσεων. Δείτε το παρακάτω παράδειγμα μονοχλωρίωσης μεθυλοβουτανίου:
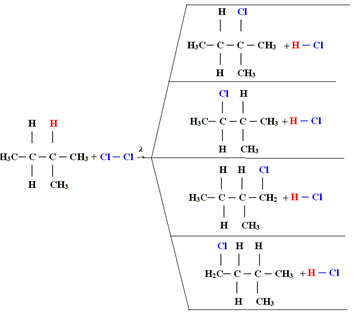
Η ποσότητα κάθε ένωσης θα είναι ανάλογη με την ακόλουθη σειρά ευκολίας με την οποία απελευθερώνεται υδρογόνο στο μόριο:

Έτσι, στην παραπάνω περίπτωση, η μεγαλύτερη ποσότητα θα είναι 2-μεθυλ-2-χλωροβουτάνιο και η μικρότερη ποσότητα θα είναι 2-μεθυλ-1-χλωροβουτάνιο.
2. Αλογόνωση βενζολίου: Το βενζόλιο δεν αντιδρά κανονικά με χλώριο ή βρώμιο. Ωστόσο, εάν ένα οξύ Lewis χρησιμοποιείται ως καταλύτης (συνήθως χρησιμοποιείται FeCl3, FeBr3 ή AlCl3, όλα σε άνυδρη μορφή), το βενζόλιο αντιδρά εύκολα σε αντίδραση αλογόνωσης.
Το χλωριούχο και το σιδηρούχο βρωμίδιο μπορούν να ληφθούν προσθέτοντας απλώς το σίδηρο στο μείγμα και έτσι αντιδρά με το αλογόνο και παράγει το οξύ Lewis:
2 Fe + 3 Br2 → 2 FeBr3
Δείτε ένα παράδειγμα αλογόνωσης βενζολίου και του μηχανισμού του:
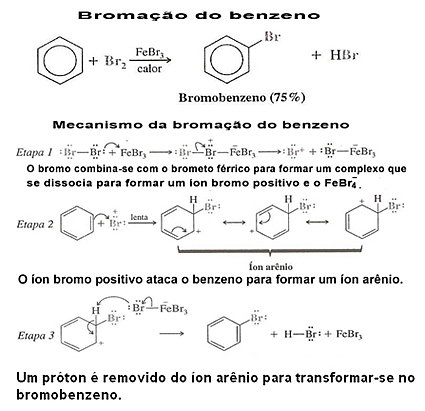
3. Αλογόνωση παραγώγων βενζολίου:Σε τέτοιες περιπτώσεις, η υποκατάσταση καθοδηγείται από τον υποκαταστάτη ή τη λειτουργική ομάδα που συνδέεται με τον αρωματικό πυρήνα. Για να δείτε πώς συμβαίνει αυτό, διαβάστε τα κείμενα "Ρίζα διεύθυνσης στο δακτύλιο βενζολίου" και "Ηλεκτρονικά εφέ ριζών μετα-και ορθο-διευθυντών”.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/reacoes-organicas-halogenacao.htm
