Στο λειτουργίες αζώτου είναι μια ομάδα από ΟΡΓΑΝΙΚΕΣ ΕΝΩΣΕΙΣ που έχουν άτομα του άζωτο συνδέεται με την αλυσίδα άνθρακα. Διακρίνονται από τις αντίστοιχες λειτουργικές τους ομάδες, οι οποίες είναι σύνολα ατόμων συνδεδεμένα σε μια συγκεκριμένη διαμόρφωση και που ορίζουν τις χαρακτηριστικές ιδιότητες κάθε συνάρτησης.
Οι λειτουργίες του αζώτου είναι:
αμίνες;
αμίδια;
νιτροενώσεις;
νιτρίλια;
ισονιτρίλια.
Διαβάστε επίσης:Ποιες είναι οι λειτουργίες του οξυγόνου;
Περίληψη των συναρτήσεων του αζώτου
Οι λειτουργίες αζώτου είναι οργανικές ενώσεις που περιέχουν άτομα του αζώτου.
Οι αμίνες, τα αμίδια, οι νιτροενώσεις, τα νιτρίλια και τα ισονιτρίλια είναι οι συναρτήσεις αζώτου.
Οι ανόργανες συναρτήσεις διακρίνονται από τη λειτουργική τους ομάδα.
Οι αμίνες προέρχονται από την υποκατάσταση του υδρογόνα αμμωνίας από ρίζες αλκυλίου.
Τα αμίδια έχουν το ίδιο άτομο άνθρακα ενωμένο με άζωτο και άνθρακα. οξυγόνο.
Οι νιτροενώσεις περιέχουν την ομάδα -ΝΟ.2.
Τα νιτρίλια χαρακτηρίζονται από την παρουσία τριπλού δεσμού μεταξύ άνθρακα και αζώτου.
Τα ισονιτρίλια έχουν τριπλό δεσμό μεταξύ αζώτου και άνθρακας, με άζωτο προσαρτημένο στην ανθρακική αλυσίδα.
Βίντεο μάθημα για τις αζωτούχες συναρτήσεις
Ποιες είναι οι λειτουργίες του αζώτου;
Οι συναρτήσεις αζώτου είναι ένα σύνολο από οργανικές συναρτήσεις που έχουν το άτομο αζώτου στη δομή τους, εκτός από άτομα άνθρακα και υδρογόνου. Είναι: αμίνες, αμίδια, νιτροενώσεις, νιτρίλια και ισονιτρίλια,
Αυτό που διαφοροποιεί τις αζωτούχες λειτουργίες είναι οι αντίστοιχες λειτουργικές ομάδες, οι οποίες είναι η δομική διάταξη των ατόμων που είναι υπεύθυνα για τις ιδιότητες της ουσίας.
Ποιες είναι οι λειτουργίες του αζώτου;
αμίνες
Η οργανική λειτουργία το ορυχείο χαρακτηρίζεται συνδέοντας τουλάχιστον μία αλυσίδα άνθρακα με το άτομο αζώτου. Η λειτουργική ομάδα των αμινών είναι -N-R1R2R3 (οι ομάδες R είναι αλυσίδες άνθρακα ή άτομα υδρογόνου, τουλάχιστον ένα από τα οποία είναι αλυσίδα άνθρακα).

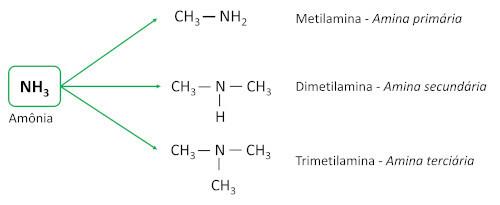
οι αμίνες προέρχονται από αμμωνία (ΝΗ3), με ένα ή περισσότερα άτομα υδρογόνου που έχουν αντικατασταθεί από άτομα άνθρακα ή συνδέτες αλκυλίου. Είναι βασικές ουσίες, αφήνοντας το pH μεγαλύτερο από 7 σε υδατικό διάλυμα.
Ταξινομούνται ανάλογα με την ποσότητα των ατόμων υδρογόνου που αντικαθίστανται από συνδέτες άνθρακα (ομάδες αλκυλίου ή αρυλίου), οι οποίοι ονομάζονται υποκαταστάτες.
- Πρωτοταγείς αμίνες: έχουν έναν μόνο υποκαταστάτη άνθρακα.
- Δευτεροταγείς αμίνες: έχουν δύο υποκαταστάτες άνθρακα.
- Τριτοταγείς αμίνες: έχουν τρεις ανθρακικούς υποκαταστάτες, δηλαδή το άτομο αζώτου δεν είναι πλέον συνδεδεμένο με κανένα άτομο υδρογόνου, δημιουργώντας τρεις Συνδέσεις απλό με άτομα άνθρακα.
ΕΝΑ ονοματολογία για αμίνες ακολουθεί τις οδηγίες του IUPAC (International Union of Pure and Applied Chemistry). Στην περίπτωση των πρωτοταγών αμινών, η κατασκευή του ονόματος λαμβάνει υπόψη τον αριθμό των ανθράκων (πρόθεμα), τη φύση του δεσμού μεταξύ των ανθράκων (επίθημα) και ο όρος χρησιμοποιείται το ορυχείο για την κατάληξη (τέλος λέξης).

Δείτε το παράδειγμα:
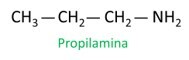
Όταν εκχωρείτε αριθμούς σε άνθρακες για τη θέση των ριζών, εκχωρείτε τον μικρότερο δυνατό αριθμό στο άτομο που βρίσκεται πλησιέστερα στην ομάδα NH.2.
Για τις δευτεροταγείς και τριτοταγείς αμίνες, η ονοματολογία θεωρεί τη μεγαλύτερη ομάδα υποκαταστάτη που συνδέεται με το άζωτο ως κύρια αλυσίδα, και οι άλλοι συνδετήρες γράφονται με το πρόθεμα που αναφέρεται στον αριθμό των ανθράκων και το επίθημα -il, με το γράμμα Ν μπροστά τους.

Παράδειγμα:
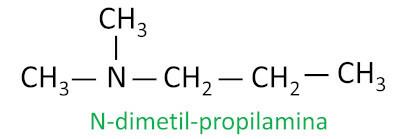
Αμίδια
Η οργανική λειτουργία αμίδιο χαρακτηρίζεται από συνδέοντας μια ομάδα καρβονυλίου (C=O) με το άτομο αζώτου, όπου το άζωτο μπορεί να συνδεθεί με άτομα άνθρακα ή υδρογόνου.
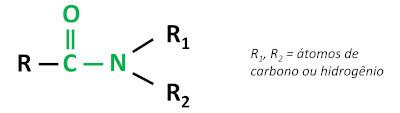
τα αμίδια είναι βασικές ουσίες, αφήνοντας το pH πάνω από 7 σε υδατικό διάλυμα. Η ουσία ουρία ανήκει στην ομάδα των αμιδίων και είναι μια ένωση που υπάρχει φυσικά στα ούρα, που προέρχεται από διαδικασίες αποδόμησης που συμβαίνουν σε ζωντανούς οργανισμούς.
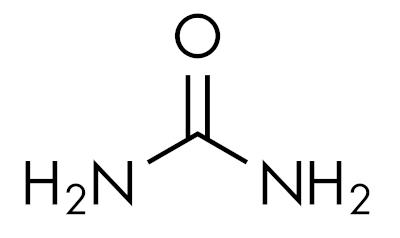
Τα αμίδια είναι χαρακτηριστικά ανάλογα με το επίπεδο υποκατάστασης του αζώτου. Σαν αυτό:
- Πρωτογενή αμίδια: κρατήστε δύο άτομα υδρογόνου μαζί με το άζωτο.
- Δευτερεύοντα αμίδιαή μονουποκατεστημένο: ένα από τα υδρογόνα έχει αντικατασταθεί από αλυσίδα άνθρακα, έτσι το άζωτο διατηρεί έναν μόνο δεσμό με το υδρογόνο.
- τριτοταγή αμίδιαή εκτοπισμένοι: Το άζωτο δεν έχει πλέον δεσμούς υδρογόνου, όλοι τους έχουν αντικατασταθεί από άνθρακες.

Τα αμίδια είναι Ονομάστηκε σύμφωνα με την IUPAC, τα μόρια ονομάζονται με την ακολουθία:

Στο διακλαδισμένο αμίδιο, το άτομο άνθρακα της αμιδικής ομάδας συμμετέχει στην κύρια αλυσίδα και ο αριθμός άνθρακα πρέπει να ξεκινά με αυτό. Κοίτα:
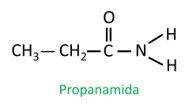 |
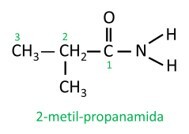 |
Σε μονουποκατεστημένα ή διυποκατεστημένα αμίδια, τα Το γράμμα N υποδηλώνει τη θέση του κλάδου που είναι συνδεδεμένο με το άτομο αζώτου. Εάν υπάρχει άλλη ρίζα στην αλυσίδα, θα γραφτεί αφού προσδιοριστεί η ρίζα που αναφέρεται στο N.
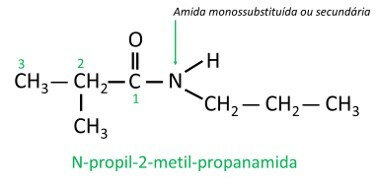
νιτροενώσεις
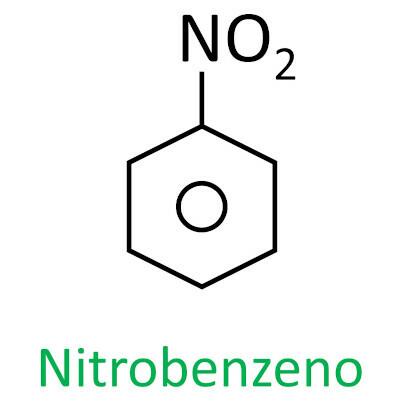
Εσείς νιτροενώσεις είναι οργανικές ενώσεις που περιέχουν μια νίτρο ομάδα (-NO2) προσαρτημένο σε μια αλυσίδα άνθρακα, το οποίο μπορεί να είναι αλειφατικό (ανοιχτό ή γραμμικό) ή αρωματικό.
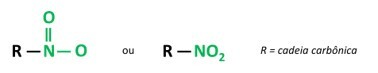
ΕΝΑ κύριο χαρακτηριστικό αυτών των ουσιών είναι η εκρηκτική τους δύναμη. Η εκρηκτική ικανότητα συνδέεται με τις αρωματικές νιτροενώσεις και όσο μεγαλύτερος είναι ο αριθμός των νιτροομάδων, τόσο μεγαλύτερη είναι η έκρηξη. Οι αλειφατικές νιτροενώσεις χρησιμοποιούνται στα εργαστήρια ως οργανικοί διαλύτες.
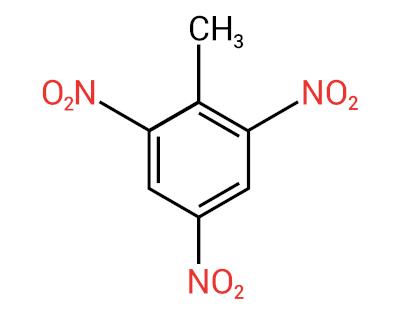
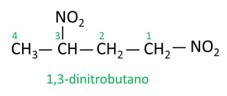
Η ονοματολογία για αυτές τις ενώσεις σχηματίζεται από τη λέξη νίτρο ακολουθούμενο από το όνομα του υδρογονάνθραξ (πρόθεμα + επίθεμα + κατάληξη -Ο).
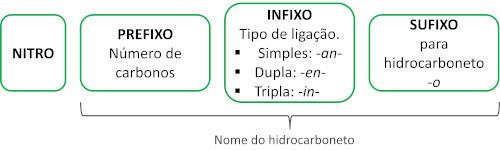
Δείτε μερικά παραδείγματα:
 |
 |
νιτρίλια
Τα νιτρίλια είναι οργανικές ενώσεις που χαρακτηρίζονται από το τριπλός δεσμός μεταξύ ενός ατόμου άνθρακα και ενός ατόμου αζώτου, παρουσιάζοντας τη λειτουργική ομάδα – C ≡ N. Στα νιτρίλια, το άζωτο βρίσκεται στο τέλος και ο άνθρακας συνδέεται απευθείας με την ανθρακική αλυσίδα.

τα νιτρίλια Γνωστό και ως κυανίδια, καθώς προέρχονται από αντιδράσεις με υδροκυανικό οξύ (HCN).
είναι ουσίες τοξικό για τον άνθρωπο, γιατί μέσα στο σώμα μπορούν να σχηματίσουν υδροκυανικό οξύ σε επαφή με το οξύ του στομάχου, εμποδίζοντας τις διεργασίες του κυτταρική αναπνοή των κυττάρων.
Στη φύση, τα νιτρίλια βρίσκονται σε ορισμένα πυρηνόκαρπα, αλλά σε πολύ χαμηλή συγκέντρωση, χωρίς κινδύνους, και στα φύλλα της άγριας μανιόκας.

Ο κανόνας Iupac για την ονοματολογία των νιτριλίων ορίζει ότι ο όρος νιτρίλιο προστίθεται ως επίθημα:

Δείτε μερικά παραδείγματα:
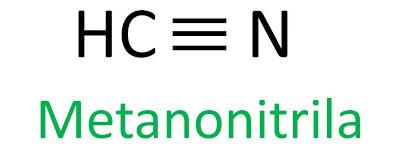 |
 |
Η συνήθης μορφή ονοματολογίας για τα νιτρίλια είναι κυάνιο + όνομα ρίζας.
ισονιτρίλια
Τα ισονιτρίλια, ή ισονιτρίλια, είναι ενώσεις που σχηματίζονται από το τριπλός δεσμός μεταξύ ενός ατόμου άνθρακα και ενός ατόμου αζώτου, παρουσιάζοντας τη λειτουργική ομάδα – R ≡ C. Στα ισονιτρίλια, ο άνθρακας βρίσκεται στο άκρο και το άζωτο συνδέεται απευθείας στην ανθρακική αλυσίδα.

Τα ισονιτρίλια διαφέρουν από τα νιτρίλια λόγω της θέσης των ατόμων αζώτου και άνθρακα, και Στα ισονιτρίλια, το άζωτο χαρακτηρίζεται ως ετεροάτομο., καθώς βρίσκεται ανάμεσα σε δύο άνθρακες.
Είναι ασταθή είδη και μπορούν να μετατραπούν σε νιτρίλια σε υψηλές θερμοκρασίες. Οι αντιδράσεις ισοκυανιδικού οξέος δημιουργούν ισονιτρίλια, γι' αυτό και αυτές οι ενώσεις είναι γνωστές και ως ισοκυανίδια.
Τα μόρια ισονιτριλίου ακολουθούν τον κανόνα Iupac για την ονομασία:
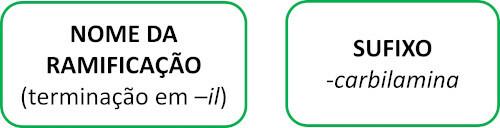
Δείτε μερικά παραδείγματα:
 |
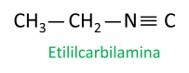 |
Εφαρμογές συναρτήσεων αζώτου
Οι ουσίες που ανήκουν στις αζωτούχες λειτουργίες έχουν πολυάριθμες εφαρμογές, κυρίως στον βιομηχανικό χώρο, για την παρασκευή πολυμερή, καουτσούκ, συνθετικές ίνες, φαρμακευτικά προϊόντα, αγροχημικά, φυτοφάρμακα και εκρηκτικά.
Στο οι αμίνες χρησιμοποιούνται στην παραγωγή βαφών, σαπούνια, φάρμακα, στη διαδικασία της βουλκανισμός καουτσούκ, εκρηκτικά και άλλες βιομηχανικές διεργασίες, ενώ βρίσκονται επίσης σε φυτά και σχηματίζονται σε διαδικασίες αποσύνθεσης οργανικής ύλης.

Στο Τα αμίδια έχουν ευρεία εφαρμογή στον βιομηχανικό και χημικό τομέα, που υπάρχουν στην παραγωγή πολυμερών (όπως νάιλον και πολυουρεθάνη), ρητινών, εκρηκτικών, λιπάσματα, εντομοαπωθητικά, λιπάσματα και φάρμακα.

Εσείς νιτροενώσειςΗ κύρια εφαρμογή του είναι η κατασκευή εκρηκτικών. που χρησιμοποιούνται στον στρατιωτικό, βιομηχανικό και μεταλλουργικό τομέα (για εξόρυξη πρώτων υλών). Μία από τις πιο γνωστές νιτροενώσεις είναι το τρινιτροτολουόλιο, ευρέως γνωστό ως TNT. Άλλες εφαρμογές των νιτροενώσεων είναι στην παραγωγή Φυτοφάρμακα, βακτηριοκτόνα, βαφές, διύλιση πετρελαίου κ.λπ.

Στο τα νιτρίλια χρησιμοποιούνται ως οργανικοί διαλύτες στο εργαστήριο και στη βιομηχανία, συμμετέχοντας στις διαδικασίες εκχύλισης και παραγωγής ορισμένων συνθετικών ινών, πλαστικών πολυμερών, βαφών και λιπασμάτων.

Στο Τα ισονιτρίλια χρησιμοποιούνται σε διάφορες διαδικασίες για την παραγωγή οργανικών ενώσεων, όπως διαλύτες, και συμμετέχουν στην κατασκευή αγροχημικών, φυτοφαρμάκων, καουτσούκ και πλαστικών.
Διαβάστε επίσης:Αλογονίδια — ουσίες που έχουν άτομα αλογόνου συνδεδεμένα στην αλυσίδα άνθρακα
Λυμένες ασκήσεις συναρτήσεων αζώτου
ερώτηση 1
(Τροποποιημένο με FPS-PE) Η εφαρμογή αζωτούχων ενώσεων στη συνθετική οργανική χημεία είναι πολύ διαφοροποιημένη και περιλαμβάνει την παρασκευή φαρμάκων, βαφών, εκρηκτικών και βιταμινών. Δείτε τις παρακάτω ενώσεις.
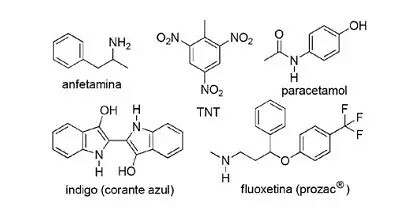
Σχετικά με αυτές τις ενώσεις, σημειώστε τη λανθασμένη δήλωση.
α) Το TNT είναι μια νίτρο ένωση.
β) Το αζωτούχο τμήμα της φλουοξετίνης είναι δευτεροταγής αμίνη.
γ) Η αμφεταμίνη ταξινομείται ως πρωτογενές αμίδιο.
δ) Το Indigo έχει ετεροαρωματικούς δακτυλίους στη δομή του.
ε) Το αζωτούχο μέρος της παρακεταμόλης είναι ένα αμίδιο.
Ανάλυση:
Γράμμα Γ
Το αντικειμενο ο είναι σωστό, επειδή η ΤΝΤ είναι μια νιτρο ένωση επειδή δεν έχει ομάδες ΟΧΙ2.
Το αντικειμενο σι είναι σωστό. Το αζωτούχο τμήμα της φλουοξετίνης είναι δευτεροταγής αμίνη επειδή συνδέεται με δύο τμήματα άνθρακα.
Το αντικειμενο w είναι λανθασμένη, καθώς η αμφεταμίνη ταξινομείται ως πρωτοταγής αμίνη και όχι ως αμίδιο. Σημειώστε ότι η παρούσα ομάδα είναι NH2. Αυτή είναι λοιπόν η ουσία της ερώτησης.
Το αντικειμενο ρε είναι σωστό, καθώς το λουλακί έχει ετεροαρωματικούς δακτυλίους στη δομή του, δηλαδή δακτυλίους που σχηματίζονται από άτομα άνθρακα και ένα άλλο στοιχείο — στην περίπτωση αυτή, άζωτο.
Το αντικειμενο είναι είναι σωστό, επειδή η παρακεταμόλη είναι ένα αμίδιο που παρουσιάζει άνθρακα συνδεδεμένο με άζωτο και οξυγόνο.
Ερώτηση 2
(UFMS) Yerba mate (Ilex paraguariensis), με καταγωγή από τη Νότια Αμερική, χρησιμοποιείται ως τονωτικό και διεγερτικό ποτό. Το προϊόν που λαμβάνεται με την επεξεργασία των φύλλων yerba mate μπορεί να χρησιμοποιηθεί για την παρασκευή chimarrão και tereré, μεταξύ άλλων ποτών που καταναλώνονται συνήθως και πολιτιστικά σε περιοχές της Αργεντινής, της Παραγουάης και Βραζιλία. Το μεγάλο ενδιαφέρον για το yerba mate οφείλεται στις χημικές ενώσεις που υπάρχουν, λόγω των αντιοξειδωτικών, διεγερτικών και διουρητικών του ιδιοτήτων.
(Διαθέσιμο σε: http://repositorio.utfpr.edu.br/jspui/bitstream/1/3158/1/PG_PPGEP_Henrique%2C%20 Flavia%20Aparecida_2018.pdf. Πρόσβαση στις: 01 Νοε. 2018. Προσαρμοσμένο).
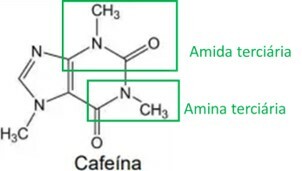
Οι διεγερτικές ιδιότητες του yerba mate σχετίζονται με την περιεκτικότητά του σε μεθυλξανθίνες, μία από τις κυριότερες από αυτές είναι η καφεΐνη, η δομή που παρουσιάζεται παρακάτω:

Κατά την ανάλυση του δομικού τύπου της καφεΐνης, είναι σωστό να δηλωθεί ότι έχει τις ακόλουθες οργανικές λειτουργίες και ιδιότητες:
α) αλδεΰδη και αμίδιο, βασικά.
β) αμίνη και αμίδιο, αλκαλικό.
γ) αμίνη και κετόνη, αλκαλική.
δ) κετόνη και αμίδιο, αμφοτερικά.
ε) καρβοξυλικό οξύ και αμίνη, βασική.
Ανάλυση:
Γράμμα Β
Αναλύοντας τη δομή της καφεΐνης, προσδιορίζονται οι λειτουργικές ομάδες αμίνης και αμιδίου, όπως επισημαίνεται στην παρακάτω εικόνα. Καθώς αυτές οι δύο ομάδες έχουν ένα βασικό ή αλκαλικό χαρακτηριστικό, η καφεΐνη έχει επίσης αυτό το χαρακτηριστικό, που σημαίνει ότι τα υδατικά διαλύματα καφεΐνης έχουν pH πάνω από 7.
Της Ana Luiza Lorenzen Lima
Καθηγητής Χημείας
Πηγή: Σχολείο Βραζιλίας - https://brasilescola.uol.com.br/quimica/funcoes-nitrogenadas.htm
