Αυτό το μείγμα αερίων δημιουργεί ομοιογενή μείγματα ή αέρια διαλύματα. Για παράδειγμα, τα αέρια που βγαίνουν από τις καμινάδες των εργοστασίων, ή τις εξατμίσεις των αυτοκινήτων, εξαπλώνονται στον αέρα ατμοσφαιρικά και, με το πέρασμα του χρόνου, δεν μπορούσαμε να τα διακρίνουμε πλέον, καθώς υπήρχε διάχυση αυτών των αερίων μέσω του αέρας.

Τα αέρια που εκπέμπονται από τις καμινάδες διαχέονται και «χάνονται» στον ατμοσφαιρικό αέρα, επειδή ο όγκος του αέρα είναι πολύ μεγαλύτερος από αυτόν του καπνού.
| Ο διάχυση ενός αερίου είναι η αυθόρμητη κίνηση ενός αερίου μέσω ενός άλλου, δηλαδή η εξάπλωσή του σε άλλο αέριο μέσο. |
| Ο διάχυση των αερίων είναι ένας ιδιαίτερος τύπος διάχυσης, στον οποίο υπάρχει διαρροή αερίων μέσω μικρών οπών (ή πορωδών τοιχωμάτων, που είναι ένα σύνολο μικρών οπών). |
Για παράδειγμα, τα μπαλόνια που πωλούνται σε παιδιά είναι γεμάτα με αέριο ήλιο. Με την πάροδο του χρόνου, αυτό το αέριο καταλήγει να περνά μέσα από τους πόρους από καουτσούκ του μπαλονιού, δηλαδή υπάρχει η διάχυσή του. Αυτό φαίνεται από το γεγονός ότι το μπαλόνι ξεφουσκώνει μετά από λίγες ώρες.
Ο Σκωτσέζος χημικός Thomas Graham, το 1829, μελέτησε αυτή τη συμπεριφορά των αερίων. Κατέληξε στο συμπέρασμα ότι η ταχύτητα με την οποία ένα αέριο διαχέεται ή διαχέεται σε ένα άλλο σχετίζεται με την πυκνότητά του. Καθώς τα πειραματικά του δεδομένα επαναλαμβάνονταν για όλα τα αέρια, δημιούργησε τον ακόλουθο νόμο που φέρει το όνομά του:
Νόμος του Γκράχαμ: ο ρυθμός διάχυσης ή διάχυσης ενός αερίου είναι αντιστρόφως ανάλογος της τετραγωνικής ρίζας της πυκνότητάς του.
Μαθηματικά, αυτός ο νόμος μπορεί να εκφραστεί με την εξίσωση:
v α 
Ή, σχετίζοντας δύο διαφορετικά αέρια, έχουμε:
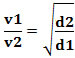
Η μονάδα που χρησιμοποιείται σε αυτήν την περίπτωση είναι ο «όγκος που διαφεύγει ανά μονάδα χρόνου». επομένως γενικά L/min (λίτρα ανά λεπτό).
Έτσι, τα αέρια με χαμηλότερη πυκνότητα διαχέονται πιο γρήγορα. Εάν είναι στην ίδια κατάσταση θερμοκρασίας και πίεσης, μπορείτε επίσης να κάνετε μια σχέση αυτού με τη μάζα μοριακό αέριο: όσο μεγαλύτερη είναι η πυκνότητα του αερίου, τόσο μεγαλύτερη είναι η μοριακή του μάζα και τόσο μικρότερη είναι η ταχύτητά του διάχυση; και αντίστροφα. Έτσι, έχουμε:
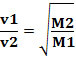
Της Jennifer Fogaça
Πτυχιούχος Χημείας
Σχολική ομάδα Βραζιλίας
Πηγή: Σχολείο Βραζιλίας - https://brasilescola.uol.com.br/quimica/difusao-efusao-dos-gases.htm
