Η οργανική χημεία είναι μια ευρεία περιοχή της χημείας που μελετά τις ενώσεις άνθρακα.
Η γνώση της Οργανικής Χημείας προσεγγίζεται με διάφορους τρόπους και, σκεφτόμαστε, έχουμε συγκεντρώσει προτεινόμενες ασκήσεις, εξετάσεις εισόδου και ερωτήσεις Enem για να δοκιμάσετε τις γνώσεις σας.
Χρησιμοποιήστε επίσης τα σχόλια αναλύσεων για να μάθετε περισσότερα σχετικά με το θέμα.
Προτεινόμενες ασκήσεις
ερώτηση 1
Κοιτάξτε τις οργανικές ενώσεις παρακάτω και προσδιορίστε τις οργανικές λειτουργίες σύμφωνα με τις επισημασμένες λειτουργικές ομάδες. Μετά από αυτό, ονομάστε τις ουσίες.
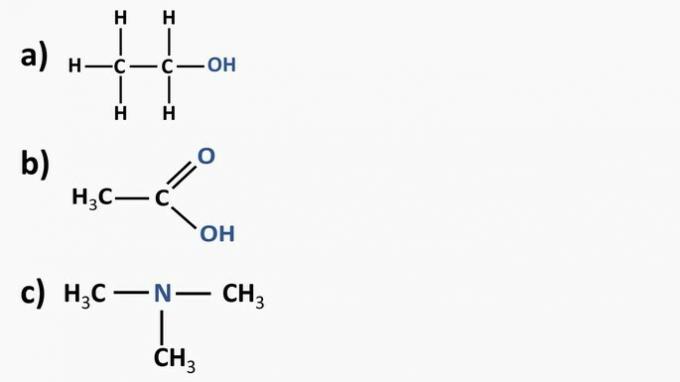
Απάντηση:
α) Οργανική ένωση: αιθανόλη
- οργανική λειτουργία: αλκοόλ
- Γενικός τύπος: R — OH
- Ταυτοποίηση: υδροξύλιο (ΟΗ) συνδεδεμένο με την αλυσίδα άνθρακα
β) Οργανική ένωση: αιθανοϊκό οξύ.
- Οργανική λειτουργία: καρβοξυλικό οξύ
- Γενικός τύπος: R — COOH
- Ταυτοποίηση: καρβοξυλική ρίζα (COOH) συνδεδεμένη με την αλυσίδα του άνθρακα
γ) Οργανική ένωση: τριμεθυλαμίνη
- Οργανική λειτουργία: αμίνη (τριτογενής)
- Γενικός τύπος:
- Ταυτοποίηση: άζωτο συνδεδεμένο με τρεις αλυσίδες άνθρακα
Ερώτηση 2
Στην οργανική χημεία, οι ενώσεις αναγνωρίζονται από τις αλυσίδες που σχηματίζονται από άνθρακα και υδρογόνο. Ωστόσο, άλλα στοιχεία μπορούν να είναι μέρος της χημικής δομής αυτών των ενώσεων, όπως το οξυγόνο.
Επιλέξτε την εναλλακτική λύση όπου οι δύο οργανικές ενώσεις έχουν οξυγονωμένες οργανικές λειτουργίες.
α) χλωροφόρμιο και μεθανοϊκό αιθύλιο
β) προπανόλη και προπανοϊκό οξύ
γ) αιθένιο και αιθανοδιόλη
δ) αιθαναμίδιο και βενζόλιο
Σωστή απάντηση: β) προπανόλη και προπανοϊκό οξύ
Α) ΛΑΘΟΣ. Έχουμε χλωροφόρμιο (CHCl3), το οποίο είναι ένα αλκυλαλογονίδιο, και ο μεθανοϊκός αιθυλεστέρας (C3Η6Ο2), το οποίο περιέχει οξυγόνο στη δομή του.
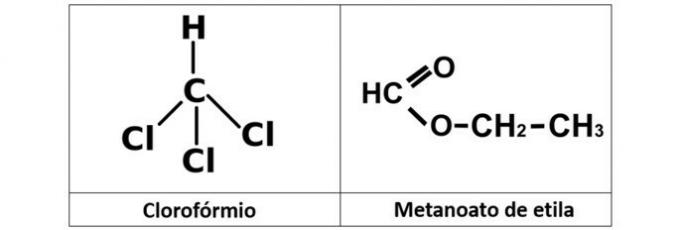
β) ΣΩΣΤΗ. Σε αυτήν την εναλλακτική λύση έχουμε δύο ενώσεις που έχουν οξυγονωμένες οργανικές λειτουργίες. Η προπανόλη (C3Η8Ο) είναι μια αλκοόλη που σχηματίζεται από τρεις άνθρακες. Το προπανοϊκό οξύ (C3Η6Ο2) είναι ένα καρβοξυλικό οξύ.
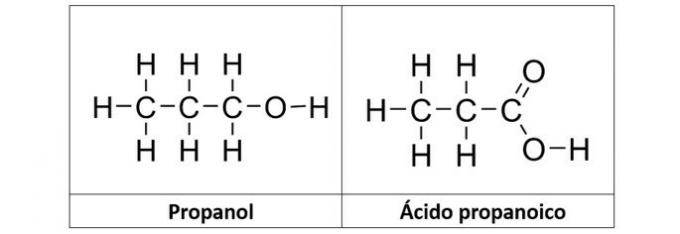
γ) ΛΑΘΟΣ. Το αιθυλένιο (C2Η4), που ονομάζεται επίσης αιθυλένιο, είναι υδρογονάνθρακας τύπου αλκενίου. Ήδη αιθανοδιόλη (Γ2Η6Ο2) είναι μια αλκοόλη με δύο υδροξύλια στη δομή της.
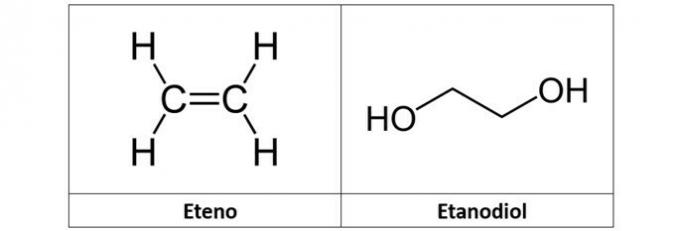
δ) ΛΑΘΟΣ. Αιθαναμίδη (C2Η5ΝΟ) είναι ένα αμίδιο και το βενζόλιο είναι ένας αρωματικός υδρογονάνθρακας και, επομένως, σχηματίζεται μόνο από άνθρακα και υδρογόνο.

ερώτηση 3
Κοιτάξτε τη δομή της οργανικής ένωσης παρακάτω και ελέγξτε τις πραγματικές δηλώσεις.

(01) Η ένωση έχει οργανική λειτουργία αζώτου.
(02) Είναι μια πρωτοταγής αμίνη, καθώς συνδέεται με ένα μόνο υδρογόνο.
(03) Το όνομα της ένωσης είναι διαιθυλαμίνη.
Σωστή απάντηση:
(01) ΣΩΣΤΗ. Η αζωτούχος οργανική λειτουργία που υπάρχει στην ένωση είναι αμίνη.
(02) ΛΑΘΟΣ. Είναι μια δευτεροταγής αμίνη, καθώς το άζωτο συνδέεται με δύο αλυσίδες άνθρακα.
(03) ΛΑΘΟΣ. Το όνομα της ένωσης είναι διμεθυλαμίνη, καθώς υπάρχουν δύο ρίζες μεθυλίου συνδεδεμένες με άζωτο.
ερώτηση 4
Η ευγενόλη, μέλος της οικογένειας φαινυλοπροπανοειδών, είναι μια αρωματική οργανική ένωση που υπάρχει στα γαρίφαλα, ένα μπαχαρικό που χρησιμοποιείται από την αρχαιότητα.

Παρατηρήστε τον συντακτικό τύπο της ένωσης και αναγνωρίστε τις οργανικές λειτουργίες που υπάρχουν.
α) Αλκοόλ και αιθέρας
β) Φαινόλη και αιθέρας
γ) Αλκοόλ και εστέρας
δ) Φαινόλη και εστέρας
ε) Αλκοόλ και υδρογονάνθρακες
Σωστή εναλλακτική λύση: β) Φαινόλη και αιθέρας.
Η ευγενόλη έχει οξυγονωμένες οργανικές λειτουργίες στην αλυσίδα της, δηλαδή, εκτός από τα άτομα άνθρακα και υδρογόνου, το οξυγόνο είναι ένα ετεροάτομο.
Η οργανική λειτουργία φαινόλης χαρακτηρίζεται από το υδροξύλιο (-ΟΗ) που συνδέεται με έναν αρωματικό δακτύλιο. Στη λειτουργία αιθέρα, το οξυγόνο βρίσκεται μεταξύ δύο αλυσίδων άνθρακα.
ερώτηση 5
Το EDTA, του οποίου το πλήρες όνομα είναι αιθυλενοδιαμινοτετραοξικό οξύ, είναι μια οργανική ένωση με πολλές εφαρμογές. Η ικανότητά του να δεσμεύει μεταλλικά ιόντα το καθιστά παράγοντα χηλίωσης που χρησιμοποιείται ευρέως τόσο στο εργαστήριο όσο και βιομηχανικά.
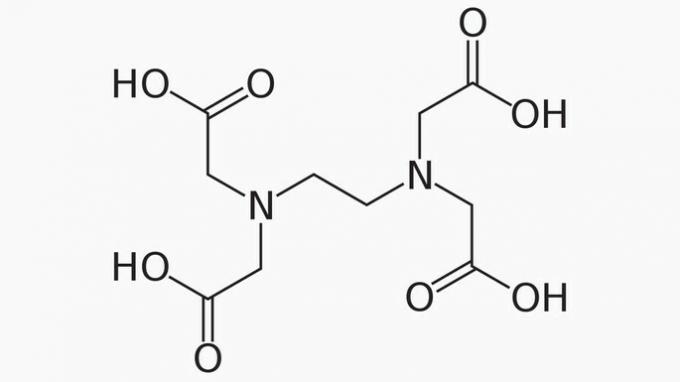
Σχετικά με το EDTA, είναι σωστό να δηλώνεται ότι η ανθρακική αλυσίδα είναι:
α) Ανοιχτό, ομοιογενές και ακόρεστο.
β) Κλειστό, ετερογενές και κορεσμένο.
γ) Ανοιχτό, ετερογενές και ακόρεστο.
δ) Κλειστό, ομοιογενές και κορεσμένο.
ε) Ανοιχτό, ετερογενές και κορεσμένο.
Σωστή απάντηση: ε) Ανοιχτό, ετερογενές και κορεσμένο.
Η αλυσίδα EDTA ταξινομείται σε:
ΑΝΟΙΞΕ. Σύμφωνα με τη διάταξη των ατόμων άνθρακα στη δομή του EDTA, μπορούμε να δούμε ότι, λόγω της παρουσίας άκρων, η αλυσίδα της ένωσης είναι ανοιχτή.
ΕΤΕΡΟΓΕΝΗΣ. Εκτός από τις ενώσεις άνθρακα και υδρογόνου, η αλυσίδα άνθρακα έχει ετεροάτομα αζώτου και οξυγόνου.
ΚΑΤΩ. Οι δεσμοί μεταξύ των ατόμων άνθρακα είναι κορεσμένοι, καθώς η αλυσίδα έχει μόνο μεμονωμένους δεσμούς.
Μάθετε περισσότερα στο: Οργανική χημεία.
ερωτήσεις για τις εισαγωγικές εξετάσεις
ερώτηση 1
(UFSC) Παρατηρήστε τις ατελείς οργανικές δομές και προσδιορίστε τα σωστά αντικείμενα:
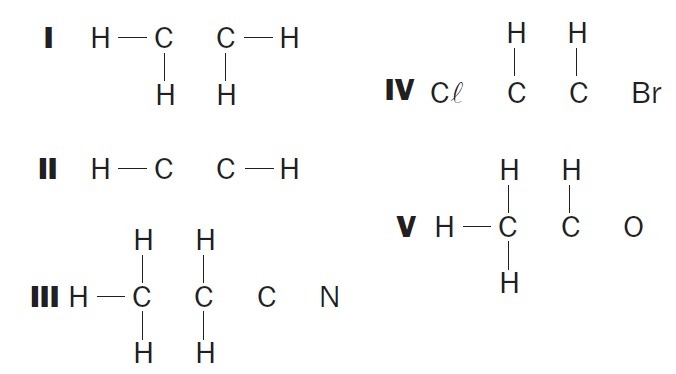
(01) Δομή Δεν έχω ούτε έναν δεσμό μεταξύ των ατόμων άνθρακα.
(02) Η δομή II στερείται τριπλού δεσμού μεταξύ των ατόμων άνθρακα.
(03) Η δομή III στερείται δύο μονών δεσμών μεταξύ ατόμων άνθρακα και τριπλού μεταξύ ατόμων άνθρακα και αζώτου.
(04) Η δομή IV στερείται δύο μονών δεσμών μεταξύ ατόμων άνθρακα και αλογόνων και διπλού δεσμού μεταξύ ατόμων άνθρακα.
(05) Η δομή V στερείται ενός μόνο δεσμού μεταξύ ατόμων άνθρακα και ενός μοναδικού δεσμού μεταξύ ατόμων άνθρακα και οξυγόνου.
Σωστές εναλλακτικές λύσεις: 02, 03 και 04.
Εκτός από τον άνθρακα, ένα υποχρεωτικό χημικό στοιχείο σε οργανικές ενώσεις, άλλα στοιχεία μπορεί να υπάρχουν σε δομές και να συνδέονται με ομοιοπολικούς δεσμούς, όπου τα ηλεκτρόνια μοιράζονται.
Το σθένος των στοιχείων καθορίζει τον αριθμό των δεσμών που μπορούν να σχηματιστούν, όπως φαίνεται στον παρακάτω πίνακα.
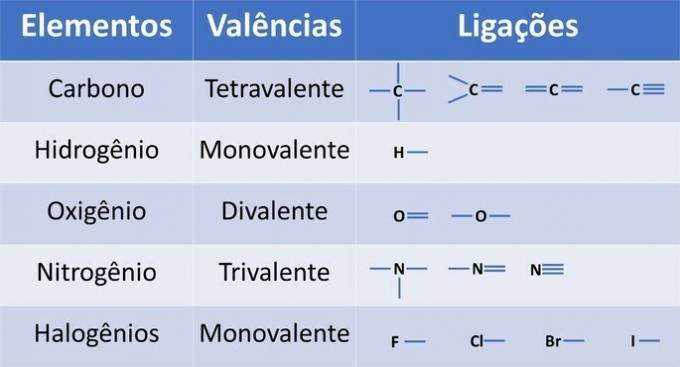
Από αυτές τις πληροφορίες, έχουμε:
(01) ΛΑΘΟΣ. Η δομή στερείται διπλού δεσμού μεταξύ των ατόμων άνθρακα για να σχηματίσει την ένωση αιθανίου.
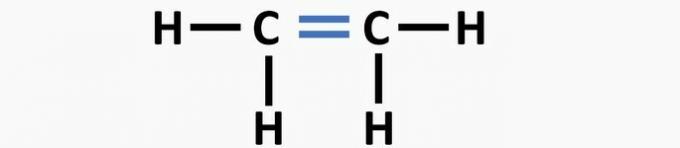
(02) ΣΩΣΤΗ. Η δομή στερείται τριπλού δεσμού μεταξύ των ατόμων άνθρακα για να σχηματίσει την ένωση αιθυνίου.
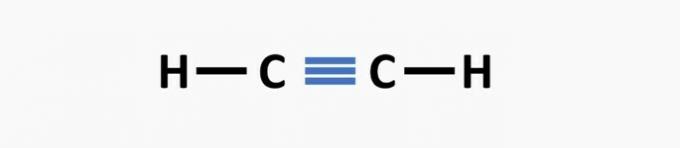
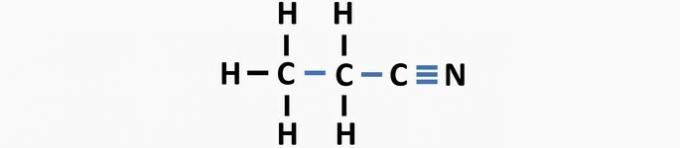
(03) ΣΩΣΤΗ. Η δομή στερείται μονών δεσμών μεταξύ άνθρακα και τριπλών δεσμών μεταξύ άνθρακα και αζώτου για να σχηματίσει την ένωση προπανενιτρίλιο.
(04) ΣΩΣΤΗ. Η δομή στερείται μονών δεσμών μεταξύ άνθρακα και αλογόνου και διπλούς δεσμούς μεταξύ άνθρακα για να σχηματίσει την ένωση διχλωροαιθυλενίου.
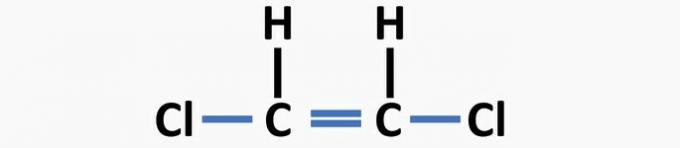
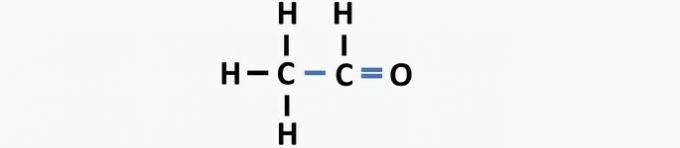
(05) ΛΑΘΟΣ. Η δομή στερείται ενός μόνο δεσμού μεταξύ των ανθράκων και ενός διπλού δεσμού μεταξύ του άνθρακα και του οξυγόνου για να σχηματίσει την αιθανική ένωση.
Ερώτηση 2
(UFPB) Η δομή της οργανικής ένωσης του μοριακού τύπου C5Η8Αυτό που παρουσιάζει μια διακλαδισμένη, ακόρεστη, ετερογενή και αλικυκλική αλυσίδα είναι:

Σωστή εναλλακτική λύση: d.
Οι αλυσίδες άνθρακα μπορούν να ταξινομηθούν ως εξής:
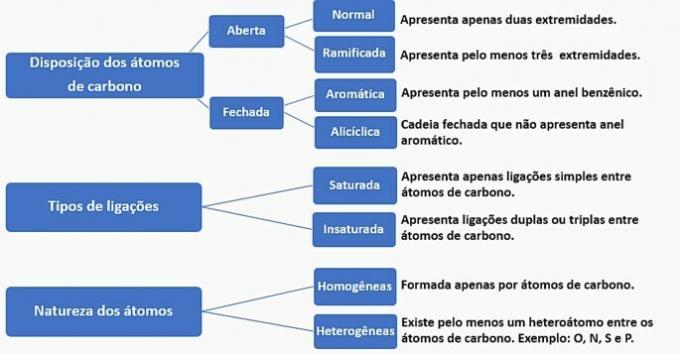
Σύμφωνα με αυτές τις πληροφορίες, έχουμε:
Α) ΛΑΘΟΣ. Η αλυσίδα ταξινομείται ως φυσιολογική, κορεσμένη, ομοιογενής και αλικυκλική.
β) ΛΑΘΟΣ. Η αλυσίδα ταξινομείται ως φυσιολογική, ακόρεστη, ομοιογενής και ανοιχτή.
γ) ΛΑΘΟΣ. Η αλυσίδα ταξινομείται ως διακλαδισμένη, ακόρεστη, ομοιογενής και ανοιχτή.
δ) ΣΩΣΤΗ. Η αλυσίδα ταξινομείται ως διακλαδισμένη, ακόρεστη, ετερογενής και αλικυκλική, ως
- Έχει έναν κλάδο: μεθυλική ρίζα.
- Έχει ακόρεστο: διπλό δεσμό μεταξύ άνθρακα.
- Έχει ένα ετεροάτομο: οξυγόνο συνδεδεμένο με δύο άνθρακες.
- Παρουσιάζει μια κλειστή αλυσίδα: άνθρακες συνδεδεμένους σε κύκλο χωρίς την παρουσία αρωματικού δακτυλίου.
ε) ΛΑΘΟΣ. Η αλυσίδα ταξινομείται ως διακλαδισμένη, ακόρεστη, ετερογενής και ανοιχτή.
ερώτηση 3
(Centec-BA) Στη δομή που φαίνεται παρακάτω, οι αριθμημένοι άνθρακες είναι, αντίστοιχα:
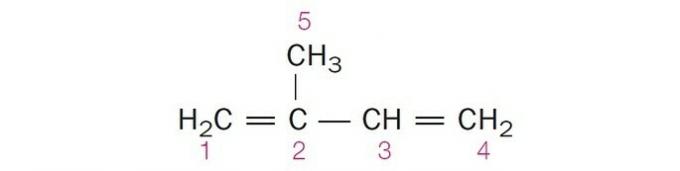
α) sp2, sp, sp2, sp2, sp3.
β) sp, sp3, sp2, sp, sp4.
γ) sp2, sp2, sp2, sp2, sp3.
δ) sp2, sp, sp, sp2, sp3.
ε) sp3, sp, sp2, sp3, sp4.
Σωστή εναλλακτική λύση: c) sp2, sp2, sp2, sp2, sp3.
Επειδή έχει 4 ηλεκτρόνια στο κέλυφος σθένους, ο άνθρακας είναι τετρασθενής, δηλαδή έχει την τάση να σχηματίζει 4 ομοιοπολικούς δεσμούς. Αυτά τα ομόλογα μπορεί να είναι μονό, διπλά ή τριπλά.
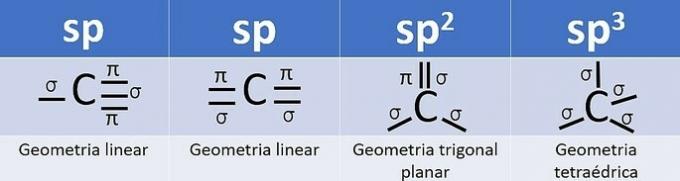
Ο αριθμός των υβριδικών τροχιακών είναι το άθροισμα των δεσμών σίγμα (σ) του άνθρακα, δεδομένου ότι ο δεσμός δεν υβριδοποιείται.
- sp: 2 σύνδεσμοι σίγμα
- sp2: 3 σύνδεσμοι σίγμα
- sp3: 4 σύνδεσμοι σίγμα
Σύμφωνα με αυτές τις πληροφορίες, έχουμε:
Α) ΛΑΘΟΣ. Ο άνθρακας 2 έχει υβριδισμό sp2, καθώς έχει 3 δεσμούς σ και έναν δεσμό .
β) ΛΑΘΟΣ. Ο άνθρακας δεν έχει υβριδισμό sp4 και η υβριδοποίηση sp συμβαίνει όταν υπάρχει τριπλός δεσμός ή δύο διπλοί δεσμοί μεταξύ άνθρακα.
γ) ΣΩΣΤΗ. Το άθροισμα των δεσμών σ σε κάθε άνθρακα δίνει την εναλλακτική υβριδοποίηση.
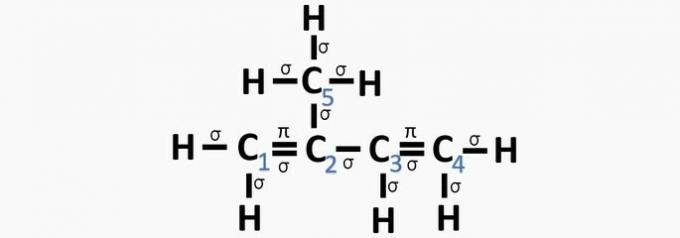
δ) ΛΑΘΟΣ. Η υβριδοποίηση Sp συμβαίνει όταν υπάρχει τριπλός δεσμός ή δύο διπλοί δεσμοί μεταξύ των ανθράκων.
ε) ΛΑΘΟΣ. Ο άνθρακας δεν έχει υβριδισμό sp4 και η υβριδοποίηση sp συμβαίνει όταν υπάρχει τριπλός δεσμός ή δύο διπλοί δεσμοί μεταξύ άνθρακα.
ερώτηση 4
(UFF) Υπάρχει ένα αέριο δείγμα που σχηματίζεται από μία από τις ακόλουθες ενώσεις: CH4; ΝΤΟ2Η4; ΝΤΟ2Η6; ΝΤΟ3Η6 ή Γ3Η8. Εάν 22 g αυτού του δείγματος καταλαμβάνουν όγκο 24,6 L σε πίεση 0,5 atm και θερμοκρασία 27 ° C (Δεδομένου: R = 0,082 L .atm. κ–1. mol–1συμπεραίνεται ότι είναι το αέριο:
α) αιθάνιο.
β) μεθάνιο.
γ) προπάνιο.
δ) προπένιο.
ε) αιθένιο.
Σωστή εναλλακτική λύση: γ) προπάνιο.
1ο βήμα: μετατροπή της μονάδας θερμοκρασίας από Κελσίου σε Kelvin.
2ο βήμα: υπολογίστε τον αριθμό γραμμομορίων της ένωσης χρησιμοποιώντας τη γενική εξίσωση αερίου.
3ο βήμα: υπολογισμός της γραμμομοριακής μάζας της ένωσης.
4ο βήμα: βρείτε τον υδρογονάνθρακα που έχει μοριακή μάζα 44 g / mol.
Μεθάνιο
Αιθίνη
Αιθάνιο
προπυλένιο
Προπάνιο
Έτσι, συμπεραίνεται ότι το αέριο που αντιστοιχεί στις πληροφορίες της δήλωσης είναι προπάνιο.
ερώτηση 5
(ITA) Εξετάστε τις ακόλουθες ουσίες:
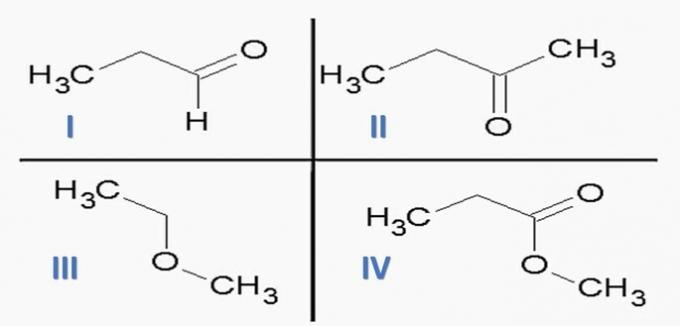
και τις ακόλουθες χημικές λειτουργίες:
Ο. καρβοξυλικό οξύ;
ΣΙ. αλκοόλ;
ντο. αλδεγύδη;
ρε. κετόνη;
και. αστήρ;
φά. αιθέρας.
Η επιλογή που συνδέει ΣΩΣΤΑ τις ουσίες με χημικές λειτουργίες είναι:
α) Αναγνωριστικό; IIc; IIIε; ΕΞΩΣΩΜΑΤΙΚΗ ΓΟΝΙΜΟΠΟΙΗΣΗ.
β) Ic; ΙΙδ; IIIε; ΔΕΞΑΜΕΝΗ
γ) Ic; ΙΙδ; IIIf; Εγώ έχω.
δ) Αναγνωριστικό; IIc; IIIf; Εγώ έχω.
ε) Ια; IIc; IIIε; IVd.
Σωστή εναλλακτική λύση: γ) Ic; ΙΙδ; IIIf; Εγώ έχω.
Οι οργανικές λειτουργίες καθορίζονται από δομές και ομαδοποιούν οργανικές ενώσεις με παρόμοια χαρακτηριστικά.
Οι χημικές λειτουργίες που υπάρχουν στις εναλλακτικές είναι:
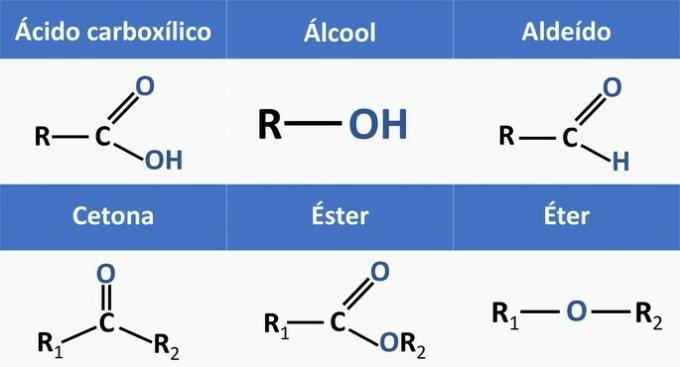
Αναλύοντας τις παραπάνω δομές και τις ενώσεις που υπάρχουν στη δήλωση, έχουμε:
Α) ΛΑΘΟΣ. Οι λειτουργίες του οργάνου είναι σωστές, αλλά η ακολουθία είναι λανθασμένη.
β) ΛΑΘΟΣ. Δεν υπάρχει καρβοξυλικό οξύ μεταξύ των ενώσεων.
γ) ΣΩΣΤΗ. Οι λειτουργικές ομάδες που υπάρχουν στις ενώσεις αντιπροσωπεύουν τις ακόλουθες χημικές λειτουργίες.

δ) ΛΑΘΟΣ. I είναι αλδεΰδη και II είναι κετόνη.
ε) ΛΑΘΟΣ. Δεν υπάρχει καρβοξυλικό οξύ μεταξύ των ενώσεων.
Μάθετε περισσότερα στο: Οργανικές λειτουργίες.
Enem ερωτήσεις
ερώτηση 1
(Enem / 2014) Μία μέθοδος για τον προσδιορισμό της περιεκτικότητας σε αιθανόλη στη βενζίνη συνίσταται στην ανάμιξη γνωστών όγκων νερού και βενζίνης σε μια συγκεκριμένη φιάλη. Αφού ανακινήσετε τη φιάλη και περιμένετε ένα χρονικό διάστημα, μετράται ο όγκος των δύο αναμίξιμων φάσεων που λαμβάνονται: το ένα οργανικό και το άλλο υδατικό. Η αιθανόλη, κάποτε αναμίξιμη με βενζίνη, είναι πλέον αναμίξιμη με νερό.
Για να εξηγήσετε τη συμπεριφορά της αιθανόλης πριν και μετά την προσθήκη νερού, είναι απαραίτητο να γνωρίζετε
α) η πυκνότητα των υγρών.
β) το μέγεθος των μορίων.
γ) το σημείο βρασμού των υγρών.
δ) τα άτομα που υπάρχουν στα μόρια.
ε) τον τύπο αλληλεπίδρασης μεταξύ των μορίων.
Σωστή εναλλακτική λύση: ε) τον τύπο αλληλεπίδρασης μεταξύ των μορίων.
Οι διαμοριακές δυνάμεις επηρεάζουν τη διαλυτότητα των οργανικών ενώσεων. Οι ουσίες τείνουν να διαλύονται μεταξύ τους όταν έχουν την ίδια διαμοριακή δύναμη.
Δείτε στον παρακάτω πίνακα μερικά παραδείγματα οργανικών λειτουργιών και τον τύπο αλληλεπίδρασης μεταξύ μορίων.
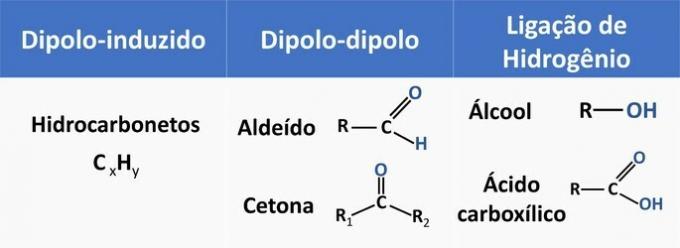
Η αιθανόλη θεωρείται πολικός διαλύτης, καθώς έχει πολική ομάδα (-ΟΗ) στη δομή της. Ωστόσο, η ανθρακική αλυσίδα της, που είναι μη πολική (CH) είναι ικανή να αλληλεπιδρά με μη πολικούς διαλύτες. Επομένως, η αιθανόλη διαλυτοποιείται τόσο στο νερό όσο και στη βενζίνη.
Σύμφωνα με αυτές τις πληροφορίες, έχουμε:
Α) ΛΑΘΟΣ. Η πυκνότητα συνδέει τη μάζα ενός σώματος με τον κατειλημμένο όγκο.
β) ΛΑΘΟΣ. Το μέγεθος των μορίων επηρεάζει την πολικότητα των ενώσεων: όσο μεγαλύτερη είναι η αλυσίδα άνθρακα, τόσο πιο μη πολική γίνεται η ουσία.
γ) ΛΑΘΟΣ. Το σημείο βρασμού είναι χρήσιμο για το διαχωρισμό των μορίων: η απόσταξη διαχωρίζει τις ενώσεις με διαφορετικά σημεία βρασμού. Όσο χαμηλότερο είναι το σημείο βρασμού, τόσο πιο εύκολα εξατμίζεται το μόριο.
δ) ΛΑΘΟΣ. Μια αλδεΰδη έχει άνθρακα, υδρογόνο και οξυγόνο στη δομή της. Αυτή η ένωση εκτελεί αλληλεπιδράσεις διπόλου-διπόλου, ενώ μια αλκοόλη, που έχει τα ίδια στοιχεία, είναι ικανή να σχηματίζει δεσμούς υδρογόνου.
ε) ΣΩΣΤΗ. Η αλληλεπίδραση της αιθανόλης με το νερό (σύνδεση υδρογόνου) είναι πιο έντονη από ό, τι με τη βενζίνη (διπλο-επαγόμενη).
Ερώτηση 2
(Enem / 2013) Τα μόρια του νανοποτάνοι Μοιάζουν με ανθρώπινες μορφές και δημιουργήθηκαν για να τονώσουν το ενδιαφέρον των νέων να κατανοήσουν τη γλώσσα που εκφράζεται σε δομικούς τύπους, που χρησιμοποιούνται ευρέως στη βιολογική χημεία. Ένα παράδειγμα είναι το NanoKid, που απεικονίζεται στο σχήμα:
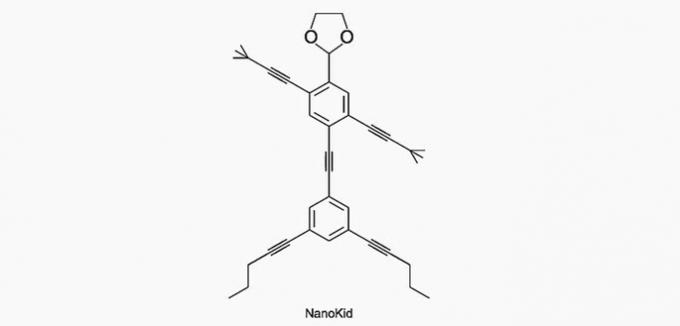
Πού στο σώμα του NanoKid υπάρχει τεταρτοταγής άνθρακας;
α) Χέρια.
β) Επικεφαλής.
γ) Στήθος.
δ) Κοιλιά.
ε) Πόδια.
Σωστή εναλλακτική λύση: α) Χέρια.
Ο άνθρακας ταξινομείται ως εξής:
- Πρωτοβάθμια: συνδέεται με έναν άνθρακα.
- Δευτερεύον: συνδέεται με δύο άνθρακες.
- Τριτοβάθμια: συνδέεται με τρεις άνθρακες.
- Τεταρτογενής: συνδέεται με τέσσερις άνθρακες.
Δείτε τα παρακάτω παραδείγματα.

Σύμφωνα με αυτές τις πληροφορίες, έχουμε:
α) ΣΩΣΤΗ. Ο άνθρακας στο χέρι συνδέεται με τέσσερις άλλους άνθρακες, οπότε είναι τεταρτοταγές.
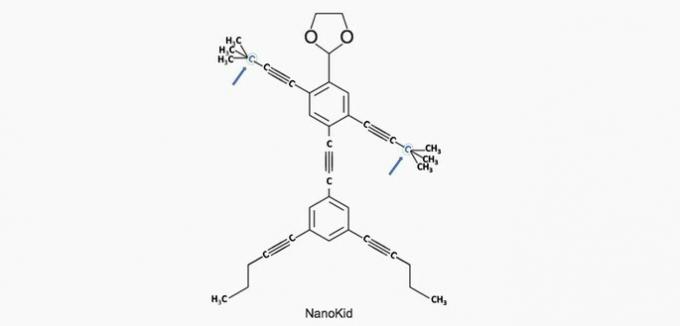
β) ΛΑΘΟΣ. Το κεφάλι αποτελείται από πρωτογενείς άνθρακες.
γ) ΛΑΘΟΣ. Το στήθος αποτελείται από δευτερογενείς και τριτογενείς άνθρακες.
δ) ΛΑΘΟΣ. Η κοιλιά αποτελείται από δευτερεύοντες άνθρακες.
ε) ΛΑΘΟΣ. Τα πόδια είναι κατασκευασμένα από πρωτογενείς άνθρακες.
ερώτηση 3
(Enem / 2014) Ορισμένα πολυμερή υλικά δεν μπορούν να χρησιμοποιηθούν για την παραγωγή ορισμένων τύπων αντικειμένων, ούτε για περιορισμοί των μηχανικών ιδιοτήτων, είτε από την ευκολία με την οποία υποφέρουν από την υποβάθμιση, δημιουργώντας ανεπιθύμητα υποπροϊόντα για αυτό εφαρμογή. Επομένως, η επιθεώρηση καθίσταται σημαντική για τον προσδιορισμό της φύσης του πολυμερούς που χρησιμοποιείται στην κατασκευή του τεχνητού. Μία από τις πιθανές μεθόδους βασίζεται στην αποσύνθεση του πολυμερούς για τη δημιουργία των μονομερών που το προκάλεσαν.
Ελεγχόμενη αποσύνθεση ενός τεχνητού διαμίνης Η2Ν (CH2)6ΝΗ2 και το HO Diacid2Γ (CH2)4CO2Η. Επομένως, το τεχνούργημα κατασκευάστηκε από
α) πολυεστέρας.
β) πολυαμίδιο.
γ) πολυαιθυλένιο.
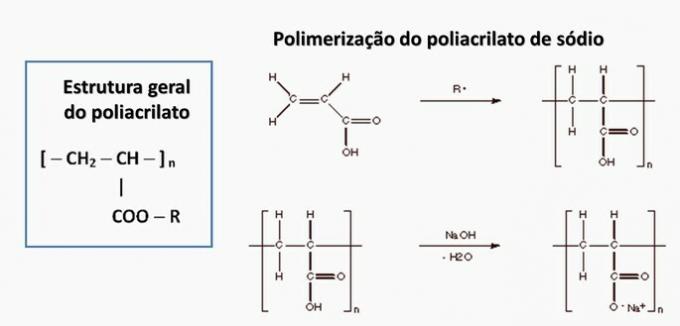
δ) πολυακρυλικό.
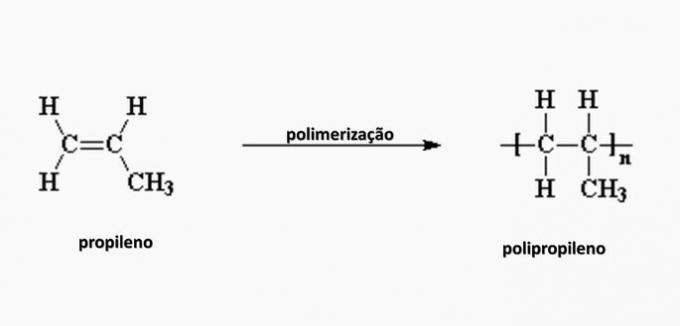
ε) πολυπροπυλένιο.
Σωστή εναλλακτική λύση: β) πολυαμίδιο.
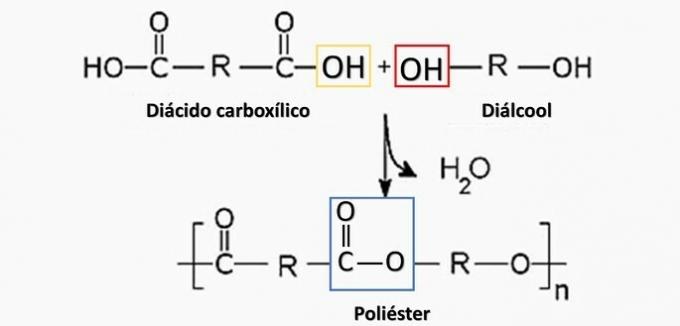
Α) ΛΑΘΟΣ. Ο πολυεστέρας σχηματίζεται στην αντίδραση μεταξύ ενός δικαρβοξυλικού οξέος (-COOH) και μιας διαλκοόλης (-OH).
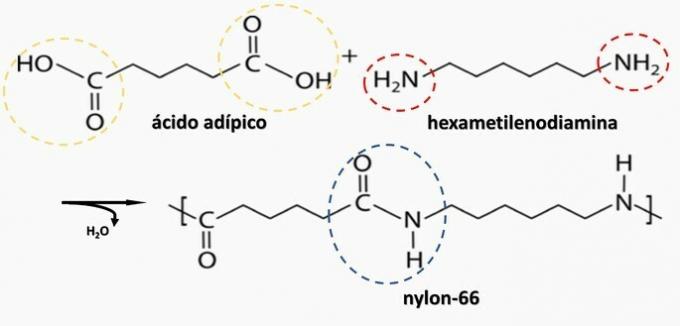
β) ΣΩΣΤΗ. Το πολυαμίδιο σχηματίζεται από τον πολυμερισμό ενός δικαρβοξυλικού οξέος (—COOH) με μια διαμίνη (—ΝΗ2).
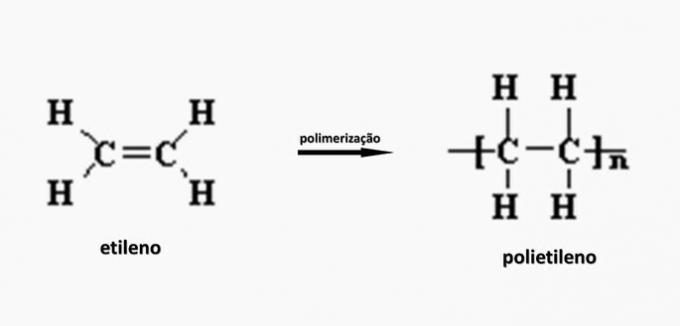
γ) ΛΑΘΟΣ. Το πολυαιθυλένιο σχηματίζεται στον πολυμερισμό του μονομερούς αιθυλενίου.
δ) ΛΑΘΟΣ. Το πολυακρυλικό σχηματίζεται από ένα άλας που προέρχεται από καρβοξυλικό οξύ.
ε) ΛΑΘΟΣ. Το πολυπροπυλένιο σχηματίζεται στον πολυμερισμό του μονομερούς προπυλενίου.
ερώτηση 4
(Enem / 2008) Η Κίνα έχει δεσμευτεί να αποζημιώσει τη Ρωσία για τη διαρροή βενζολίου από μια βιομηχανία Κινεζικά πετροχημικά στον ποταμό Songhua, παραπόταμος του ποταμού Amur, ο οποίος αποτελεί μέρος των συνόρων μεταξύ των δύο χώρες. Ο πρόεδρος της Ομοσπονδιακής Υπηρεσίας Υδατικών Πόρων της Ρωσίας διαβεβαίωσε ότι το βενζόλιο δεν θα φτάσει στους αγωγούς του πόσιμο νερό, αλλά ζήτησε από τον πληθυσμό να βράσει τρεχούμενο νερό και να αποφύγει την αλιεία στον ποταμό Amur και σε αυτό παραπόταμοι. Οι τοπικές αρχές αποθηκεύουν εκατοντάδες τόνους άνθρακα, καθώς το ορυκτό θεωρείται αποτελεσματικό απορροφητικό βενζολίου. Διαδίκτυο: (με προσαρμογές). Λαμβάνοντας υπόψη τα μέτρα που έχουν ληφθεί για την ελαχιστοποίηση των ζημιών στο περιβάλλον και τον πληθυσμό, είναι σωστό να το δηλώσετε αυτό
α) ο άνθρακας, όταν τοποθετείται σε νερό, αντιδρά με βενζόλιο, εξαλείφοντας τον.
β) το βενζόλιο είναι πιο πτητικό από το νερό και, ως εκ τούτου, πρέπει να βράσει.
γ) ο προσανατολισμός για την αποφυγή της αλιείας οφείλεται στην ανάγκη διατήρησης των ψαριών.
δ) το βενζόλιο δεν θα μολύνει τους σωλήνες πόσιμου νερού, καθώς θα αποχύθηκε φυσικά στον πυθμένα του ποταμού.
ε) η ρύπανση που προκαλείται από τη διαρροή βενζολίου της κινεζικής βιομηχανίας θα περιοριζόταν στον ποταμό Songhua.
Σωστή εναλλακτική λύση: β) το βενζόλιο είναι πιο πτητικό από το νερό και επομένως είναι απαραίτητο να βράσει.
Α) ΛΑΘΟΣ. Ο άνθρακας περιέχει στη δομή του αρκετούς πόρους και χρησιμοποιείται ως προσροφητικό, καθώς είναι ικανός να αλληλεπιδρά με μολυσματικούς παράγοντες και να τους συγκρατεί στην επιφάνειά του, αλλά να μην τους εξαλείφει.
β) ΣΩΣΤΗ. Όσο μεγαλύτερη είναι η πτητικότητα μιας ουσίας, τόσο πιο εύκολα μεταβάλλεται σε αέρια κατάσταση. Ενώ το σημείο βρασμού του νερού είναι 100 ° C, αυτό του βενζολίου είναι 80,1 ° C. Αυτό συμβαίνει επειδή το νερό είναι μια πολική ένωση και το βενζόλιο είναι μια μη πολική ένωση.
Ο τύπος αλληλεπιδράσεων που δημιουργούν τα μόρια είναι διαφορετικός και επηρεάζει επίσης το σημείο βρασμού των ουσιών. Το μόριο του νερού είναι ικανό να δημιουργεί δεσμούς υδρογόνου, έναν τύπο αλληλεπίδρασης πολύ ισχυρότερο από αυτό που μπορεί να παράγει το βενζόλιο, με το διεγερμένο δίπολο.
γ) ΛΑΘΟΣ. Σε μια τροφική αλυσίδα, το ένα γίνεται τροφή του άλλου ανάλογα με τις αλληλεπιδράσεις των ειδών σε μια τοποθεσία. Όταν μια τοξική ουσία απελευθερώνεται σε ένα περιβάλλον, υπάρχει προοδευτική συσσώρευση και ψάρια μολυσμένο, όταν καταναλώνεται από τον άνθρωπο, μπορεί να πάρει βενζόλιο μαζί του και να προκαλέσει μεταλλάξεις DNA και ακόμη και ακόμη και καρκίνος.
δ) ΛΑΘΟΣ. Το βενζόλιο έχει χαμηλότερη πυκνότητα από το νερό. Έτσι, η τάση είναι ότι ακόμη και υποβρύχια συνεχίζει να εξαπλώνεται.
ε) ΛΑΘΟΣ. Οι εποχικές αλλαγές μπορούν να αυξήσουν περαιτέρω το πρόβλημα, καθώς οι χαμηλές θερμοκρασίες μειώνουν τη βιολογική ικανότητα αποσύνθεσης των χημικών με τη δράση του ήλιου ή των βακτηρίων.
ερώτηση 5
(Enem / 2019) Οι υδρογονάνθρακες είναι οργανικά μόρια με μια σειρά βιομηχανικών εφαρμογών. Για παράδειγμα, υπάρχουν σε μεγάλες ποσότητες σε διάφορα κλάσματα πετρελαίου και συνήθως διαχωρίζονται με κλασματική απόσταξη με βάση τη θερμοκρασία βρασμού τους. Ο πίνακας παρουσιάζει τα κύρια κλάσματα που λαμβάνονται κατά την απόσταξη του πετρελαίου σε διαφορετικές θερμοκρασίες.
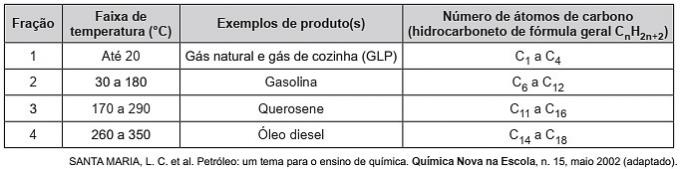
Στο κλάσμα 4, ο διαχωρισμός των ενώσεων συμβαίνει σε υψηλότερες θερμοκρασίες επειδή
α) οι πυκνότητές τους είναι μεγαλύτερες.
β) ο αριθμός των καταστημάτων είναι μεγαλύτερος.
γ) η διαλυτότητά του στο λάδι είναι μεγαλύτερη.
δ) οι διαμοριακές δυνάμεις είναι πιο έντονες.
ε) η αλυσίδα άνθρακα είναι πιο δύσκολο να σπάσει.
Σωστή εναλλακτική λύση: δ) οι διαμοριακές δυνάμεις είναι πιο έντονες.
Οι υδρογονάνθρακες αλληλεπιδρούν από διεγερμένο δίπολο και αυτός ο τύπος διαμοριακής δύναμης εντείνεται με την αύξηση της ανθρακικής αλυσίδας.
Επομένως, τα βαρύτερα κλάσματα πετρελαίου έχουν υψηλότερη θερμοκρασία βρασμού, καθώς οι αλυσίδες αλληλεπιδρούν πιο έντονα από ένα επαγόμενο δίπολο.
Για περισσότερες ασκήσεις, με ανάλυση σχολίων, δείτε επίσης:
- Ασκήσεις σε Υδρογονάνθρακες
- Ασκήσεις σε οργανικές λειτουργίες
- Ερωτήσεις Χημείας στο Enem

