Το μόριο είναι ένα σύνολο ατόμων, το ίδιο ή διαφορετικό, ενωμένο με ομοιοπολικούς δεσμούς.
Αυτά τα χημικά είδη είναι ηλεκτρικά ουδέτερα και αντιπροσωπεύουν τη μονάδα σχηματισμού μιας ουσίας.
Υπάρχουν απλά μόρια όπως το οξυγόνο (O2) του αέρα που αναπνέουμε. Ωστόσο, υπάρχουν επίσης σύνθετες ενώσεις, όπως μπαμπούδες (60 άτομα άνθρακα συνδεδεμένα σε σχήμα σφαίρας), τα οποία είναι τα μεγαλύτερα μόρια που έχουν βρεθεί ποτέ στο διάστημα.
Μελέτη μορίων
Η ομοιοπολική σύνδεση σε ένα μόριο αντιστοιχεί στην κατανομή ηλεκτρονίων, συνήθως μεταξύ μη μεταλλικών στοιχείων.
Δείτε το μόριο του νερού ως παράδειγμα μιας απλής ένωσης.
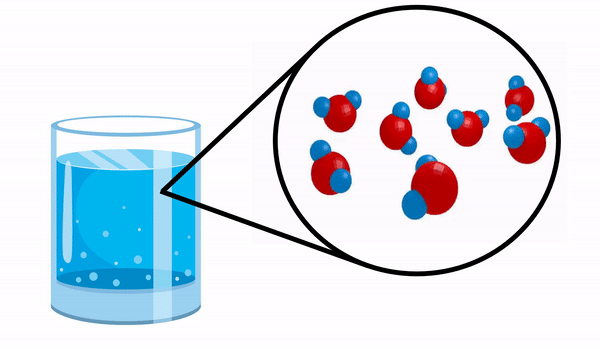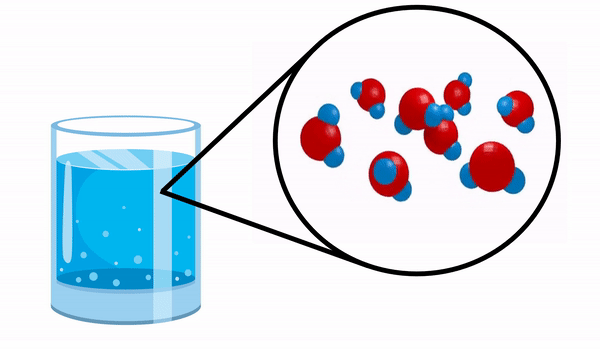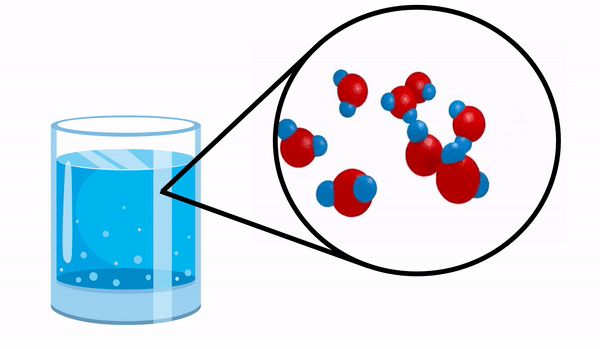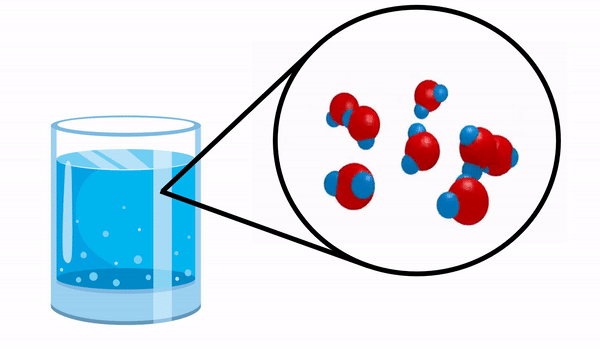
Όταν παρατηρούμε ένα ποτήρι με Νερό δεν έχουμε ιδέα ότι αυτή η ουσία αποτελείται από αρκετά μόρια Η2Ο. Αυτός ο τύπος δείχνει ότι το νερό αποτελείται από 3 άτομα: δύο άτομα υδρογόνου και ένα οξυγόνο, τα οποία μοιράζονται ηλεκτρόνια μεταξύ τους.
Η ζάχαρη, την οποία χρησιμοποιούμε για να γλυκάνουμε τους χυμούς και να φτιάχνουμε κέικ, αποτελείται επίσης από μόρια. Η μονάδα σχηματισμού ζάχαρης είναι η σακχαρόζη.

Αυτό το μόριο είναι πολύ πιο περίπλοκο, καθώς υπάρχουν 45 άτομα συνδεδεμένος. Σχηματίζεται από: 12 άτομα άνθρακα, 22 άτομα υδρογόνου και 11 άτομα οξυγόνου.
Τα μόρια είναι δομές γνωστής μοριακής μάζας, αλλά υπάρχουν επίσης μακρομόρια, τα οποία είναι "γιγαντιαίες δομές" που σχηματίζονται από τόσα πολλά άτομα που η σύνθεσή τους είναι ακόμη και ακαθόριστη. Ένα παράδειγμα αυτού του τύπου είναι το διαμάντι, ένα μακρομόριο που σχηματίζεται από πολλά άτομα άνθρακας σε ένα ομοιοπολικό δίκτυο.
Ομοιοπολικό δεσμό
Ένας ομοιοπολικός χημικός δεσμός δημιουργείται μεταξύ δύο ατόμων όταν μοιράζονται αυτά ηλεκτρόνια πιο εξωτερικά (του σθένους). Τα μόρια μπορούν να έχουν δύο τύπους δεσμών:
Μοριακός ομοιοπολικός δεσμός: το ζευγάρι των ηλεκτρονίων των δύο ατόμων σύνδεσης είναι κοινόχρηστα.

Ομοιοπολικό ομοιοπολικό δεσμό (γενικό): τα κοινόχρηστα ηλεκτρόνια προέρχονται από ένα μόνο από τα εμπλεκόμενα άτομα.
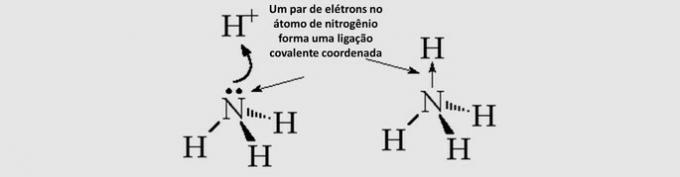
Μοριακή Γεωμετρία
Όταν σχηματίζεται ένα μόριο, τα άτομα τοποθετούνται με διαφορετικούς τρόπους, έτσι ώστε η χωρική διάταξη να είναι πιο σταθερή. Επομένως, τα σύνθετα υλικά έχουν διαφορετικές γεωμετρίες.
Εδώ είναι μερικές από τις γεωμετρίες που μπορούν να έχουν τα μόρια.
| Μοριακή Γεωμετρία | ||
|---|---|---|
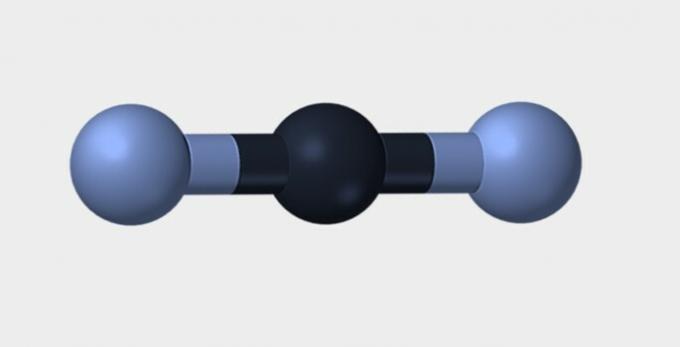
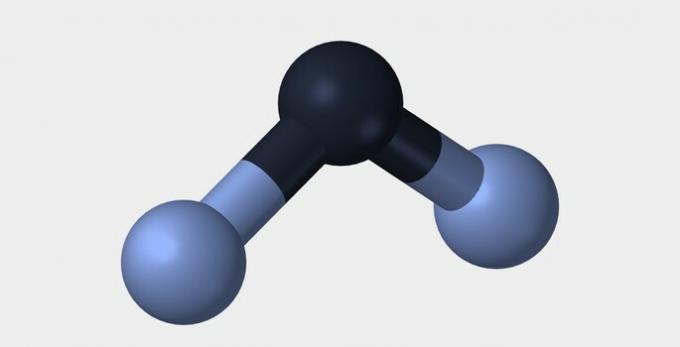
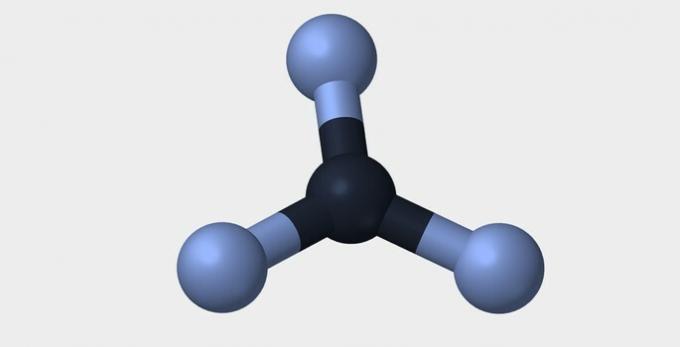
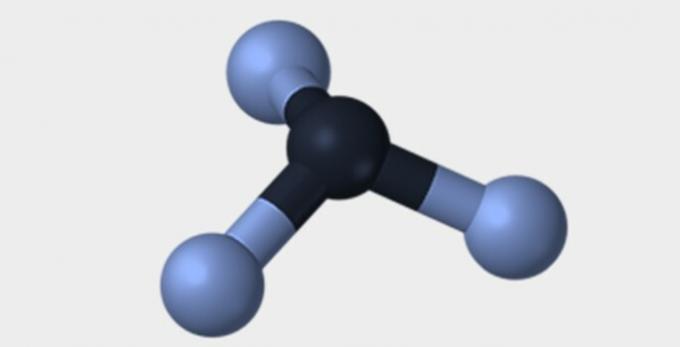
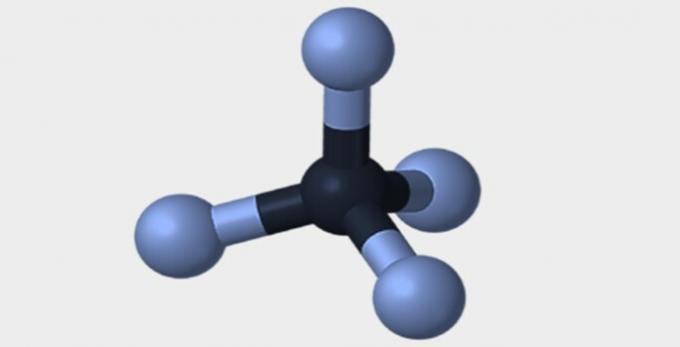
| Γραμμικός | Γωνιώδης | Τριγωνικός |
 |
 |
 |
| Πυραμιδικός | τετράεδρος | οκτάεδρος |
 |
 |
 |
Πολικά και μη πολικά μόρια
Τα μόρια ταξινομούνται σύμφωνα με το πόλωση.
μη πολικά μόρια: δεν υπάρχει διαφορά στην ηλεκτροπαραγωγικότητα μεταξύ ατόμων.
| Άζωτο (Ν2) | διοξείδιο του άνθρακα (CO2) |
|---|---|
 |
 |
Άζωτο (Ν2) είναι ένα μη πολικό μόριο επειδή σχηματίζεται από το ίδιο χημικό στοιχείο και ως εκ τούτου δεν υπάρχει διαφορά στην ηλεκτροπαραγωγικότητα. διοξείδιο του άνθρακα (CO2) είναι μη πολική λόγω της γραμμικής γεωμετρίας της, η οποία σταθεροποιεί την έλξη οξυγόνου από τα ηλεκτρόνια.
πολικά μόρια: υπάρχει διαφορά στην ηλεκτροπαραγωγικότητα μεταξύ των ατόμων, με θετικό πόλο και αρνητικό πόλο.
| Νερό (Η2Ο) | Αμμωνία (NH3) |
|---|---|
 |
 |
Και στα δύο παραδείγματα, βλέπουμε ότι τα κεντρικά άτομα, το οξυγόνο και το άζωτο, έχουν ζεύγη ηλεκτρονίων χωρίς ζεύγη που σχηματίζουν σύννεφα ηλεκτρονίων. Δεδομένου ότι υπάρχουν περισσότερα ηλεκτρονικά σύννεφα γύρω από τα κεντρικά άτομα από ό, τι υπάρχουν καθιερωμένοι χημικοί δεσμοί, τα μόρια είναι πολικά.
Παραδείγματα μορίων
| Ουσία | Χαρακτηριστικά | Μόριο | Τύπος |
|---|---|---|---|
| Υδρογόνο | Καύσιμο και άφθονο στον φλοιό της γης. | 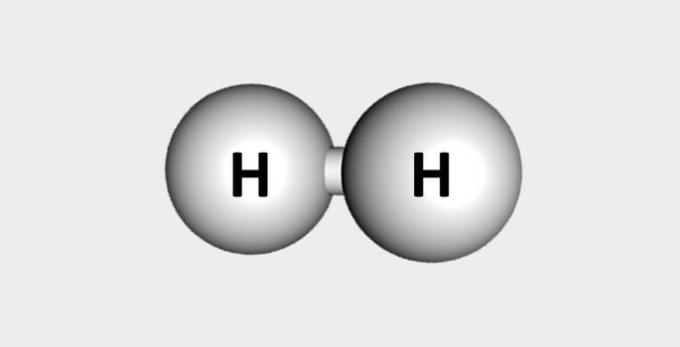 |
Η2 |
| Οξυγόνο | Απαραίτητο για την αναπνοή και συμμετέχει σε διάφορες χημικές αντιδράσεις | 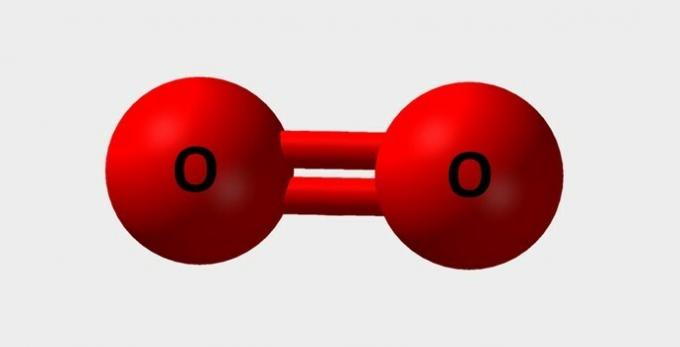 |
Ο2 |
| Θείο | Κίτρινη σκόνη που χρησιμοποιείται για την παρασκευή βαφών. | 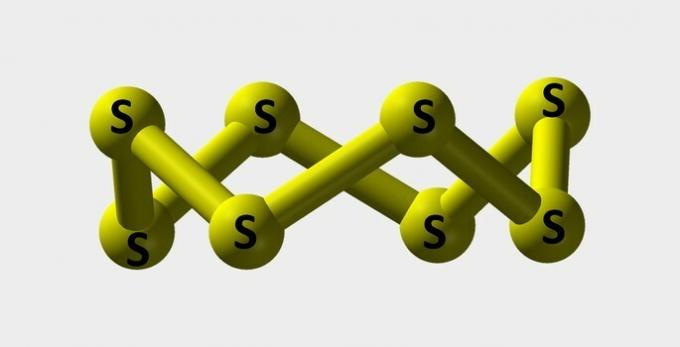 |
μικρό8 |
| Διοξείδιο του άνθρακα | Χρησιμοποιείται σε πυροσβεστήρες και ψυκτικά μέσα. | 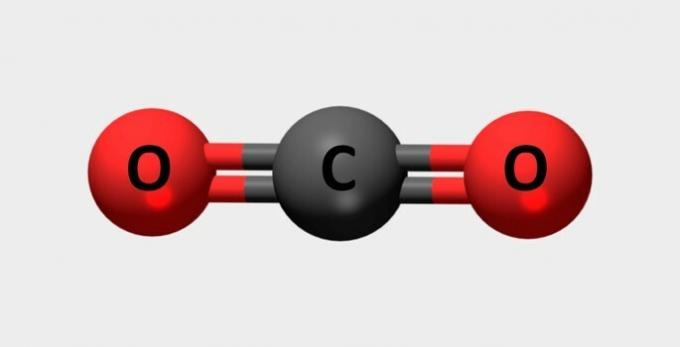 |
CO2 |
| Αιθανόλη | Κοινό αλκοόλ που χρησιμοποιείται ως καύσιμο και σε αρώματα. | 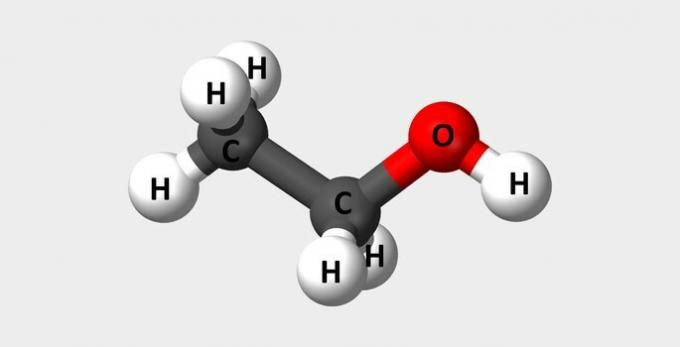 |
ΝΤΟ2Η6Ο |
Φροντίστε να δείτε αυτά τα κείμενα σε θέματα που σχετίζονται με αυτά που μόλις μάθατε:
- Βιομόρια
- ΟΡΓΑΝΙΚΕΣ ΕΝΩΣΕΙΣ
- Μοριακή μάζα
- Κανόνας Octet
- Χημικοί δεσμοί
- Πολικότητα σύνδεσης
- Διαμοριακές δυνάμεις

