Ο Διάγραμμα φάσεων είναι ένα γράφημα που σας επιτρέπει να ορίσετε σε ποια φυσική κατάσταση βρίσκεται μια ουσία ανά πάσα στιγμή, γνωρίζοντας τη θερμοκρασία και την πίεση.
Οι εργαστηριακές μετρήσεις χρησιμοποιούνται για την κατασκευή του διαγράμματος φάσης μιας δεδομένης ουσίας.
Το διάγραμμα χωρίζεται σε τρεις περιοχές, οι οποίες αντιπροσωπεύουν την κατάσταση στερεών, υγρών και ατμών.
Οι τελείες στις γραμμές που οριοθετούν αυτές τις περιοχές υποδηλώνουν τις τιμές της θερμοκρασίας και της πίεσης που μπορεί να έχει η ουσία σε δύο καταστάσεις.
Ένα διάγραμμα φάσης έχει τα ακόλουθα στοιχεία:
- καμπύλη του Σύντηξη: διαχωρίζει τις περιοχές που αντιστοιχούν σε στερεές και υγρές καταστάσεις.
- καμπύλη του εξάτμιση: διαχωρίζει τις περιοχές που αντιστοιχούν στις φάσεις υγρού και ατμού.
- καμπύλη του εξάχνιση: διαχωρίζει τις περιοχές που αντιστοιχούν στις φάσεις στερεών και ατμών.
- τριπλό σημείο: σημείο τομής των τριών καμπυλών (σύντηξη, εξάτμιση και εξάχνωση). Αυτό το σημείο δείχνει τις τιμές θερμοκρασίας και πίεσης που η ουσία μπορεί ταυτόχρονα να βρίσκεται στις τρεις καταστάσεις.
- Κρίσιμο σημείο: υποδεικνύει την υψηλότερη θερμοκρασία που η ουσία είναι ατμός. Από εκεί και πέρα, δεν είναι πλέον δυνατόν να γίνει διάκριση μεταξύ υγρών και ατμών. Σε θερμοκρασίες πάνω από το κρίσιμο σημείο, η ουσία γίνεται αέριο.
Στο παρακάτω σχήμα, παρουσιάζουμε μια αναπαράσταση ενός διαγράμματος φάσης:

Διαβάστε περισσότερα στο: Η φυσική κατάσταση αλλάζει.
καμπύλη τήξης
Οι ουσίες, γενικά, αυξάνουν τον όγκο όταν υφίστανται σύντηξη και, αντίθετα, μειώνονται στον όγκο όταν στερεοποιούνται. Κατά συνέπεια, η αύξηση της πίεσης οδηγεί σε αύξηση του σημείου τήξης (θερμοκρασία τήξης).
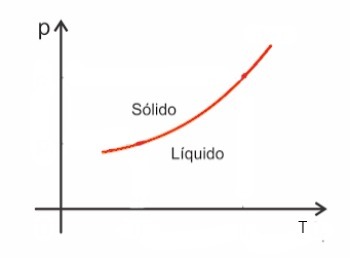
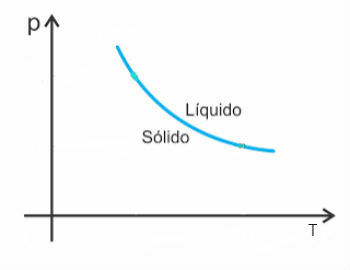
Ωστόσο, υπάρχουν μερικές εξαιρέσεις ανάμεσά τους το νερό, το οποίο κατά την τήξη μειώνεται στον όγκο. Σε αυτήν την περίπτωση, μια αύξηση της πίεσης προκαλεί μείωση του σημείου τήξεως.
Έτσι, η καμπύλη τήξης αυτών των ουσιών θα έχει την εξής μορφή:
Παράδειγμα
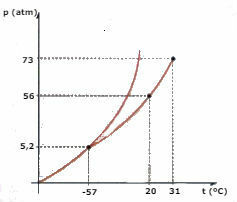
Εξετάστε το διάγραμμα φάσης CO2 (διοξείδιο του άνθρακα) που παρουσιάζεται παρακάτω και απαντά στις ερωτήσεις:
α) Ποια φάση είναι το CO2 , όταν η θερμοκρασία είναι -60 ºC και η πίεση είναι 50 atm;
β) Μια ορισμένη ποσότητα CO2 Το υγρό υπόκειται σε πίεση 56 atm, και περιορίζεται σε δοχείο. Εάν το υγρό θερμαίνεται, διατηρώντας την πίεση σταθερή, ποια είναι η τιμή θερμοκρασίας στην οποία θα συμβεί εξάτμιση;
γ) Ποια είναι η θερμοκρασία και η τιμή πίεσης του τριπλού σημείου CO2?
δ) Ένα κομμάτι ξηρού πάγου (CO2) υπόκειται σε πίεση 2 atm. Θερμαίνεται, διατηρώντας σταθερή πίεση. Σε μια συγκεκριμένη στιγμή αρχίζει να εμφανίζεται μια αλλαγή φάσης. Ποιο είναι το όνομα αυτής της αλλαγής;
Ανάλυση:
α) Παρατηρώντας το διάγραμμα, συμπεραίνουμε ότι το CO2 θα είναι στη σταθερή φάση.
β) Η εξάτμιση θα συμβεί όταν η θερμοκρασία φτάσει τους 20 ° C.
γ) Το τριπλό σημείο αντιστοιχεί στη διασταύρωση των τριών καμπυλών, στην περίπτωση CO2, όταν έχει θερμοκρασία -57 ° C και πίεση 5,2 atm, οι τρεις φυσικές καταστάσεις μπορούν να συνυπάρχουν.
δ) Θα συμβεί εξάχνωση
Για να μάθετε περισσότερα, διαβάστε επίσης:
- Στερεοποίηση
- Σημείο τήξεως και βρασμού
- Εξάτμιση
- Συμπύκνωση
Λύσεις ασκήσεις
1) Enem - 2000
Ακόμα και σήμερα, είναι πολύ κοινό για τους ανθρώπους να χρησιμοποιούν πήλινα δοχεία (βάζα ή κεραμικά δοχεία χωρίς υαλοπίνακες) για τη διατήρηση του νερού σε θερμοκρασία χαμηλότερη από εκείνη του περιβάλλοντος. Αυτό είναι επειδή:
α) ο πηλός απομονώνει νερό από το περιβάλλον, διατηρώντας το πάντα σε χαμηλότερη θερμοκρασία από το δικό του, σαν να ήταν φελιζόλ.
β) ο πηλός έχει τη δύναμη να «παγώσει» νερό λόγω της χημικής του σύνθεσης. Στην αντίδραση, το νερό χάνει θερμότητα.
γ) ο πηλός είναι πορώδης, επιτρέποντας στο νερό να περάσει μέσα από αυτό. Μέρος αυτού του νερού εξατμίζεται, λαμβάνοντας θερμότητα από το Mororing και το υπόλοιπο νερό, το οποίο στη συνέχεια ψύχεται.
δ) ο πηλός είναι πορώδης, επιτρέποντας στο νερό να καθιζάνει στο εξωτερικό της κανάτας. Το εξωτερικό νερό είναι πάντα σε υψηλότερη θερμοκρασία από το εσωτερικό.
ε) Το Moringa είναι ένα είδος φυσικού ψυγείου, απελευθερώνοντας υγροσκοπικές ουσίες που φυσικά μειώνουν τη θερμοκρασία του νερού.
Εναλλακτική γ: ο πηλός είναι πορώδης, επιτρέποντας στο νερό να περάσει. Μέρος αυτού του νερού εξατμίζεται, λαμβάνοντας θερμότητα από το Mororing και το υπόλοιπο νερό, το οποίο στη συνέχεια ψύχεται.
2) Ita - 2013
Εξετάστε το υποθετικό διάγραμμα φάσης που απεικονίζεται σχηματικά στο ακόλουθο σχήμα:

Τι αντιπροσωπεύουν τα σημεία A, B, C, D και E;
σημείο Α: σημείο εξάχνωσης
σημείο Β: τριπλό σημείο
Σημείο C: σημείο τήξης / στερεοποίησης
σημείο Δ: σημείο εξάτμισης / συμπύκνωσης
σημείο Ε: κρίσιμο σημείο
3) UECE - 2009
Κοιτάζοντας το διάγραμμα φάσης PT που φαίνεται παρακάτω. Μπορεί να συναχθεί, σωστά, ότι μια ουσία που έχει περάσει από τη διαδικασία εξάχνωσης ακολουθεί την τροχιά:

α) Χ ή Υ
β) Y ή U
γ) U ή V
δ) T ή X
Εναλλακτική β: Y ή U