Ο περιοδικός πίνακας είναι ένα σημαντικό εργαλείο μελέτης που συγκεντρώνει πληροφορίες για όλα τα γνωστά χημικά στοιχεία.
Δοκιμάστε τις γνώσεις σας με αυτήν τη λίστα 17 ερωτήσεις με τις διαφορετικές προσεγγίσεις για το θέμα και λύστε τις αμφιβολίες σας με τα ψηφίσματα που σχολιάστηκαν μετά τα σχόλια.
Για να κατανοήσετε τις ερωτήσεις, χρησιμοποιήστε το Περιοδικός Πίνακας πλήρης και ενημερωμένη.
Οργάνωση περιοδικού πίνακα
ερώτηση 1
(UFU) Στις αρχές του 19ου αιώνα, με την ανακάλυψη και την απομόνωση πολλών χημικών στοιχείων, έγινε απαραίτητο να ταξινομηθούν ορθολογικά, προκειμένου να διεξαχθούν συστηματικές μελέτες. Προστέθηκαν πολλές συνεισφορές μέχρι την επίτευξη της τρέχουσας περιοδικής ταξινόμησης των χημικών στοιχείων. Όσον αφορά την τρέχουσα περιοδική ταξινόμηση, απαντήστε:
α) Πώς αναφέρονται τα στοιχεία διαδοχικά στον περιοδικό πίνακα;
Ο περιοδικός πίνακας οργανώνεται σε ακολουθίες χημικών στοιχείων σε αύξουσα σειρά ατομικός αριθμός. Αυτός ο αριθμός αντιστοιχεί στον αριθμό των πρωτονίων στον πυρήνα του ατόμου.
Αυτή η μέθοδος οργάνωσης προτάθηκε από τον Henry Moseley όταν αναδιαμόρφωσε τον πίνακα που πρότεινε ο Dmitri Mendeleiev.
Ένα στοιχείο μπορεί να εντοπιστεί στον πίνακα από την οικογένεια και την περίοδο κατά την οποία εισάγεται. Αυτή η διανομή πραγματοποιείται ως εξής:
| ομάδες ή οικογένειες | 18 κάθετες ακολουθίες |
| Ομάδες στοιχείων που έχουν παρόμοια χαρακτηριστικά. |
| Εμμηνα | 7 οριζόντιες ακολουθίες |
| Αριθμός ηλεκτρονικών επιπέδων που διαθέτει το στοιχείο. |
β) Ποιες ομάδες του περιοδικού πίνακα μπορούν να βρεθούν: αλογόνο, μέταλλο αλκαλίου, μέταλλο αλκαλικής γαίας, χαλκογόνο και ευγενές αέριο;
Η ταξινόμηση των στοιχείων σε ομάδες γίνεται σύμφωνα με τις ιδιότητες. Τα στοιχεία που βρίσκονται στην ίδια ομάδα έχουν παρόμοια χαρακτηριστικά και για τις ταξινομήσεις που δίνονται πρέπει:
| Ταξινόμηση | Ομάδα | Οικογένεια | Στοιχεία |
| αλαγόνο | 17 | 7Α | F, Cl, Br, I, At και Ts |
| αλκαλι μέταλλο | 1 | 1Α | Li, Na, K, Rb, Cs και Fr |
| μέταλλο αλκαλικής γαίας | 2 | 2Α | Be, Mg, Ca, Sr, Ba και Ra |
| χαλκογόνο | 16 | 6Α | O, S, Se, Te, Po και Lv |
| ευγενες αεριο | 18 | 8Α | Αυτός, Ne, Ar, Kr, Xe, Rn και Og |
Ερώτηση 2
(PUC-SP) Επιλύστε το ζήτημα με βάση την ανάλυση των παρακάτω δηλώσεων.
I - Ο τρέχων σύγχρονος περιοδικός πίνακας είναι διατεταγμένος σε αύξουσα σειρά ατομικής μάζας.
II - Όλα τα στοιχεία που έχουν 1 ηλεκτρόνιο και 2 ηλεκτρόνια στο κέλυφος σθένους είναι, αντίστοιχα, μέταλλα αλκαλίων και μέταλλα αλκαλικών γαιών, υπό τον όρο ότι ο κύριος κβαντικός αριθμός αυτού του επιπέδου (n 1).
III - Την ίδια περίοδο, τα στοιχεία παρουσιάζουν τον ίδιο αριθμό επιπέδων (επίπεδα).
IV - Στην ίδια ομάδα (οικογένεια), τα στοιχεία έχουν τον ίδιο αριθμό επιπέδων (επίπεδα).
Συνάγεται το συμπέρασμα ότι, όσον αφορά τον τρέχοντα περιοδικό πίνακα χημικών στοιχείων, είναι σωστά:
α) I και IV (μόνο).
β) I και II (μόνο).
γ) II και III (μόνο).
δ) II και IV (μόνο).
ε) III και IV (μόνο).
Σωστή εναλλακτική λύση: γ) II και III (μόνο).
Αναλύοντας κάθε εναλλακτική λύση πρέπει:
ΕΓΩ ΛΑΘΟΣ. Τα στοιχεία διατάσσονται με αύξουσα σειρά ατομικού αριθμού.
II - ΣΩΣΤΗ. Τα ηλεκτρόνια στο κέλυφος σθένους ορίζουν την ομάδα στην οποία βρίσκεται το στοιχείο.
| αλκαλι μέταλλα | 1 ηλεκτρόνιο στο κέλυφος σθένους |
| 3ανάγνωση | 2-1 |
| 11Στο | 2-8-1 |
| 19κ | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87Πρ | 2-8-18-32-18-8-1 |
| μέταλλα αλκαλικών γαιών | 2 ηλεκτρόνια στο κέλυφος σθένους |
| 4είναι | 2-2 |
| 12mg | 2-8-2 |
| 20Εδώ | 2-8-8-2 |
| 38κύριος | 2-8-18-8-2 |
| 56Μπα | 2-8-18-18-8-2 |
| 88Βάτραχος | 2-8-18-32-18-8-2 |
Ο κύριος κβαντικός αριθμός αντιστοιχεί στο κέλυφος στο οποίο βρίσκεται το ηλεκτρόνιο, που διαφέρει από το 1 επειδή από την ηλεκτρονική διανομή παρατηρούμε ότι η θέση του ηλεκτρονίου είναι από το δεύτερο κέλυφος ή n = 2.
III - ΣΩΣΤΗ. Η θέση ενός στοιχείου σε μια συγκεκριμένη περίοδο οφείλεται στον αριθμό των επιπέδων κατά την ηλεκτρονική διανομή.
| Εμμηνα | 7 οριζόντιες ακολουθίες |
| 1η περίοδος | 1 στρώμα: Κ |
| 2η περίοδος | 2 στρώματα: K, L |
| 3η περίοδος | 3 στρώματα: K, L, M |
| 4η περίοδος | 4 στρώματα: K, L, M, N |
| 5η περίοδος | 5 στρώματα: K, L, M, N, O |
| 6η περίοδος | 6 στρώματα: K, L, M, N, O, P |
| 7η περίοδος | 7 επίπεδα: K, L, M, N, O, P, Q |
Παράδειγμα: χημικό στοιχείο που βρίσκεται στη δεύτερη περίοδο.
IV - ΛΑΘΟΣ. Τα στοιχεία που ανήκουν στην ίδια ομάδα έχουν παρόμοια χαρακτηριστικά και αυτό οφείλεται στο γεγονός ότι έχουν τον ίδιο αριθμό ηλεκτρονίων στο κέλυφος σθένους.
Παράδειγμα:
| Βηρύλλιο | Μαγνήσιο |
|
2 ηλεκτρόνια σε στρώμα σθένους. |
2 ηλεκτρόνια σε στρώμα σθένους. |
Επομένως, το βηρύλλιο και το μαγνήσιο αποτελούν μέρος της ομάδας 2 του περιοδικού πίνακα.
ερώτηση 3
(Unitins) Όσον αφορά τη σύγχρονη περιοδική ταξινόμηση των στοιχείων, προσδιορίστε την πραγματική δήλωση:
α) σε μια οικογένεια, τα στοιχεία έχουν γενικά τον ίδιο αριθμό ηλεκτρονίων στο τελευταίο κέλυφος.
β) στον περιοδικό πίνακα, τα χημικά στοιχεία τοποθετούνται σε φθίνουσα σειρά ατομικών μαζών.
γ) σε μια οικογένεια, τα στοιχεία έχουν πολύ διαφορετικές χημικές ιδιότητες.
δ) σε μια περίοδο, τα στοιχεία έχουν παρόμοιες χημικές ιδιότητες.
ε) όλα τα αντιπροσωπευτικά στοιχεία ανήκουν στην ομάδα Β του περιοδικού πίνακα.
Σωστή εναλλακτική λύση: α) σε μια οικογένεια, τα στοιχεία έχουν γενικά τον ίδιο αριθμό ηλεκτρονίων στο τελευταίο κέλυφος.
α) ΣΩΣΤΗ. Χημικά στοιχεία της ίδιας οικογένειας έχουν τον ίδιο αριθμό ηλεκτρονίων στο τελευταίο κέλυφος και αυτό τα κάνει να έχουν παρόμοια χαρακτηριστικά.
β) ΛΑΘΟΣ. Οι ατομικές μάζες αυξάνονται καθώς ο ατομικός αριθμός του στοιχείου αυξάνεται.
γ) ΛΑΘΟΣ. Οι χημικές ιδιότητες των στοιχείων είναι παρόμοιες, επομένως ομαδοποιούνται στην ίδια οικογένεια.
δ) ΛΑΘΟΣ. Ταυτόχρονα, τα στοιχεία έχουν τα ηλεκτρόνια τους κατανεμημένα στον ίδιο αριθμό κελυφών.
ε) ΛΑΘΟΣ. Τα αντιπροσωπευτικά στοιχεία ανήκουν στην ομάδα Α, η οποία αντιστοιχεί στις οικογένειες: 1A, 2A, 3A, 4A, 5A, 6A, 7A και 8A. Τα στοιχεία που ανήκουν στην ομάδα Β είναι στοιχεία μετάβασης.
ερώτηση 4
(Vunesp) Λαμβάνοντας υπόψη τις ιδιότητες των χημικών στοιχείων και τον περιοδικό πίνακα, δεν είναι σωστό να αναφέρετε:
α) ένα μέταλλο είναι μια ουσία που διεξάγει ηλεκτρικό ρεύμα, είναι όλκιμο και ελατό.
β) ένα μη μέταλλο είναι μια ουσία που δεν αγωγεί ηλεκτρικό ρεύμα, δεν είναι όλκιμο ούτε ελατό.
γ) ένα ημιμετάλλο έχει τη φυσική εμφάνιση ενός μετάλλου, αλλά χημική συμπεριφορά παρόμοια με εκείνη ενός μη μετάλλου.
δ) τα περισσότερα χημικά στοιχεία αποτελούνται από μη μέταλλα.
ε) τα ευγενή αέρια είναι μονοατομικά.
Λανθασμένη εναλλακτική λύση: δ) τα περισσότερα χημικά στοιχεία είναι μη μέταλλα.
Σημειώστε την ταξινόμηση των χημικών στοιχείων στον περιοδικό πίνακα σε μέταλλα, μη μέταλλα και ημιμέταλλα.

Όπως μπορούμε να δούμε, τα περισσότερα στοιχεία είναι μέταλλα.
α) ΣΩΣΤΗ. Τα μέταλλα μεταφέρουν ηλεκτρισμό λόγω των σύννεφων ηλεκτρονίων που σχηματίζονται από ελεύθερα ηλεκτρόνια, τα οποία είναι χαρακτηριστικά της δομής τους. Είναι όλκιμα επειδή μπορούν να μετατραπούν σε σύρματα ή φύλλα, ανάλογα με την περιοχή όπου ασκείται πίεση. Είναι επίσης ελαστικά, καθώς μπορούν να παραχθούν πολύ λεπτά φύλλα με αυτόν τον τύπο υλικού.
β) ΣΩΣΤΗ. Τα μη μέταλλα έχουν τα αντίθετα χαρακτηριστικά των μετάλλων. Αντί για αγωγούς, είναι καλοί θερμικοί μονωτές και, καθώς είναι εύθραυστοι, δεν διαμορφώνονται σε σύρματα ή φύλλα καθώς δεν έχουν καλή ολκιμότητα και ελαστικότητα.
γ) ΣΩΣΤΗ. Τα ημιμετάλλα έχουν χαρακτηριστικά ενδιάμεσα με μέταλλα και μη μέταλλα. Όντας ημιαγωγοί ηλεκτρικής ενέργειας, έχουν μεταλλική γυαλάδα αλλά είναι εύθραυστα σαν μη μέταλλα.
δ) ΛΑΘΟΣ. Τα περισσότερα στοιχεία ταξινομούνται ως μέταλλα. Οι κατηγορίες μετάλλων που υπάρχουν στον περιοδικό πίνακα είναι: αλκαλική, αλκαλική γη, μεταβατική εσωτερική και εξωτερική.
ε) ΣΩΣΤΗ. Τα ευγενή αέρια είναι μονοατομικά, έτσι αντιπροσωπεύονται μόνο από τα αρχικά τους.
Παράδειγμα:
| ευγενες αεριο | χαλκογόνο |
| Ήλιο (Αυτός) | Οξυγόνο (Ο2) |
| μονοατομική: σχηματίζεται από ένα άτομο | διατομική: σχηματίζεται από δύο άτομα |
Λόγω της σταθερότητας των ευγενών αερίων, τα στοιχεία αυτής της οικογένειας έχουν χαμηλή αντιδραστικότητα και είναι επίσης γνωστά ως αδρανή.
ερώτηση 5
Σχετικά με την οργάνωση του τρέχοντος περιοδικού πίνακα, απαντήστε:
α) Τι είναι οι στήλες;
β) Ποιες είναι οι γραμμές;
γ) Ποια είναι η μέθοδος που χρησιμοποιείται για την οργάνωση των χημικών στοιχείων;
Απαντήσεις:
α) οι στήλες είναι οι ομάδες του Περιοδικού Πίνακα, παλαιότερα καλούμενες οικογένειες, που συγκεντρώνουν χημικά στοιχεία με παρόμοιες ιδιότητες.
β) Οι γραμμές είναι οι περίοδοι του Περιοδικού Πίνακα και δείχνουν τον αριθμό των ηλεκτρονικών στρωμάτων ενός ατόμου στην κατάσταση του εδάφους.
γ) Τα χημικά στοιχεία στον τρέχοντα Περιοδικό Πίνακα είναι διατεταγμένα σε αύξουσα σειρά ατομικού αριθμού, που δείχνει τον αριθμό των πρωτονίων στον πυρήνα του ατόμου.
Περιοδικές οικογένειες πίνακα
ερώτηση 1
(CESGRANRIO) Κάνοντας τη σχέση μεταξύ των παρακάτω στηλών, οι οποίες αντιστοιχούν στις οικογένειες στοιχείων σύμφωνα με τον περιοδικό πίνακα, η αριθμητική ακολουθία θα είναι:
| 1. ευγενή αέρια | • Ομάδα 1Α |
| 2. αλκαλι μέταλλα | • Ομάδα 2Α |
| 3. μέταλλα αλκαλικών γαιών | • Ομάδα 6Α |
| 4. Χαλκογόνα | • Ομάδα 7Α |
| 5. Αλογόνα | • Ομάδα 0 |
α) 1, 2, 3, 4, 5.
β) 2, 3, 4, 5, 1.
γ) 3, 2, 5, 4, 1.
δ) 3, 2, 4, 5, 1.
ε) 5, 2, 4, 3, 1.
Σωστή εναλλακτική λύση: β) 2, 3, 4, 5, 1.
| ομάδες | ηλεκτρονική διαμόρφωση |
| • Ομάδα 1Α: 2. αλκαλι μέταλλα | μας1 (με n |
| • Ομάδα 2Α: 3. μέταλλα αλκαλικών γαιών | μας2 (με n |
| • Ομάδα 6Α: 4. Χαλκογόνα | μας2np4 |
| • Ομάδα 7Α: 5. Αλογόνα | μας2np5 |
| • Ομάδα 0: 1. ευγενή αέρια | 1δ2 (Αυτός) ή εμάς2np6 (εάν n> 1) |
Ερώτηση 2
(UECE) Το χημικό στοιχείο με Z = 54 έχει στο στρώμα σθένους του τη διαμόρφωση 5s2 5ρ6. Τα στοιχεία με Z = 52 και με Z = 56 ανήκουν στις οικογένειες:
α) χαλκογόνα και αλκαλική γη
β) αλογόνα και αλκάλια
γ) αλογόνα και αλκαλική γη
δ) χαλκογόνα και αλκάλια
Σωστή εναλλακτική λύση: α) χαλκογόνα και αλκαλικές γαίες.
Δεδομένων των ατομικών αριθμών, πραγματοποιήσαμε την ηλεκτρονική διανομή και βρήκαμε τα ακόλουθα αποτελέσματα:
| 54X και | 52Εσείς | 56Μπα |
|
8 ηλεκτρόνια σε στρώμα σθένους |
6 ηλεκτρόνια σε στρώμα σθένους |
2 ηλεκτρόνια σε στρώμα σθένους |
| Noble Gases: 8Α οικογένεια | Χαλκογόνα: 6Α οικογένεια | Αλκαλική Γη: οικογένεια 2Α |
ερώτηση 3
(ΦΑ. Ibero-Americana-SP) Η ομάδα περιοδικών πινάκων που χαρακτηρίζεται από την υπεροχή των τεχνητών στοιχείων είναι η ακόλουθη:
α) λανθανίδες
β) ευγενή αέρια
γ) μέταλλα μετάβασης
δ) μέταλλα αλκαλικών γαιών
ε) ακτινίδες
Σωστή εναλλακτική λύση: ε) ακτινίδες.
Τεχνητά στοιχεία είναι εκείνα που δεν υπάρχουν στη φύση και έχουν συντεθεί στο εργαστήριο μέσω πυρηνικών αντιδράσεων.
Ονομάζονται επίσης transuranic στοιχεία, καθώς αυτά τα ραδιενεργά στοιχεία έχουν ατομικό αριθμό μεγαλύτερο από 92, που αντιστοιχεί στο ουράνιο.
Γενικά, αυτά τα στοιχεία είναι βραχύβια, διαρκούν έως κλάσματα του δευτερολέπτου.
Σύμφωνα με αυτές τις πληροφορίες πρέπει:
Τα στοιχεία που βρίσκονται στη φύση είναι: λανθανίδες, ευγενή αέρια, μέταλλα μετάβασης και μέταλλα αλκαλικών γαιών. Με την εξαίρεση του τεχνητίου και του προμηθίου, που είναι τεχνητά
Η υπεροχή των τεχνητών στοιχείων είναι τα ακτινίδια, ταξινομούνται ως εσωτερικά μεταβατικά μέταλλα και εισάγονται στον περιοδικό πίνακα κάτω από τα λανθανίδια. Από αυτήν τη σειρά, μόνο το ακτίνιο, το θόριο, το πρωτακίνιο και το ουράνιο είναι φυσικά.
ερώτηση 4
(ΗΠΑ Καθολική Εκκλησία του Σαλβαδόρ-BA) Το είδος X2- με 8 ηλεκτρόνια στο εξώτατο κέλυφος (κέλυφος σθένους) μπορεί να είναι από το στοιχείο Χ, το οποίο, στον Περιοδικό Πίνακα, ανήκει στην ομάδα:
α) 7Α
β) 6Α
γ) 2Α
δ) 1Α
ε) 8Α
Σωστή εναλλακτική λύση: β) 6Α.
Σύμφωνα με τον κανόνα οκτάδας, για ένα στοιχείο που αποκτά σταθερότητα, προϋποθέτει την ηλεκτρονική διαμόρφωση ενός ευγενούς αερίου, το οποίο έχει 8 ηλεκτρόνια στο κέλυφος σθένους.
Φόρτιση 2- στα είδη X2- δείχνει ότι το στοιχείο έχει αποκτήσει 2 ηλεκτρόνια.
Η ηλεκτρονική διαμόρφωση του είδους που έχει 8 ηλεκτρόνια στο εξώτατο κέλυφος είναι ns2np6.
Με την απώλεια δύο ηλεκτρονίων, το στοιχείο επιστρέφει στην κατάσταση γείωσης με διαμόρφωση ηλεκτρονίων ns2np4.
Τα 6 ηλεκτρόνια στο κέλυφος σθένους είναι χαρακτηριστικά των χαλκογόνων, στοιχεία της οικογένειας 6Α.
Για παράδειγμα:
| Στοιχείο: οξυγόνο | ηλεκτρονική διαμόρφωση |
| 8Ο | 1δ22δ22ρ4 |
| είδος O2- | 1δ22δ22ρ6 |
Μάθε περισσότερα για Περιοδικές οικογένειες πίνακα.
Χημικά στοιχεία
ερώτηση 1
(CESGRANRIO) Δεδομένων των στοιχείων των ατομικών αριθμών 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 και 75, η επιλογή που περιέχει μόνο αλκαλικά μέταλλα είναι:
α) 3, 11, 37 και 55
β) 3, 9, 37 και 55
γ) 9, 11, 38 και 55
δ) 12, 20, 38 και 56
ε) 12, 37, 47 και 75
Σωστή εναλλακτική λύση: α) 3, 11, 37 και 55
Τα αλκαλικά μέταλλα αντιστοιχούν στα χημικά στοιχεία που τερματίζουν την ηλεκτρονική διανομή με ένα ηλεκτρόνιο στο δευτερεύον επίπεδο.
Κάνοντας την ηλεκτρονική διανομή των δεδομένων ατομικών αριθμών, έχουμε τα ακόλουθα αλκαλικά μέταλλα:
| Ζ = 3 | Ζ = 11 | Ζ = 37 | Ζ = 55 |
| Λίθιο | Νάτριο | Ρουβίνιο | Καίσιο |
Οι άλλοι ατομικοί αριθμοί αντιστοιχούν σε στοιχεία των ακόλουθων ομάδων:
Μέταλλα αλκαλικών γαιών: τερματίστε την ηλεκτρονική διανομή στο sublevel s2.
| Ζ = 12 | Ζ = 38 | Ζ = 56 |
| Μαγνήσιο | Στρόντιο | Βάριο |
Μεταβατικά μέταλλα: τερματίστε την ηλεκτρονική διανομή στο υπο επίπεδο.
| Ζ = 30 | Ζ = 47 | Ζ = 75 |
| Ψευδάργυρος | Ασήμι | Ρήνιο |
Αλογόνα: τερματισμός της ηλεκτρονικής διανομής στο υπόγειο σελ5.
| Ζ = 9 |
Ερώτηση 2
(Unirio) «Η τεχνητή καρδιά που τοποθετήθηκε στο Eloi άρχισε να αναπτύσσεται πριν από τέσσερα χρόνια στις Ηνωμένες Πολιτείες και χρησιμοποιείται ήδη από περίπου 500 άτομα. Το σετ, που ονομάζεται Heartmate, αποτελείται από τρία κύρια κομμάτια. Το πιο σημαντικό είναι μια στρογγυλή τσάντα τεσσάρων κιλών, διαμέτρου 12 εκατοστών και πάχους 3 εκατοστών, κατασκευασμένη από τιτάνιο - ένα ασημί-λευκό μέταλλο, ελαφρύ και δυνατό. " Περιοδικό Veja, Ιούλιος 1999.
Μεταξύ των παρακάτω μετάλλων, αυτό που έχει, στο τελευταίο στρώμα, αριθμό ηλεκτρονίων ίσο με αυτό του τιτανίου είναι:
μετα Χριστον
β) Σε
γ) Γα
δ) Mg
ε) Xe
Σωστή εναλλακτική λύση: δ) Mg.
| Τιτάνιο | ηλεκτρονική διαμόρφωση | Κατανομή στρώματος |
| 22Εσείς | 1δ2 2δ2 2ρ6 3δ2 3ρ6 4δ2 3δ2 | 2, 8, 10, 2 |
Από την ηλεκτρονική διανομή τιτανίου, βλέπουμε ότι αυτό το στοιχείο έχει 2 ηλεκτρόνια στο τελευταίο κέλυφος.
| Στοιχείο | ηλεκτρονική διαμόρφωση | Κατανομή στρώματος |
| 6ΝΤΟ | 1δ2 2δ2 2ρ2 | 2, 4 |
| 11Στο | 1δ2 2δ2 2ρ6 3δ1 | 2, 8, 1 |
| 31Γα | 1δ2 2δ2 2ρ6 3δ2 3ρ6 4δ2 3δ104ρ1 | 2, 8, 18, 3 |
| 12mg | 1δ2 2δ2 2ρ6 3δ2 | 2, 8, 2 |
| 54X και | 1δ2 2δ2 2ρ6 3δ2 3ρ6 3δ10 4δ2 4ρ6 4δ10 5 δευτ2 5ρ6 | 2, 8, 18, 18, 8 |
Το στοιχείο που έχει επίσης 2 ηλεκτρόνια στο τελευταίο κέλυφος είναι μαγνήσιο.
ερώτηση 3
(UFPA) Σκεφτείτε ένα συγκεκριμένο χημικό στοιχείο του οποίου το πιο ενεργητικό υπόστρωμα είναι 5s2. Ο ατομικός του αριθμός και η ομάδα στην οποία βρίσκεται στον Περιοδικό Πίνακα είναι, αντίστοιχα:
α) 20 · 1Α
β) 20; 2Α
γ) 38; 2Α
δ) 38; 1Α
ε) 39; 2Α
Σωστή εναλλακτική λύση: γ) 38; 2Α
Κάνοντας την ηλεκτρονική διανομή, διαπιστώσαμε ότι:
- Το χημικό στοιχείο βρίσκεται στην οικογένεια 2Α, καθώς έχει το πιο ενεργητικό sublevel του s2
- Έχει ατομικό αριθμό 38, που αντιστοιχεί στον συνολικό αριθμό ηλεκτρονίων που διανέμονται.
- Βρίσκεται στην πέμπτη περίοδο, καθώς η ηλεκτρονική διανομή πραγματοποιήθηκε μέχρι το πέμπτο επίπεδο.
Ελέγχοντας αυτές τις πληροφορίες στον Περιοδικό Πίνακα, μπορούμε να επιβεβαιώσουμε ότι είναι το στοιχείο στρόντιο.
ερώτηση 4
(UFC) Ένα άτομο x έχει ένα περισσότερο πρωτόνιο από ένα άτομο y. Με βάση αυτές τις πληροφορίες, καθορίστε τη σωστή δήλωση.
a) Εάν το y είναι αλκαλική γη, το x είναι αλκαλικό μέταλλο.
β) Εάν το y είναι ευγενές αέριο, το x είναι αλογόνο.
c) Εάν το y είναι μέταλλο μετάβασης, το x είναι ένα ευγενές αέριο.
δ) Εάν το y είναι ένα ευγενές αέριο, το x είναι ένα μέταλλο αλκαλίου.
ε) το x βρίσκεται στην ίδια περίοδο πριν από το άτομο y στον περιοδικό πίνακα.
Σωστή εναλλακτική λύση: δ) Εάν το y είναι ευγενές αέριο, το x είναι αλκαλικό μέταλλο.
Ο περιοδικός πίνακας διατάσσεται με αύξουσα σειρά ατομικού αριθμού.
Εάν το Υ έχει ατομικό αριθμό z και το Χ έχει ένα περισσότερο πρωτόνιο από αυτό, αυτό σημαίνει ότι αυτά τα δύο στοιχεία βρίσκονται στην ίδια περίοδο και το Χ ακολουθεί το Υ.
Παράδειγμα:
| Στοιχείο | επόμενο στοιχείο |
| ζΓ | z + 1Χ |
| 11Στο | 12mg |
Τα δύο στοιχεία βρίσκονται στην 3η περίοδο και το μαγνήσιο έχει ένα ακόμη πρωτόνιο από το νάτριο.
Σύμφωνα με αυτόν τον συλλογισμό πρέπει:
Α) ΛΑΘΟΣ. Ένα αλκαλικό μέταλλο έρχεται πριν από ένα μέταλλο αλκαλικής γαίας στον περιοδικό πίνακα. Η σωστή δήλωση θα ήταν: Εάν το y είναι αλκαλικό μέταλλο, το x είναι αλκαλική γη.
β) ΛΑΘΟΣ. Ένα αλογόνο έρχεται πριν από το ευγενές αέριο στον περιοδικό πίνακα. Η σωστή δήλωση θα ήταν: Εάν το y είναι αλογόνο, το x είναι ευγενές αέριο.
γ) ΛΑΘΟΣ. Τα μεταβατικά μέταλλα και τα ευγενή αέρια διαχωρίζονται από άλλα χημικά στοιχεία και επομένως δεν είναι διαδοχικά.
δ) ΣΩΣΤΗ. Τα ευγενή αέρια είναι η τελευταία ομάδα στον περιοδικό πίνακα και τα πρώτα αλκαλικά μέταλλα, επομένως είναι διαδοχικά.
Παράδειγμα:
| ευγενες αεριο | αλκαλι μέταλλο |
| ζΓ | z + 1Χ |
| 2αυτός | 3ανάγνωση |
Το λίθιο, ένα αλκαλικό μέταλλο, έχει ένα περισσότερο πρωτόνιο από το ήλιο, το οποίο είναι ένα ευγενές αέριο.
ε) ΛΑΘΟΣ. Το Χ είναι στην ίδια περίοδο με το Υ αλλά μετά από αυτό, όχι νωρίτερα με τις εναλλακτικές καταστάσεις.
ερώτηση 5
Από τον ατομικό αριθμό ενός χημικού στοιχείου είναι δυνατόν να γνωρίζουμε:
α) τον αριθμό των νετρονίων στον πυρήνα
β) τον αριθμό ηλεκτρονίων στην ηλεκτροσφαίρα
γ) τη βασική μάζα
Απάντηση: β) ο αριθμός ηλεκτρονίων στην ηλεκτροσφαίρα
Ένα άτομο στην κατάσταση του εδάφους είναι ηλεκτρικά ουδέτερο. Γνωρίζοντας λοιπόν τον ατομικό αριθμό, ο οποίος αντιστοιχεί στον αριθμό των πρωτονίων (θετικά φορτισμένα σωματίδια), γνωρίζουμε τον αριθμό των ηλεκτρονίων (αρνητικά φορτισμένα σωματίδια) στην ηλεκτρόσφαιρα.
Για παράδειγμα, ο σίδηρος έχει ατομικό αριθμό 26, έτσι στην κατάσταση του εδάφους έχει 26 ηλεκτρόνια γύρω από τον πυρήνα.
Μάθε περισσότερα για χημικά στοιχεία είναι το ατομικός αριθμός.
Περιοδικές και περιοδικές ιδιότητες
ερώτηση 1
(UFSM) Να κρίνει εάν οι δηλώσεις που σχετίζονται με τις περιοδικές ιδιότητες των στοιχείων είναι αληθείς (Τ) ή ψευδείς (F).
Εξαρτάται από τις ατομικές μάζες των στοιχείων.
() Επαναλαμβάνονται σε λίγο ή πολύ τακτικά διαστήματα σε σχέση με την αύξηση των ατομικών αριθμών.
() Είναι παρόμοια στην ίδια ομάδα στοιχείων.
() Είναι παρόμοια στην ίδια περίοδο των στοιχείων.
() Στην ίδια ομάδα, οι αριθμητικές τιμές των περιοδικών ιδιοτήτων αυξάνονται πάντα όταν υπάρχει αύξηση του ατομικού αριθμού στοιχείων.
Η σωστή ακολουθία είναι:
α) V - F - V - F - F
β) V - F - F - V - V
γ) F - V - V - F - F
δ) F - V - F - V - V
ε) V - F - F - V - F
Σωστή εναλλακτική λύση: c) F - V - V - F - F
(ΨΕΥΔΗΣΕξαρτηθείτε από τις ατομικές μάζες των στοιχείων.
Σύμφωνα με τον νόμο περιοδικότητας του Moseley, πολλές φυσικές και χημικές ιδιότητες των χημικών στοιχείων ποικίλλουν ανά ατομικό αριθμό.
(ΑΛΗΘΗΣΕπαναλαμβάνονται σε λίγο ή πολύ τακτικά διαστήματα σε σχέση με την αύξηση των ατομικών αριθμών.
Ιδιότητες όπως η ατομική ακτίνα, ο ατομικός όγκος, η πυκνότητα, το σημείο τήξης και το σημείο βρασμού είναι παραδείγματα ιδιοτήτων που επαναλαμβάνονται τακτικά στον περιοδικό πίνακα.
(ΑΛΗΘΗΣ) Είναι παρόμοια στην ίδια ομάδα στοιχείων.
Οι ομάδες περιοδικών πινάκων έχουν διευθετηθεί με στοιχεία που έχουν παρόμοιες ιδιότητες.
(ΨΕΥΔΗΣ) Είναι παρόμοια στην ίδια περίοδο των στοιχείων.
Οι ιδιότητες είναι παρόμοιες σε οικογένειες και όχι σε περιόδους. Σε περιόδους, τα στοιχεία κατανέμονται με τον αριθμό των ηλεκτρονικών επιπέδων.
(ΨΕΥΔΗΣΣτην ίδια ομάδα, οι αριθμητικές τιμές των περιοδικών ιδιοτήτων αυξάνονται πάντα όταν υπάρχει αύξηση στον ατομικό αριθμό στοιχείων.
Οι ιδιότητες μπορούν να αυξηθούν ή να μειωθούν ανάλογα με τον ατομικό αριθμό. Ένα παράδειγμα αυτού είναι η ηλεκτροπαραγωγικότητα, η οποία μειώνεται καθώς ο ατομικός αριθμός αυξάνεται σε μια δεδομένη ομάδα.
Διαβάστε επίσης: Περιοδικές Ιδιότητες
Ερώτηση 2
(FAESP) Οι περιοδικές ιδιότητες των στοιχείων είναι:
α) πυκνότητα, ατομικός όγκος και ατομική μάζα.
β) σημείο τήξεως, ηλεκτροαναρτητικότητα και ειδική θερμότητα.
γ) ατομικός όγκος, ατομική μάζα και σημείο τήξης.
δ) ατομική μάζα, ειδική θερμότητα και σημείο τήξης.
ε) ατομική μάζα και ειδική θερμότητα.
Σωστή εναλλακτική λύση: ε) ατομική μάζα και ειδική θερμότητα.
Οι απεριδικές ιδιότητες επαναλαμβάνονται σε τακτά χρονικά διαστήματα.
Η ατομική μάζα είναι το μέτρο του βάρους του ατόμου σε μονάδες ατομικής μάζας, το οποίο αντιστοιχεί σε της μάζας άνθρακα-12.
Η ειδική θερμότητα καθορίζει την ποσότητα θερμότητας που απαιτείται για την αύξηση της θερμοκρασίας κατά 1 ° C από 1 g του στοιχείου.
Αυτές οι δύο ιδιότητες δεν σχετίζονται με τη θέση του στοιχείου στον περιοδικό πίνακα.
Οι άλλες ιδιότητες ταξινομούνται ως περιοδικές καθώς αυξάνονται ή μειώνονται με τον ατομικό αριθμό. Είναι αυτοί:
- Πυκνότητα: αντιπροσωπεύει το πηλίκο μεταξύ της μάζας και του όγκου ενός στοιχείου.
- Ατομικός όγκος: αντιπροσωπεύει τον όγκο ενός συνόλου ατόμων και επηρεάζει την απόσταση μεταξύ τους.
- Σημείο τήξεως: θερμοκρασία στην οποία πραγματοποιείται η μετάβαση από στερεό σε υγρό.
- Ηλεκτροναραγωγικότητα: η ικανότητα του ατόμου να προσελκύσει στον εαυτό του το ηλεκτρονικό ζεύγος που μοιράζεται σε έναν ομοιοπολικό δεσμό.
Διαβάστε επίσης: ηλεκτροαρνητικότητα και Ηλεκτρονική συγγένεια
ερώτηση 3
(PUC-PR) Μεταξύ των παρακάτω διαγραμμάτων που σχετίζονται με τον περιοδικό πίνακα, ποια είναι σωστά;
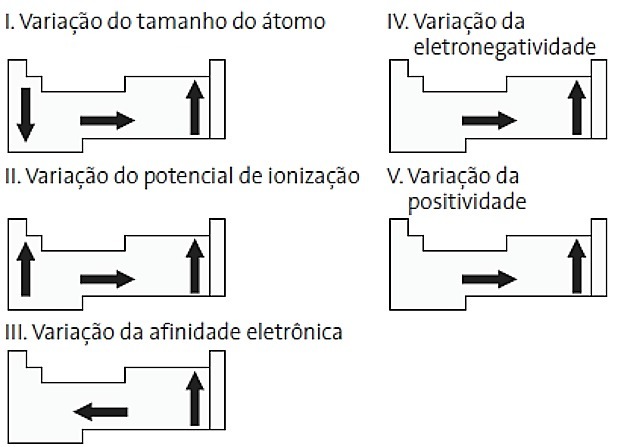
α) II και V
β) II και III
γ) I και V
δ) II και IV
ε) III και IV
Σωστή εναλλακτική λύση: δ) II και IV.
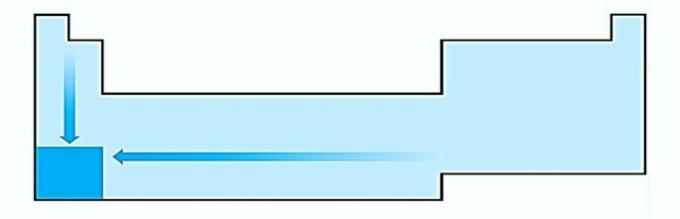
ΕΓΩ. ΛΑΝΘΑΣΜΕΝΟΣ. Η διακύμανση του μεγέθους του ατόμου μετράται από τη μέση απόσταση από τον πυρήνα προς το εξόχως ηλεκτρονικό. Τα μεγαλύτερα άτομα βρίσκονται στο κάτω μέρος του πίνακα, οπότε η αύξηση συμβαίνει σύμφωνα με τον ατομικό αριθμό και η σωστή αναπαράσταση είναι:
ΙΙ. ΣΩΣΤΟΣ Η ενέργεια που απαιτείται για την απόσπαση ενός ηλεκτρονίου από ένα απομονωμένο άτομο στην αέρια κατάσταση ονομάζεται δυναμικό ιονισμού. Αυξάνεται όπως φαίνεται στο διάγραμμα δήλωσης.
III. ΛΑΝΘΑΣΜΕΝΟΣ. Η ηλεκτρονική συγγένεια εκφράζει την ενέργεια που απελευθερώνεται όταν ένα ουδέτερο άτομο στην αέρια κατάσταση δέχεται ένα ηλεκτρόνιο, το οποίο είναι μια πολύ σημαντική ιδιότητα των μη μετάλλων. Οι υψηλότερες ηλεκτρονικές συγγένειες παρατηρούνται σε αλογόνα και οξυγόνο.
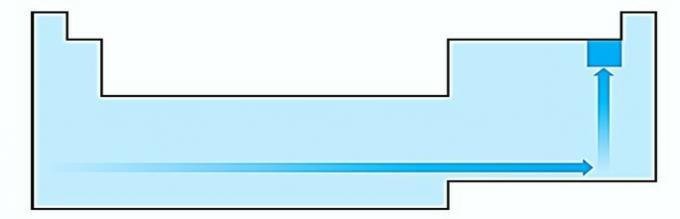
IV. ΣΩΣΤΟΣ Η ηλεκτροπαραγωγικότητα σχετίζεται με το δυναμικό ιονισμού και τη συγγένεια ηλεκτρονίων. Ως τέτοια, τα αλογόνα είναι τα πιο ηλεκτροαρνητικά στοιχεία στον περιοδικό πίνακα.
V. ΛΑΝΘΑΣΜΕΝΟΣ. Η ηλεκτροθετικότητα δημιουργείται στην αντίθετη κατεύθυνση με την ηλεκτροαρνητικότητα. Αντιπροσωπεύει την ικανότητα του ατόμου να εγκαταλείψει τα ηλεκτρόνια.
Επομένως, τα αλκαλικά μέταλλα έχουν την υψηλότερη ηλεκτροθετικότητα.
Συνεχίστε να δοκιμάζετε τις γνώσεις σας με τις λίστες:
- Ασκήσεις σε χημικούς δεσμούς
- Ασκήσεις ηλεκτρονικής διανομής
- Ασκήσεις σε ατομικά μοντέλα
- Ασκήσεις θερμοχημείας