Τα κύτταρα ή οι μπαταρίες που έχουν το λίθιο ως κύριο συστατικό τους έχουν ως ένα από τα χαρακτηριστικά τους το γεγονός ότι είναι πολύ ελαφριά, καθώς το λίθιο είναι το λιγότερο πυκνό μέταλλο που έχει ανακαλυφθεί μέχρι τώρα. Για να σας δώσω μια ιδέα, αυτό το ασημί λευκό μέταλλο επιπλέει στο νερό, καθώς είναι διπλάσιο πυκνό. Αυτό οφείλεται στο γεγονός ότι το λίθιο έχει μόνο τρία πρωτόνια και τρία νετρόνια.
Υπάρχουν δύο κύριοι τύποι μπαταριών λιθίου, ένας από τους οποίους ονομάζεται μπαταρία λιθίου ιωδίου. Αναπτύχθηκε κυρίως για χρήση σε καρδιακοί βηματοδότες, δεδομένου ότι είναι πολύ ελαφρύ, ασφαλές (δεν απελευθερώνει αέρια, καθώς είναι ερμητικά κλειστό), έχει ένα καλό ανθεκτικότητα (περίπου 8 έως 10 έτη), παρέχει τάση 2,8 V και υψηλή πυκνότητα φόρτισης (0,8 Wh / cm3).
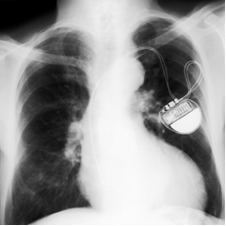
Τα ηλεκτρόδια σχηματίζονται από λίθιο και σύμπλοκο ιωδίου, τα οποία διαχωρίζονται από ένα κρυσταλλικό στρώμα ιωδιούχου λιθίου που επιτρέπει τη διέλευση του ηλεκτρικού ρεύματος. Ο μεταλλικό λίθιο λειτουργεί σαν το άνοδος αυτού του κυττάρου, δηλαδή, ο αρνητικός πόλος που οξειδώνεται, χάνοντας ηλεκτρόνια. ήδη το
κάθοδος, ο θετικός πόλος που μειώνει, λαμβάνει ηλεκτρόνια, είναι το σύμπλεγμα ιωδίου.Δείτε τις ημι-αντιδράσεις που εμφανίζονται στα ηλεκτρόδια και την εξίσωση που αντιπροσωπεύει την παγκόσμια αντίδραση αυτού του τύπου κυττάρου:
Μισή αντίδραση ανόδου: 2 Li(μικρό) → 2 Διάβασα+(μικρό) + 2ε-
Ημι-αντίδραση καθόδου: 1 I2 (α) + 2ε-→ 2 Ι-(μικρό)
Παγκόσμια αντίδραση: 2 Li(μικρό) + 1 εγώ2 (α) → 2 LiI(μικρό)
Οι μπαταρίες λιθίου-ιωδίου έχουν πολύ μικρά νομίσματα, όπως φαίνεται στο παρακάτω σχήμα:

Ο άλλος τύπος κυψέλης ή μπαταρίας είναι το ιόν λιθίου. Παίρνει αυτό το όνομα ακριβώς επειδή η λειτουργία του βασίζεται στην κίνηση των ιόντων λιθίου (Li+). Αυτή τη στιγμή χρησιμοποιείται ευρέως στο μπαταρίες κινητού τηλεφώνου και το δυναμικό του κυμαίνεται μεταξύ 3,0 και 3,5 V.

Η άνοδος και η κάθοδος σχηματίζονται από άτομα διατεταγμένα σε επίπεδα όπως φύλλα με χώρους όπου εισάγονται ιόντα λιθίου. Ο άνοδος σχηματίζεται από γραφίτη με μέταλλο χαλκού και τα ιόντα παρεμβάλλονται στα επίπεδα των εξαγωνικών δομών άνθρακα, σχηματίζοντας την ακόλουθη ουσία: ανάγνωσηεΝΤΟ6ήδη το κάθοδος σχηματίζεται από ιόντα λιθίου που παρεμβάλλονται σε οξείδιο με ελασματοειδή δομήανάγνωσηΧΕρωτολογώ2).
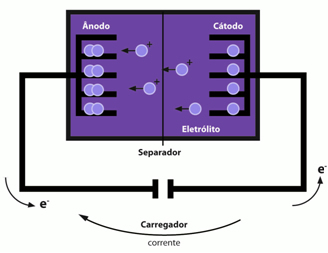
Έτσι, έχουμε ότι τα ιόντα λιθίου αφήνουν την άνοδο και μεταναστεύουν μέσω ενός μη υδατικού διαλύτη στην κάθοδο.
Μισή αντίδραση ανόδου: LiεΝΤΟ6 (α) → y Λι + ΝΤΟ6+ε-
Ημι-αντίδραση καθόδου: LiΧΕρωτολογώ2 (α) + ε ανάγνωση+(μικρό) + ε και- → Διάβασαx + εΕρωτολογώ2 (α)
Παγκόσμια αντίδραση: ΛιεΝΤΟ6 (α) + διαβάστεΧΕρωτολογώ2 → ΝΤΟ6(μικρό) +ανάγνωσηx + εΕρωτολογώ2 (α)
Αυτές οι μπαταρίες είναι επαναφορτιζόμενες, απλά χρησιμοποιώντας ένα εξωτερικό ηλεκτρικό ρεύμα που προκαλεί τη μετανάστευση ιόντων λιθίου στην αντίθετη κατεύθυνση, δηλαδή, από το οξείδιο στον γραφίτη.

Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/pilhas-baterias-litio.htm