Πολυμερισμός είναι το όνομα της χημικής διαδικασίας που οδηγεί στο σχηματισμό μακρομορίων (μεγάλα μόρια) που ονομάζονται πολυμερή, μέσω του συνδυασμού μικρότερων μορίων, των μονομερών.
η αντίδραση του πολυμερισμός Είναι πολύ συνηθισμένο στη φύση, όπως μπορούμε να δούμε στους υδατάνθρακες (όπως το άμυλο) και τις πρωτεΐνες (όπως η καζεΐνη στο γάλα). Εμφανίζεται επίσης συνθετικά, καθώς η συντριπτική πλειονότητα των πολυμερών που χρησιμοποιούνται από τα ανθρώπινα όντα στην καθημερινή τους ζωή κατασκευάζονται τεχνητά.
Το πρώτο πολυμερές παράγεται από πολυμερισμός συνθετικός ήταν ο Μπακελίτης, το 1909, από τον Βέλγο χημικό Leo Hendrik Baekeland.
Γενικά, για ένα μονομερές να συνδυάζεται με ένα άλλο (είτε είναι το ίδιο είτε διαφορετικό) σε μια αντίδραση του πολυμερισμός, είναι απαραίτητο να υπάρχει ελεύθερος σθένος (χημικός δεσμός) και στα δύο μονομερή.
Αυτές οι σθένες προκύπτουν ως αποτέλεσμα της διάσπασης των δεσμών, μέσω της χρήσης καταλυτών (όπως το νικέλιο), εξωτερικές συνθήκες όπως φως και θερμότητα ή από το φαινόμενο συντονισμού στη δομή (μετατόπιση ηλεκτρονίων).
Στο σχηματισμό πολυπροπυλενίου (πολυμερές PP), για παράδειγμα, που χρησιμοποιείται σε οικιακά σκεύη και παιχνίδια, το pi σύνδεσμος (π) σε κάθε μόριο αναλύεται ως εξής:
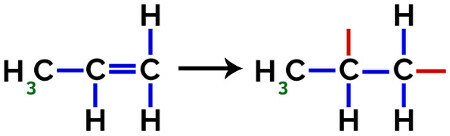
Θραύση του δεσμού pi σε προπυλένιο
Έτσι, κάθε μονομερές προπυλενίου μπορεί να συνδέεται με δύο άλλα μονομερή προπυλενίου και να σχηματίζει το πολυμερές ΡΡ ή πολυπροπυλένιο (το πρόθεμα πολυ υποδεικνύει πολλές μονομερείς μονάδες). Ο πιο συχνός τρόπος αναπαραγωγής ενός πολυμερούς έχει το μονομερές μεταξύ παρενθέσεων και, στο εξωτερικό, το γράμμα n, το οποίο δείχνει πολλά μονομερή, όπως μπορούμε να δούμε στην περίπτωση του πολυμερούς PP:
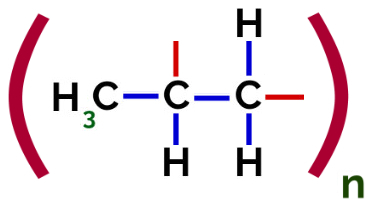
Αναπαράσταση πολυμερούς PP
η αντίδραση του πολυμερισμός μπορεί να γίνει με διαφορετικούς τρόπους, όπως θα δούμε παρακάτω:
α) Αντίδραση του πολυμερισμός προσθήκης
Σε αυτό πολυμερισμός, υπάρχει πάντα ένα σπάσιμο ενός δεσμού pi στο μονομερές, το οποίο προκαλεί δύο ελεύθερους σθένους να εμφανίζονται στη δομή, όπως στον σχηματισμό του πολυαιθυλενο, πολυμερές που χρησιμοποιείται ευρέως στη φαρμακευτική συσκευασία.
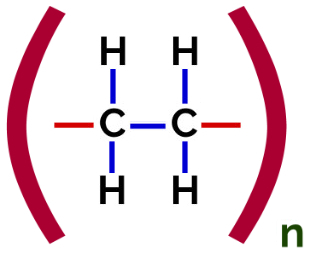
Δομικός τύπος πολυμερούς προσθήκης πολυαιθυλενίου
Στο πολυμερισμός πολυαιθυλενίου, μόρια αιθυλενίου (αιθένιο) χρησιμοποιούνται ως το μονομερές, το οποίο έχει δεσμό pi μεταξύ των δύο ατόμων άνθρακα. Όταν αυτός ο δεσμός σπάσει, εμφανίζονται δύο ελεύθερα σθένη, ένα σε κάθε άτομο άνθρακα που συμμετείχε στον δεσμό π. Τα μονομερή ενώνονται ακριβώς σε καθένα από αυτά τα σθένη, δηλαδή, το σθένος του ενός συνδέεται με το σθένος του άλλου, και ούτω καθεξής.
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
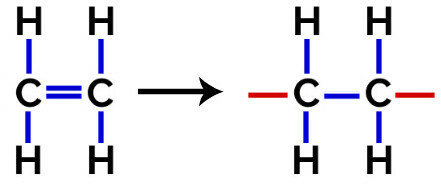
Εξίσωση σχηματισμού πολυαιθυλενίου
β) Αντίδραση πολυμερισμού προσθήκης 1.4
Σε αυτόν τον πολυμερισμό, τα μονομερή παρουσιάζουν δύο εναλλασσόμενους διπλούς δεσμούς (ένα pi και ένα σίγμα), που ευνοούν το φαινόμενο συντονισμού (εναλλασσόμενη θέση των ηλεκτρονίων pi του δεσμού pi), όπως στον σχηματισμό συνθετικού καουτσούκ (πολυβουταδιένιο)

Δομικός τύπος πολυβουταδιενίου
Η μονομερής μονάδα αυτού του πολυμερούς είναι το βουταδιένιο, το οποίο έχει δύο εναλλασσόμενους διπλούς δεσμούς. Με συντονισμό, η δομή έχει διπλό δεσμό μεταξύ των ανθράκων 2 και 3, και δύο ελεύθερων σθένους στους άνθρακες 1 και 4. Ακριβώς σε αυτά τα ελεύθερα σθένη άνθρακα 1 και 4 συνδυάζονται τα μονομερή.

Συντονισμός στο βουταδιένιο
γ) Αντίδραση του πολυμερισμός συμπύκνωσης ή εξάλειψη
Είναι μια αντίδραση του πολυμερισμός στο οποίο, υποχρεωτικά, δύο μονομερή (το ίδιο ή διαφορετικό) χάνουν ταυτόχρονα άτομα ή ομάδες, με αποτέλεσμα δύο ελεύθερα σθένη σε καθένα από αυτά. Με αυτόν τον τρόπο, υπάρχει πάντα η απομάκρυνση του υδρογόνου από ένα μονομερές, το οποίο στη συνέχεια ενώνει ένα αλογόνο (F, Cl, Br, I), OH, NH2ή στο CN του άλλου μονομερούς.
Έτσι, στο πολυμερισμός με αποβολή, υπάρχει πάντα ο σχηματισμός νερού, αλογονωμένου οξέος (HCl, HI, HF, HBr), αμμωνίας (NH3) ή υδροκυανικό οξύ (HCN) επιπλέον του πολυμερούς. Δείτε, για παράδειγμα, την αναπαράσταση του σχηματισμού πολυεστέρα, ενός υλικού που χρησιμοποιείται ως ύφασμα:

Εξίσωση σχηματισμού πολυεστέρα
Τα μονομερή που σχηματίζουν πολυεστέρες είναι ρ-βενζενδιοϊκό οξύ και αιθάνιο-1,2-διόλη. Μπορούμε να το παρατηρήσουμε σε αυτό πολυμερισμός η απομάκρυνση των μορίων του νερού συμβαίνει, αφού τα δύο μονομερή έχουν δύο υδροξύλια. Σε αυτήν τη διαδικασία, το οξύ χάνει τα δύο υδροξύλια και η διαλκοόλη χάνει μόνο το υδρογόνο από τα υδροξύλια του:

Δομή πολυεστέρα
Τα μονομερή πολυεστέρα ενώνονται με το οξυγόνο στην αλκοόλη και τον άνθρακα στο καρβοξυλικό οξύ.
Από μένα. Diogo Lopes Dias