Ισορροπίαθερμικός είναι η κατάσταση στην οποία ένα σώμα βρίσκεται στο ίδιοθερμοκρασία από το περιβάλλον τους. Παρατηρείται ότι όλα τα σώματα που βρίσκονται σε υψηλότερες θερμοκρασίες από ό, τι οι γείτονές τους τείνουν να τους θερμαίνουν αυθόρμητα έως ότου και οι δύο αρχίσουν να παρουσιάζουν την ίδια θερμοκρασία.
Κοίταεπίσης:Βασικές αρχές θερμολογίας
Θερμική ισορροπία και ο μηδενικός νόμος της Θερμοδυναμικής
Η θερμική ισορροπία είναι η κεντρική ιδέα πίσω από τον μηδενικό νόμο της θερμοδυναμικής. Ένας τέτοιος νόμος ορίζει ότι, στην περίπτωση που δύο θερμοδυναμικά συστήματα, Ο και σι, βρίσκονται σε θερμική ισορροπία με ένα τρίτο θερμοδυναμικό σύστημα, ΝΤΟ, έπειτα, Ο και σι θα είναι επίσης σε θερμική ισορροπία.
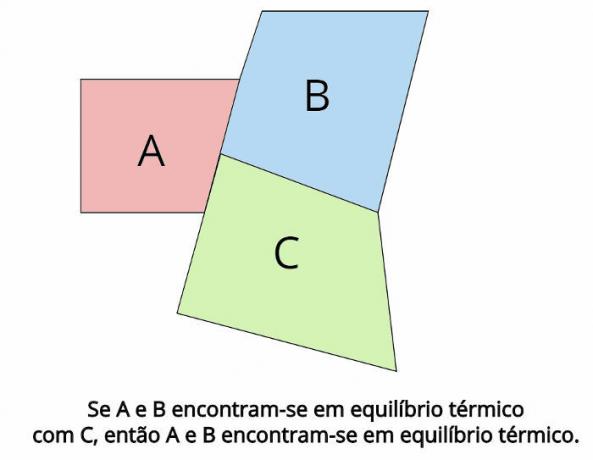
Στη θερμική ισορροπία, οι τελικές θερμοκρασίες κάθε σώματος πρέπει να είναι ίσες: TΟ = Τσι = ΤΝΤΟ
Δείτε τι θεσπίζει η δήλωση του μηδενικού νόμου της θερμοδυναμικής:
“Εάν δύο σώματα βρίσκονται σε θερμική ισορροπία με ένα τρίτο σώμα, τότε αυτά τα σώματα θα βρίσκονται σε θερμική ισορροπία μεταξύ τους. "
Ένας άλλος τρόπος κατανόησης της θερμικής ισορροπίας βασίζεται στην εσωτερική ενέργεια των σωμάτων. Η εσωτερική ενέργεια, ή απλά η θερμική ενέργεια, είναι μια φυσική ποσότητα κατευθείαναναλογικά à θερμοκρασία του σώματος. Επομένως, εάν υπάρχουν σώματα με διαφορετικές θερμοκρασίες μέσα στο ίδιο θερμοδυναμικό σύστημα, θα έχουν διαφορετικές μονάδες εσωτερική ενέργεια και επομένως θα μεταφέρει μέρος αυτής της ενέργειας μεταξύ τους έως ότου δεν υπάρχει διαφορά μεταξύ των ενεργειών τους. εσωτερικός. Θέλετε να μάθετε περισσότερα για το ποια είναι η εσωτερική ενέργεια και ποιες είναι οι ιδιότητές της; Πρόσβαση στο άρθρο: Εσωτερική ενέργεια.
θερμική και θερμική ισορροπία
Η μεταφορά θερμότητας συμβαίνει πάντα αυθόρμητα, από το σώμα με την υψηλότερη θερμοκρασία στο σώμα με τη χαμηλότερη θερμοκρασία. Αυτή η μεταφορά ενέργειας με τη μορφή θερμότητας μπορεί να πραγματοποιηθεί μέσω διεργασιών όπως οδήγηση, μεταγωγή και ακτινοβολία.
Οδήγηση: Είναι η μεταφορά θερμότητας μεταξύ των σωμάτων που συμβαίνει ειδικά στα στερεά. Σε αυτόν τον τύπο αγωγής, δεν πραγματοποιούνται μαζικές μεταφορές. Αυτός ο τύπος μεταφοράς θερμότητας εξηγεί πώς συμβαίνει η θερμική ισορροπία στα μέταλλα, για παράδειγμα.
Μεταγωγή: Είναι μια μεταφορά θερμότητας που λαμβάνει χώρα σε υγρά. Σε αυτόν τον τρόπο μεταφοράς θερμότητας, υπάρχει μεταφορά μάζας, καθώς το θερμαινόμενο ρευστό κινείται, σχηματίζοντας ρεύματα μεταφοράς έως ότου όλο το ρευστό φτάσει στη θερμική ισορροπία.
Ακτινοβολία: Είναι η μετάδοση θερμότητας μέσω ηλεκτρομαγνητικών κυμάτων, οπότε αυτή η διαδικασία συμβαίνει ακόμη και αν δεν υπάρχει φυσικό μέσο μεταξύ του σώματος και ενός άλλου σώματος σε διαφορετικές θερμοκρασίες. Η θερμότητα που μεταφέρεται, στην περίπτωση αυτή, είναι το ισοδύναμο των ηλεκτρομαγνητικών κυμάτων με λιγότερη ενέργεια από ορατό φως, ως εκ τούτου θερμική ακτινοβολία, που βρίσκεται στην περιοχή του υπέρυθρο.
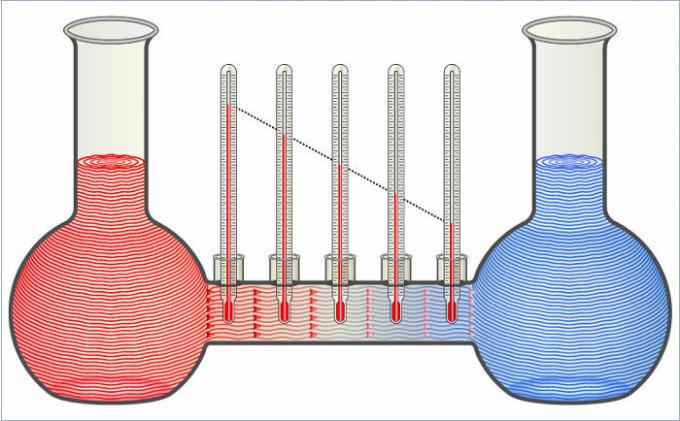
Τα δύο υγρά στο σχήμα μεταφέρουν θερμότητα μεταξύ τους έως ότου οι θερμοκρασίες τους είναι ίσες.
Θέλετε να μάθετε περισσότερα για το πώς πραγματοποιείται κάθε διαδικασία μεταφοράς θερμότητας; Πρόσβαση στο άρθρο: Διαδικασίες διάδοσης θερμότητας.
λογική θερμότητα
όταν υπάρχει διαφοράσεθερμοκρασία μεταξύ δύο σωμάτων, ή μεταξύ ενός σώματος και του περιβάλλοντός του, θα υπάρξει ανταλλαγή θερμότητας μεταξύ τους αυθόρμητα, έτσι ώστε το σώμα υψηλότερης θερμοκρασίας κρυώνει και τα σώματα χαμηλότερης θερμοκρασίας θερμαίνονται μέχρι να φτάσουν όλοι στη θερμοκρασία σε ισορροπίαθερμικός.
Η ποσότητα θερμότητας που ανταλλάσσεται μεταξύ σωμάτων σε διαφορετικές θερμοκρασίες καλείται λογική θερμότητα και αυτό το ποσό μπορεί να υπολογιστεί από τον τύπο που φαίνεται στο παρακάτω σχήμα:
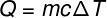
Ερ - θερμότητα (ασβέστης ή J)
Μ - μάζα (g ή kg)
ντο - ειδική θερμότητα (cal / gºC ή J / kg. Κ)
ΔΤ - διακύμανση θερμοκρασίας (° C ή K)
Στον τύπο που φαίνεται παραπάνω, είναι σημαντικό να επισημάνετε το μεγαλείο του ονόματος ειδική θερμότητα. τέτοιο μέγεθος μετρά το ποσότητα ενέργειας ανά μάζα που μια ουσία πρέπει να αποδώσει ή να απορροφήσει, ώστε η θερμοκρασία της να κυμαίνεται κατά 1 ° C. Στην περίπτωση καθαρού νερού, για παράδειγμα, και υπό κανονικές συνθήκες πίεσης, για να μεταβάλλεται η θερμοκρασία του κατά 1ºC, απαιτείται 1,0 θερμίδες για κάθε γραμμάριο νερού.
Έτσι, όλες οι ουσίες που έχουν καθιερώσει θερμική επαφή μεταξύ τους τείνουν να φθάσουν στην κατάσταση ισορροπίαθερμικός με την πάροδο του χρόνου αυθόρμητα, ωστόσο, ορισμένοι απαιτούν μεγαλύτερη ποσότητα ενέργειας για να το πράξουν και αυτό επηρεάζει άμεσα τη θερμοκρασία για να φθάσει στη θερμική ισορροπία.
ανάγνωσηεπίσης:Τι είναι η θερμοκρασία;
λανθάνουσα θερμότητα
Είναι πιθανό ότι κατά τη διάρκεια της ανταλλαγής θερμότητας με το περιβάλλον του, ένα σώμα παρουσιάζει πίεση, θερμοκρασία και όγκο που το προκαλούν να υποστεί μια αλλαγή στη φυσική του κατάσταση. Αυτές οι αλλαγές συμβαίνουν στο θερμοκρασίασυνεχής (για σώματα που αποτελούνται από μία μόνο ουσία, χωρίς ακαθαρσίες), δηλαδή, παρά τη λήψη ή τη θερμότητα στο εξωτερικό περιβάλλον, η θερμοκρασία αυτών των σωμάτων δεν αλλάζει.
Αυτό είναι δυνατό μόνο επειδή όλη η ενέργεια που ανταλλάσσεται, στην περίπτωση αυτή, χρησιμοποιείται για να αλλάξει τη διαμόρφωση των μορίων σας. Από τη στιγμή που το ενεργειακό φράγμα "ξεπεραστεί" και όλο το περιεχόμενο του σώματος βρίσκεται σε άλλη φυσική κατάσταση, το Το σώμα συνεχίζει να ανταλλάσσει θερμότητα με το περιβάλλον του, εκτός εάν, φυσικά, η θερμοκρασία του είναι ίση με την εξωτερική θερμοκρασία.
Ο λανθάνουσα θερμότητα μπορεί να υπολογιστεί από τον τύπο που φαίνεται στο παρακάτω σχήμα, ελέγξτε το:
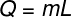
Ερ - λανθάνουσα θερμότητα (ασβέστης ή J)
Μ - μάζα (g ή kg)
μεγάλο - ειδική λανθάνουσα θερμότητα (cal / g ή J / kg)
Τύπος θερμικής ισορροπίας
Σε περίπτωση που θέλουμε να μάθουμε τι είναι θερμοκρασίασεισορροπία κάποιου θερμοδυναμικού συστήματος, είναι απαραίτητο να θεωρήσουμε το εν λόγω σύστημα ως α Σύστημααπομονωμένος, δηλαδή, πρέπει να υποθέσουμε ότι δεν ανταλλάσσεται θερμότητα με τις γειτονιές αυτού του συστήματος.
Από αυτήν την κατάσταση, μπορούμε να πούμε ότι το σύνολο της θερμότητας που ανταλλάσσεται ανταλλάσσεται μόνο μεταξύ των φορέων που απαρτίζουν αυτό το σύστημα, αγνοώντας τις απώλειες θερμότητας για τα τοιχώματα του δοχείου, για παράδειγμα. Σε αυτήν την περίπτωση, λέμε ότι το δοχείο έχει θερμική χωρητικότητα αμελητέο, δηλαδή δεν απορροφά θερμότητα.
Φανταστείτε την ακόλουθη κατάσταση: σε ένα φλιτζάνι ζεστό τσάι, με αμελητέα θερμότητα, ρίξτε μερικά παγάκια. Προκειμένου να προσδιοριστεί η θερμοκρασία θερμικής ισορροπίας, εκτός από το να γνωρίζουμε τις αρχικές συνθήκες του συστήματος, πρέπει να κάνουμε κάποιες σκέψεις:
Όλη η ποσότητα θερμότητας που δίνει το ζεστό τσάι στον πάγο θα απορροφηθεί πλήρως από αυτό, καθώς το κύπελλο έχει αμελητέα θερμική ικανότητα.
Πρέπει να αγνοήσουμε τις απώλειες θερμότητας στον αέρα και σε οποιοδήποτε άλλο περιβάλλον, έτσι ώστε αυτό το φλιτζάνι τσάι να μπορεί να γίνει κατανοητό ως κλειστό θερμοδυναμικό σύστημα.
Με αυτόν τον τρόπο, μπορούμε να διαπιστώσουμε ότι ολόκληρη η ποσότητα θερμότητας που λαμβάνεται από τον πάγο απορρίφθηκε από το ζεστό τσάι, με αυτό, γράψαμε τον τύπο μας για τον υπολογισμό της θερμικής ισορροπίας:
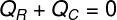
ΕρΡ - Η θερμότητα έλαβε
ΕρΝΤΟ - θερμότητα που δίνεται
Η θερμότητα που δίνεται στο (QΝΤΟ), αναφέρεται στην ποσότητα θερμότητας που μεταφέρθηκε το ζεστό τσάι στους παγάκια που εισήχθησαν σε αυτό. Ήδη η θερμότητα έλαβε (ΕρΡ) είναι η ποσότητα θερμότητας που έλαβαν αυτά τα παγάκια. Αυτή η ποσότητα θερμότητας θα έχει δύο φύσεις: θερμότητα ευαίσθητος και ζεστός λανθάνων, αφού, για να εισέλθουν σε θερμική ισορροπία, οι παγάκια πιθανότατα να λιώσουν.
Προσδιορισμός της θερμοκρασίας θερμικής ισορροπίας
Ας προσδιορίσουμε τη θερμοκρασία θερμικής ισορροπίας από την ακόλουθη κατάσταση:
Ένα φλιτζάνι, με αμελητέα θερμική χωρητικότητα, το οποίο περιέχει 200 ml (200 g) τσαγιού σε αρχική θερμοκρασία 70 ° C, δέχεται 10 g πάγου σε θερμοκρασία -10 ° C. Προσδιορίστε τη θερμοκρασία θερμικής ισορροπίας του συστήματος (υποθέστε ότι η συγκεκριμένη θερμότητα του τσαγιού είναι ίση με τη συγκεκριμένη θερμότητα του νερού):
Δεδομένα:
ντοΝΕΡΟ = 1,0 cal / g ° C
ντοΠΑΓΟΣ = 0,5 cal / g ° C
μεγάλοΠΑΓΟΣ = 80 cal / g
Πρώτον, θεωρούμε ότι όλη η θερμότητα που έλαβε ο πάγος εκχωρήθηκε από το τσάι:

Στη συνέχεια, είναι απαραίτητο να διευκρινιστεί ποιες μορφές θερμότητας δόθηκαν και ελήφθησαν:
Τσάι: Το τσάι έδωσε μόνο λογική θερμότητα (Ερμικρό), καθώς η φυσική του κατάσταση δεν έχει αλλάξει.
Πάγος: Ο πάγος ήταν αρχικά στους -10 ° C, οπότε δέχθηκε αισθητή θερμότητα (Qμικρό) έως τη θερμοκρασία 0 ºC, στη συνέχεια έλαβε λανθάνουσα θερμότητα (Qμεγάλο) σε υγροποίηση. Αφού έγινε υγρό, έλαβε λανθάνουσα θερμότητα (Qμικρό) έως ότου εισέλθει στη θερμική ισορροπία (Tφά) με τσάι.
Μεταφράζοντας όσα αναλύθηκαν παραπάνω με τη μορφή εξίσωσης, θα έχουμε τον ακόλουθο υπολογισμό για επίλυση:
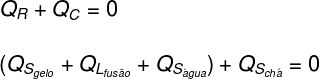
Αντικαθιστώντας τα δεδομένα που παρέχονται από την άσκηση στην παραπάνω εξίσωση, θα πρέπει να επιλύσουμε τον ακόλουθο υπολογισμό:
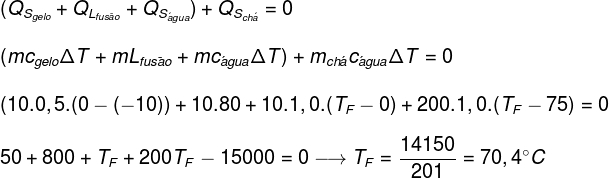
Σύμφωνα με τον παραπάνω υπολογισμό, η θερμοκρασία ισορροπίας του συστήματος τσαγιού + πάγου πρέπει να είναι περίπου 70,4 ° C.
Πείραμα θερμικής ισορροπίας
Για να ελέγξουμε τη θερμική ισορροπία μεταξύ δύο σωμάτων, μπορούμε να πραγματοποιήσουμε πολλά πειράματα. Το απλούστερο από αυτά, ωστόσο, περιλαμβάνει τη χρήση ενός θερμιδόμετρο είναι ένα θερμόμετρο. Το θερμιδόμετρο είναι ένα αδιαβατικό δοχείο (το οποίο δεν επιτρέπει τη διέλευση της θερμότητας), με θερμική χωρητικότητα σχετικά μεαμελητέος, όπως ένα δοχείο επενδεδυμένο με φελιζόλ, για παράδειγμα, το οποίο είναι ένα καλό θερμομονωτικό.

Το θερμιδόμετρο χρησιμοποιείται για τη μέτρηση της διακύμανσης της θερμοκρασίας του εσωτερικού συστήματος.
Θερμική ισορροπία και ζωή στη Γη
Ο ισορροπίαθερμικός παίζει θεμελιώδη ρόλο στην επίγεια ζωή. Χωρίς την παρουσία αερίων θερμοκηπίου στην ατμόσφαιρα της Γης, τα περισσότερα από τα θερμική ακτινοβολία του πλανήτη θα το άφηνε, διαδίδοντας στο διάστημα. Με την πάροδο του χρόνου, αυτό θα προκαλούσε μαζική ψύξη σε όλο τον πλανήτη, κάνοντας τους ωκεανούς να παγώσουν με την πάροδο του χρόνου.
Επιπλέον, οι ωκεανοί διαδραματίζουν βασικό ρόλο ισορροπίαθερμικός του πλανήτη. Λόγω της μεγάλης του ζυμαρικά και θερμότηταειδικός, οι ωκεανοί είναι προικισμένοι με ένα τεράστιο χωρητικότηταθερμικός, Δηλαδή, πρέπει να λαμβάνουν τεράστιες ποσότητες θερμότητας για να αλλάξουν τη θερμοκρασία τους. Για αυτόν τον λόγο, είναι σε θέση να ρυθμίζουν τη θερμοκρασία του πλανήτη πολύ αποτελεσματικά. Περιοχές μακριά από τους ωκεανούς και με λίγο νερό τείνουν να έχουν μεγάλες θερμικές σειρές, όπως στην περίπτωση των ερήμων, οι οποίες είναι εξαιρετικά ζεστές κατά τη διάρκεια της ημέρας και παγώνουν τη νύχτα.
Επομένως, ο ισορροπίαθερμικός Είναι μια διαδικασία θεμελιώδους σημασίας για τη διατήρηση φυσικών, χημικών και βιολογικών διεργασιών στον πλανήτη και, ως εκ τούτου, απαραίτητη για την ύπαρξη ζωής στη Γη.
Από εμένα, Rafael Helerbrock
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/equilibrio-termico.htm