Μέταλλα είναι στοιχεία που χαρακτηρίζονται από φωτεινότητα, αντοχή, θερμική και ηλεκτρική αγωγιμότητα. Αυτοί είναι εφαρμόζεται σχεδόν σε όλες τις βιομηχανικές διεργασίες, να υπάρχει σε μεταλλικά κράματα που χρησιμοποιούνται στην κατασκευή εργαλείων, κοσμημάτων και νομισμάτων και σε χημικές διεργασίες όπως η redox, υπεύθυνη για τη λειτουργία στοίβες και μπαταρίες.
Στον Περιοδικό Πίνακα, ταξινομούνται σε:
ημιμεταλλικά
μέταλλα μετάβασης
αλκαλι μέταλλα
μέταλλα αλκαλικών γαιών
Στη βιομηχανία χάλυβα, χωρίζονται σε:
σιδηρούχα μέταλλα
μη σιδηρούχα μέταλλα
βαριά μέταλλα
Διαβάστε επίσης: Ποια είναι τα νέα στοιχεία του περιοδικού πίνακα;
Χαρακτηριστικά μετάλλων

Είναι, ως επί το πλείστον, εξαιρετικοί αγωγοί θερμότητας και ηλεκτρικής ενέργειας.
Έχουν γυαλιστερή εμφάνιση.
έχουν υψηλό πυκνότητα.
Είναι ηλεκτροθετικά στοιχεία (τείνουν να σχηματίζουν κατιόντα - θετικά φορτία).
Με εξαίρεση το Ερμής, Είναι στοιχεία με υψηλό σημείο τήξης και στερεά σε θερμοκρασία δωματίου.
Έχουν μηχανική αντοχή (αντοχή).
Είναι ελαστικά (μπορούν να διαμορφωθούν χωρίς να σπάσουν).
Μην σταματάς τώρα... Υπάρχουν περισσότερα μετά τη διαφήμιση.)
Περιοδικός πίνακας μετάλλων
αλκαλι μέταλλα
Είναι τα στοιχεία του πρώτη στήλη του περιοδικού πίνακα, οικογένεια 1Α. Ονομάζονται αλκαλικά μέταλλα επειδή, όταν αναμιγνύονται με νερό, σχηματίζουν υδροξείδια, δηλαδή αλκαλικό (βασικό) διάλυμα.
Εσείς στοιχεία που ανήκουν σε αυτήν την ομάδα είναι:
Λίθιο (λι)
Νάτριο (Στο)
Κάλιο (Κ)
Ρουβίδιο (Rb)
Καίσιο (Cs)
Φράγκο (Fr)
Η ηλεκτρονική διαμόρφωση αλκαλικών μετάλλων σε ουδέτερη (μη φορτισμένη / ιονισμένη) κατάσταση εμφανίζεται μόνο ένα ηλεκτρόνιο στο τελευταίο κέλυφος (στρώμα σθένους). Ο ατομική ακτίνα και η αντιδραστικότητα αυτών των μετάλλων αυξάνεται από πάνω προς τα κάτω (παρατηρώντας το Περιοδικός Πίνακας). Έχουν χαμηλό σημείο τήξης σε σύγκριση με άλλα μέταλλα, είναι ελαστικά και όχι πολύ πυκνά, έχουν ματ όψη λόγω της υψηλό δυναμικό οξείδωσης.
Δείτε επίσης:Ποιες είναι οι ιδιότητες της ύλης;
μέταλλα αλκαλικών γαιών
Αυτά είναι στοιχεία που εμφανίζονται στο δεύτερη στήλη του περιοδικού πίνακα, οικογένεια 2Α. λέγονται αλκαλική γη από την τάση σχηματισμού λύσεων βασικού (αλκαλικού) χαρακτήρα, και από τη γη γιατί, πριν από τον 19ο αιώνα, τα οξείδια που σχηματίστηκαν από αυτές τις ουσίες χαρακτηρίστηκαν με αυτόν τον τρόπο. Αυτός ο όρος χρησιμοποιήθηκε για να προσδιορίσει μη αδιάλυτα μέταλλα που δεν υπέστησαν μετάλλαξη όταν θερμάνθηκαν, κοινά χαρακτηριστικά των στοιχείων της ομάδας 2. Αργότερα, υπό το φως νέων ερευνών και πειραμάτων, ανακαλύφθηκε ότι τα στοιχεία της «γης» ήταν στην πραγματικότητα οξείδια που σχηματίστηκαν από μέταλλα.
Είναι εύκαμπτα μέταλλα, με χαμηλή πυκνότητα, έχουν δύο ηλεκτρόνια στο εξωτερικό του κέλυφος, βρίσκονται, υπό κανονικές συνθήκες θερμοκρασίας και πίεσης, σε στερεή κατάσταση. Ανήκει σε αυτήν την ομάδα:
Βηρύλλιο (Είναι)
Μαγνήσιο (Mg)
Ασβέστιο (Εδώ)
Στρόντιο (κ.)
Βάριο (Μπα)
Ραδιόφωνο (Βάτραχος)
μέταλλα μετάβασης
συνθέτουν το ομάδα Β του περιοδικού πίνακα, και βρίσκονται μεταξύ των μετάλλων αλκαλικής γαίας και του αμετάλλους. Ορίστηκαν από το IUPAC ως στοιχεία που έχουν ένα ελλιπές ενεργειακό υπόστρωμα του energéticad. Ο όρος "μέταλλα μετάβασης" αναφέρεται σε μετάβαση από την ομάδα 2 σε 13 στον Περιοδικό Πίνακα και την αυξανόμενη προσθήκη ηλεκτρονίων στην τροχιά «d».
Η ομάδα μετάλλων μετάβασης αποτελείται από πυκνά στοιχεία, με υψηλά σημεία τήξης και βρασμού, και λιγότερο αντιδραστικό από τα μέταλλα της ομάδας 1 και 2 (Οικογένεια 1Α και 2Α). Μεταξύ των μετάλλων μετάβασης είναι το βολφράμιο, το οποίο είναι το στοιχείο με το υψηλότερο σημείο τήξης (3422 ° C), και ο υδράργυρος (Hg), ο οποίος είναι ένα μέταλλο που είναι υγρό υπό κανονικές συνθήκες θερμοκρασίας και πίεσης, το σημείο τήξεως του είναι (-38,83 ° C).
Τα μεταβατικά μέταλλα έχουν διάφορες καταστάσεις οξείδωσης (ΝΟΧ μεταβλητή) και σχηματίζουν έγχρωμες ουσίες.

Στοιχεία εσωτερικής μετάβασης
Στοιχεία εσωτερικής μετάβασης αυτοί είναι:
Λανθάνης: σειρές που αποτελούνται από στοιχεία που έχουν από 57 έως 71 πρωτόνια και τα οποία, με εξαίρεση το προμέθιο, είναι φυσικά.
Ακτινίδες: ομάδα που σχηματίζεται από τα στοιχεία που κυμαίνονται από 89 έως 103 σε ατομικό αριθμό και οι οποίες, ως επί το πλείστον, είναι συνθετικές. Όλη αυτή η ομάδα είναι ραδιενεργός με σύντομο χρόνο ημιζωής.
Τα στοιχεία αυτών των δύο ομάδων έχουν υψηλό σημείο τήξεως και είναι όλα στερεά σε θερμοκρασία δωματίου.
Ημι μέταλλα
Εσείς ημιμεταλλικά υπάρχουν, συνολικά, επτά στοιχεία:
Βόριο (Β)
Πυρίτιο (Si)
Γερμάνιο (Ge)
Αρσενικό (ως)
Αντιμόνιο (Δευ)
Τελλούριο (Te)
Πολώνιο (Po)
Αυτή η ταξινόμηση δίνεται σε στοιχεία που έχουν φυσικοχημικά χαρακτηριστικά που σχετίζονται με μέταλλα και άλλα που σχετίζονται με μη μεταλλικά στοιχεία. Τα ημιμετάλια έχουν λάμψη, είναι εύθραυστα συστατικά, ικανά να σχηματίσουν κατιόντα και επίσης ανιόντα (ανάλογα με την κατάσταση), και είναι ενδιάμεσοι αγωγοί.
Τύποι μετάλλων
Υποσιδηρούχος: ουσίες που περιέχουν σίδηρο στη σύνθεσή τους. Αυτοί είναι μεταλλικά κράματα που περιέχουν σίδηρο ως κοινό στοιχείο, αλλά μπορούν να διαμορφωθούν με διαφορετικές συγκεντρώσεις άνθρακας, Για παράδειγμα, ή σφυρηλατημένο με διαφορετικές τεχνικές, έχοντας έτσι προϊόντα με διαφορετικές φυσικές ιδιότητες.
Μη σιδηρούχα: κράματα που σχηματίζονται από άλλους τύπους μετάλλων, όπως αλουμίνιο, χαλκός, νικέλιο, ψευδάργυρος, τιτάνιο.
Βαριά μέταλλα: μόλυβδος, νικέλιο, ψευδάργυρος, υδράργυρος. Είναι αντιδραστικά, τοξικά και βιοσυσσωρεύσιμα μέταλλα. Χρησιμοποιούνται, μεταξύ άλλων, σε μπαταρίες, λαμπτήρες, πυρομαχικά για πολεμικά αντικείμενα.
Χημικοί δεσμοί μετάλλων
Τα μέταλλα είναι στοιχεία ηλεκτρισμένος θετικά, δηλαδή, έχουν την τάση να χάνουν ηλεκτρόνια σε χημικό δεσμό. Όταν ένα μέταλλο αλληλεπιδρά με ένα μη μέταλλο, αυτό εκτελέστε έναν ιοντικό δεσμό λόγω της διαφοράς σε ηλεκτροαρνητικότητα. Η άλλη δυνατότητα σύνδεσης για μέταλλα είναι μεταλλικοί δεσμοί.
Στο μεταλλικές συνδέσεις συμβαίνουν μεταξύ μετάλλων, με μερική απελευθέρωση ηλεκτρονίων και σχηματισμό νέφους ή θάλασσας ηλεκτρονίων γύρω από τα άτομα, το οποίο εγγυάται στα μεταλλικά μέρη τις ιδιότητες του αγώγιμο ηλεκτρική και ελαστικότητα.
Δείτε επίσης: Αγωγοί και μονωτές - ποιες είναι οι διαφορές;
Λήψη μετάλλων
Τα περισσότερα μέταλλα βρίσκονται φυσικά στο πετρώματα και μέταλλα που σχετίζονται με άλλα στοιχεία. Υπάρχουν πολλές τεχνικές για τον εξευγενισμό των μετάλλων, όπως μέσω της ηλεκτρόλυσης και των χημικών αντιδράσεων σε διαχωρισμούς ενώσεων.
Στην περίπτωση των μετάλλων, οι δύο πιο χρησιμοποιούμενες τεχνικές σε βιομηχανική κλίμακα για την απόκτηση ορισμένου βαθμού καθαρότητας σε ένα μέταλλο είναι: διαφορά του πυκνότητα και μαγνητική ευαισθησία (τάση ότι το μέταλλο πρέπει να αντιδράσει σε α μαγνητικό πεδίο).

λύσεις ασκήσεις
Ερώτηση 1 - (Enem) Το κάδμιο, που υπάρχει στις μπαταρίες, μπορεί να φτάσει στο έδαφος όταν αυτά τα υλικά απορρίπτονται παράνομα στο περιβάλλον ή όταν αποτεφρώνονται. Σε αντίθεση με τη μεταλλική μορφή, τα ιόντα Cd2 + είναι εξαιρετικά επικίνδυνα για το σώμα καθώς μπορούν να αντικαταστήσουν Ιόντα Ca2 +, προκαλώντας εκφυλιστική ασθένεια στα οστά, καθιστώντας τα πολύ πορώδη και προκαλώντας έντονο πόνο στα οστά. αρθρώσεις. Μπορούν επίσης να αναστέλλουν τα ένζυμα που ενεργοποιούνται από το κατιόν Zn2 +, τα οποία είναι εξαιρετικά σημαντικά για τη λειτουργία των νεφρών. Το σχήμα δείχνει τη διακύμανση της ακτίνας ορισμένων μετάλλων και των αντίστοιχων κατιόντων τους.
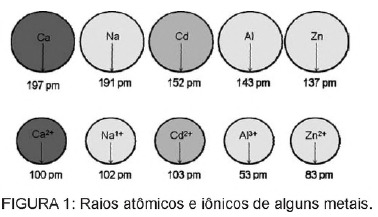
Με βάση το κείμενο, η τοξικότητα του καδμίου στην ιοντική του μορφή είναι συνέπεια αυτού του στοιχείου
Α) παρουσιάζει ενέργεια χαμηλού ιονισμού, η οποία ευνοεί το σχηματισμό του ιόντος και διευκολύνει τη σύνδεσή του με άλλες ενώσεις.
Β) έχουν την τάση να ενεργούν σε βιολογικές διεργασίες που μεσολαβούνται από μεταλλικά κατιόντα με φορτία που κυμαίνονται από +1 έως +3.
Γ) έχουν ακτίνα και φορτίο σχετικά κοντά στα μεταλλικά ιόντα που δρουν σε βιολογικές διεργασίες, προκαλώντας παρεμβολές σε αυτές τις διεργασίες.
Δ) έχουν μεγάλη ιοντική ακτίνα, επιτρέποντάς της να παρεμβαίνει σε βιολογικές διεργασίες στις οποίες συνήθως συμμετέχουν μικρότερα ιόντα.
Ε) να έχει ένα φορτίο +2, το οποίο του επιτρέπει να παρεμβαίνει σε βιολογικές διεργασίες στις οποίες, συνήθως, συμμετέχουν ιόντα με χαμηλότερα φορτία.
Ανάλυση
Εναλλακτική Γ. Το κάδμιο είναι ένα στοιχείο παρόμοιο με τα μεταλλικά ιόντα που φυσικά έχουμε στο σώμα. Εκτός από το ότι είναι βιοσυσσωρεύσιμο, το κάδμιο, που έχει αυτή την ομοιότητα με τις μεταλλικές ομάδες, μπορεί να δεσμευτεί σε ομάδες σουλφυδρυλίου μορίων πρωτεΐνης, προκαλώντας έτσι αλλαγές σε βιολογικές διεργασίες, όπως αφαλάτωση, και καταστροφή ιστών και ερυθρών αιμοσφαιρίων αίμα.
Ερώτηση 2 - Για χαρακτηριστικά που σχετίζονται με μέταλλα, σημειώστε τη λανθασμένη εναλλακτική λύση.
Α) Τα περισσότερα μέταλλα είναι καλοί ηλεκτρικοί και θερμικοί αγωγοί.
Β) Ορισμένα μέταλλα είναι επιρρεπή σε οξείδωση και / ή μείωση.
Γ) Ο σίδηρος είναι ένα ανθεκτικό και εύπλαστο μέταλλο, δηλαδή είναι εύκολο να χυθεί.
Δ) Τα μέταλλα αλκαλικών γαιών έχουν αυτό το όνομα «γη» που αναφέρεται στα οξείδια αυτών των μετάλλων, τα οποία έχουν σκούρο χρώμα.
Ε) Τα μέταλλα είναι στοιχεία ποικίλων χρωμάτων και θαμπό, λόγω της δράσης της οξείδωσης.
Ανάλυση
Εναλλακτική Ε. Τα μέταλλα είναι φυσικά γυαλιστερά και μεταλλικά στο χρώμα, μπορούν να υποστούν οξείδωση, η οποία προκαλεί αλλαγές στα χαρακτηριστικά που σχετίζονται με πτυχή του μέρους, αλλά αυτό δεν είναι ένα φαινόμενο που συμβαίνει σε όλα τα μέταλλα και, σε ορισμένες περιπτώσεις, η οξείδωση εξαρτάται από διάφορους παράγοντες εξωτερικός.
από τη Laysa Bernardes
Καθηγητής Χημείας

