Das Phänomen der Radioaktivität erregte die Aufmerksamkeit zahlreicher Wissenschaftler, darunter des neuseeländischen Physikers Ernest Rutherford (1871-1937). Er führte ein Experiment durch, bei dem ein Strahl von Alphateilchen (α) einem elektrischen Feld ausgesetzt war. Rutherford stellte am Ende des Experiments fest, dass diese Strahlung würde von positiven Teilchen gebildet, da sie vom negativen Pol angezogen wurde.
Das hat er auch gefunden es gab negative Teilchen, die vom positiven Pol angezogen wurden; dies waren die Beta(β)-Partikel.Außerdem hatte diese Strahlung eine höhere Durchdringungskraft als Alphastrahlung.
Es gab jedoch eine der radioaktiven Emissionen, die Reichweite (γ), der sich von keinem der Pole angezogen fühlte. Dies ist sogar energiereicher als andere Strahlungen. Daher wurde der Schluss gezogen, dass Gammastrahlung (γ) besteht nicht aus Partikeln, sondern würde wie Röntgenstrahlen von elektromagnetischen Wellen gebildet, zusätzlich dazu, dass sie keine Ladung oder Masse hat. Da sie keine Ladung hat, wird diese Strahlung im elektrischen Feld nicht gestört.
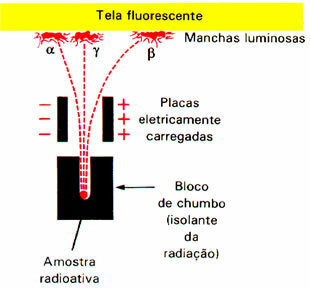
Ein von Rutherford durchgeführtes Experiment zeigte, dass die Alpha- und Beta-Teilchen durch das elektromagnetische Feld abgelenkt wurden.
Diese und andere spätere Studien zeigten, dass das Atommodell von Dalton, in dem das Atom eine Kugel, massiv und unteilbar, wäre, nicht korrekt sein konnte; denn wie oben gesehen, sollte das Atom kleinere Teilchen mit positiver und negativer Ladung haben.
1911, Rutherford schlug vor, dass das Atom aus einem Atomkern bestehen würde, in dem sich die positiven Teilchen befinden, die Protonen genannt werden; und in der Elektrosphäre, also im Bereich um den Kern, würden die negativen Teilchen (Elektronen) auf Kreisbahnen rotieren.
Später fand er selbst heraus, dass Radioaktivität ein Phänomen war, das in instabilen Atomkernen auftrat.
Physiker F. Soddy, A. Russell und K. Fajans entdeckte unabhängig voneinander die entsprechenden Teile dieser Strahlungen innerhalb des Atoms:
*Alpha-Partikel (α):Bei der Emission eines Alphateilchens emittiert das radioaktive Elementatom tatsächlich zwei Protonen und zwei Neutronen (die positive Ladung ist auf die Protonen zurückzuführen);

Wenn ein Element ein Alphateilchen aussendet, sendet es zwei Protonen und zwei Neutronen aus.
*Beta-Partikel (β): Wenn ein radioaktives Element ein Betateilchen emittiert, verliert es ein Elektron und ein Subteilchen, das als Antineutrino bezeichnet wird. Ein Neutron zerfällt, wobei ein im Kern verbleibendes Proton, ein Elektron und ein Antineutrino emittiert werden.
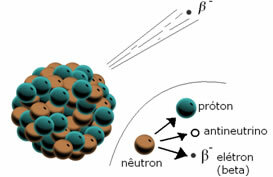
Wenn ein Element ein Beta-Teilchen emittiert, emittiert es ein Elektron.
Daher ist die Charakterisierung dieser drei Strahlungsarten im Folgenden angegeben:
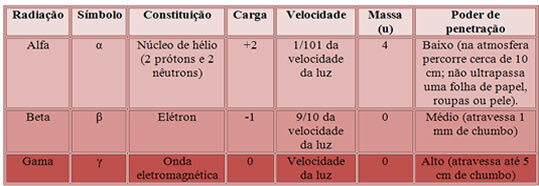
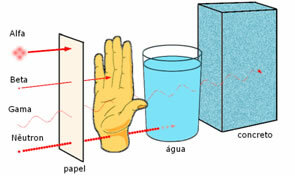
Durchdringungskraft der drei wichtigsten Kernstrahlungen.
Von Jennifer Fogaça
Abschluss in Chemie
Schulteam Brasilien.
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/radioatividade-estrutura-atomo.htm

