Die überwiegende Mehrheit der in der Natur, in unserer Gesellschaft und in unserem Körper vorkommenden Materialien sind keine reinen Stoffe, sondern tatsächlich Mischungen von zwei oder mehr Substanzen.
Obwohl wir Mineralwasser meist nur als „Wasser“ bezeichnen, hat es in Wirklichkeit nicht nur den Reinstoff H2O, weil es das Ergebnis eines Prozesses ist, bei dem Regenwasser in den Boden eindringt und verschiedene Gesteine durchdringt.
Wie der Name schon sagt, enthält es neben Wasser auch mehrere gelöste Mineralien. Wenn Sie neugierig sind, das Etikett eines Mineralwassers zu überprüfen, werden Sie feststellen, dass es in seiner Zusammensetzung enthalten ist Chemie Strontiumsulfate, Calcium, Natrium, Kalium, Natriumbicarbonat, Natriumfluorid, unter anderem Andere.
Mindmap: Mischungen
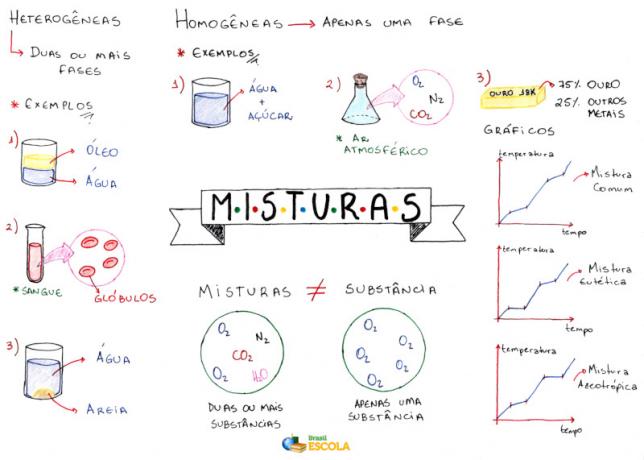
* Um die Mindmap als PDF herunterzuladen, Klicke hier!
Wie kann man einen Stoff von einem Gemisch unterscheiden?
Das unten gezeigte destillierte Wasser ist eine reine Substanz, die nur H. enthält2Ö:

Destilliertes Wasser im Labor verwendet
Optisch sieht es genauso aus wie eine Mischung aus Wasser und Salz; sie können jedoch von der Mischungsdefinition unterschieden werden. Aussehen:
→ Mischungen sind Materialien, deren physikalische Eigenschaften nicht konstant sind, sondern bei einer bestimmten Temperatur und einem bestimmten Druck variieren.
Also, messen Sie einfach die physikalische Eigenschaften, wie Schmelz- und Siedepunkt und Dichte. Wenn sie konstant und wohldefiniert sind, ist es a reine Substanz (im Fall von destilliertem Wasser beträgt seine Dichte bei 4 °C 1,0 g/cm²3 und auf Meereshöhe betragen der Schmelz- und Siedepunkt 0 °C bzw. 100 °C).
Wenn jedoch Variationen präsentiert werden, handelt es sich um eine Mischung. Wenn Sie das Wasser-Salz-Gemisch erhitzen, um den Siedepunkt zu überprüfen, sehen Sie, dass beim Übergang vom flüssigen Zustand in den Gas bleibt die Temperatur nicht konstant, wie bei destilliertem Wasser, das bei 100 °C bleibt, bis sich alle Flüssigkeit dreht Dampf.
Jetzt sind da Mischungen dass es nicht einmal notwendig ist, ihre physikalischen Eigenschaften zu bestimmen, um zu wissen, dass es sich um Mischungen handelt, schauen Sie nur, wie es bei der folgenden Mischung aus Wasser und Öl der Fall ist:

Gemisch aus Wasser und Öl
Dies weist darauf hin, dass es verschiedene Arten von Gemischen gibt, die in homogen und heterogen. Siehe jeden:
Homogene Mischungen:
Sie sind diejenigen, die ein einheitliches Aussehen haben, mit einer einzigen Phase (einzelphase). Beispiele:
Kochsalzlösung (0,9 g Natriumchlorid in 100 ml Wasser);
Kochsalzlösung (36 g Salze wie Natriumchlorid, Magnesiumchlorid, Kaliumjodat, Anti-Feuchthaltemittel und 100 ml Wasser);
hydratisierter Alkohol (Ethanol und Wasser);
Luft (78% Stickstoffgas, 20% Sauerstoffgas, 2% andere Gase und Wasserdampf);
Stahl (Metalllegierung aus 98,5 % Eisen und 1,5 % Kohlenstoff).

Kochsalzlösung, Stahl und Formaldehyd, Beispiele für homogene Mischungen
Die obigen Beispiele zeigen, dass homogene Mischungen sie können in festem, flüssigem oder gasförmigem Zustand vorliegen. Diese homogenen Mischungen heißen Lösungen und sie können nicht durch physikalische Methoden getrennt werden, sondern nur durch chemische Techniken. Um beispielsweise Alkohol aus Wasser zu trennen, ist es notwendig, einen Prozess von Destillation, weil ein Zentrifuge oder Filterung es würde nicht gehen.
Darüber hinaus ist es wichtig zu betonen, dass sie sein müssen homogen auch beim Blick unter ein Ultramikroskop. Mit bloßem Auge können zum Beispiel Milch und Blut homogen erscheinen, aber unter dem Ultramikroskop sehen wir, dass sie es sind heterogen. Sehen Sie sich das Bild des Blutes unter dem Ultramikroskop und seiner einzelnen Phasen an, nachdem es in eine Ultrazentrifuge gegeben wurde:
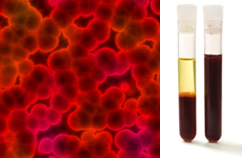
Mikroskopisches Bild und Blutphasen
Heterogene Mischungen:
Sind diejenigen, die mehr als eine Phase haben. Beispiele: Wasser und Öl, Wasser und Sand, Eis und Wasser, Granit, Wasser und Eisen, ungelöstes Salz in Wasser usw.
Die Komponenten von heterogene Mischungen sie treten in den meisten Fällen in verschiedenen physikalischen Zuständen auf und können durch physikalische Methoden getrennt werden. Ein Beispiel tritt auf, wenn wir Kaffee zubereiten und den Feststoff filtern, um ihn von der Flüssigkeit zu trennen.
Dies geschieht jedoch nicht immer, wie im Fall von Öl und Wasser gezeigt, die sich, obwohl beide Flüssigkeiten sind, aufgrund unterschiedlicher Polaritäten seiner Moleküle.
Mentale Karte Von Mutter Victor Ricardo Ferreira
Chemielehrer
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/tipos-misturas.htm
