Ö Ameisensäure hat seinen Namen, weil seine erste Gewinnung durch die Destillation von roten Ameisen (aus dem Lateinischen Resopal = Ameise), die diese Carbonsäure durch ihren Biss injizieren und starke Schmerzen, Schwellungen und Juckreiz verursachen.
Seine offizielle Nomenklatur ist jedoch Methansäure, deren Strukturformel unten dargestellt ist:

Neben Ameisen kommt Methansäure auch in Bienen, Brennnesseln, Kiefern und einigen Früchten vor.
Bei Raumtemperatur ist es farblos, flüssig, ätzend, stark riechend und reizend. Diese Säure wird als Beizmittel, zur Herstellung von Kohlenmonoxid, zur Behandlung von Rheuma, bei der Herstellung von Oxalsäure, als Germizid, als Desinfektionsmittel und bei der Herstellung anderer Produkte Bio.
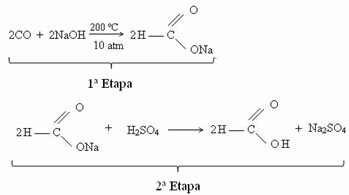
Ameisensäure wird derzeit durch die Reaktion von Kohlenmonoxid und Natronlauge gewonnen. Diese Reaktion ist eine ähnliche Technik wie die 1855 von dem französischen Chemiker Marcellin Berthelot (1827-1907) entwickelte. Als nächstes haben wir diese Reaktion, bei der zunächst Natriummethanoat gewonnen wird, das nach Reaktion mit Schwefelsäure Methansäure als eines der Produkte erzeugt:
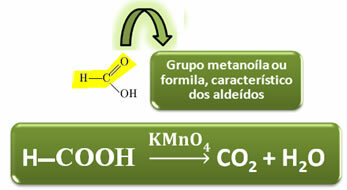
Im Gegensatz zu anderen Carbonsäuren besitzt Ameisensäure die funktionelle Gruppe der Aldehyde, was ihr die Eigenschaft verleiht, als Reduktionsmittel zu wirken. Reduziert Fehling- und Tollens-Reaktionen, die zu Kohlendioxid und Wasser oxidiert werden.
Von Jennifer Fogaça
Abschluss in Chemie

