Um zu verstehen, warum Holz beim Verbrennen nicht schmilzt, erinnern wir uns zunächst daran, was eine geschmolzene Substanz ist, dh sie befindet sich in einem flüssigen Zustand.
Der Unterschied zwischen festem, flüssigem und gasförmigem Zustand besteht nur im Aggregatzustand der Partikel. In den drei Zuständen besteht die Substanz aus den gleichen Teilchen, aber zwischen ihnen ist mehr oder weniger Raum.
Im Festkörper liegen die Teilchen näher beieinander, ohne viel Bewegungsfreiheit. Im flüssigen Zustand haben Partikel mehr Freiheit und können sich bewegen.
Es stellt sich heraus, dass ein Großteil des Holzes (50 %) aus Zellulose besteht, die eigentlich ein Polymer ist. Ein Polymer entsteht durch die Vereinigung mehrerer Moleküle, sogenannter Monomere. Im Fall von Cellulose wird es durch die Vereinigung von Hunderten von β-Glucose-Molekülen gebildet, wie unten gezeigt. Cellulose hat dann die Formel (C6H10Ö5)Nein und erreicht Molekülmassen in der Größenordnung von 400.000 u.
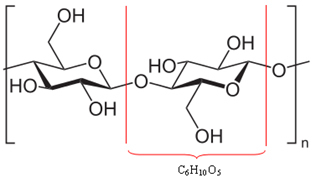
Da es sich um riesige Moleküle handelt, können sich diese Polymere, aus denen Holz besteht, nicht leicht bewegen. Beachten Sie auch, dass die β-Glucose-Moleküle, aus denen Cellulose besteht, Hydroxylgruppen (─ OH) haben. Diese Gruppen binden Wasserstoff aneinander, was die intensivste Art von intermolekularer Kraft ist und das Polymer fest zusammenhält.

Wasserstoffbrückenbindungen zwischen Molekülen, aus denen das Cellulosepolymer besteht*
So, Um diese Bindungen zu lösen, müssten wir so viel Energie in das System stecken, dass sich das Holz noch vor dem Schmelzen zersetzt und dann kein Holz mehr ist.
Holz durchläuft also beim Verbrennen eine chemische Reaktion, die mehr ist als eine einfache Aggregatzustandsänderung. Seine Moleküle zerfallen und rekombinieren mit dem in der Luft vorhandenen Sauerstoff und bilden dann neue Substanzen wie Kohlenstoffgas und Wasser.

* Quelle und Autor des Bildes: laghi.l.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/por-que-madeira-nao-derrete.htm
