GasIdeal ist der, wo die Kollisionen zwischen den Partikeln sind perfekt elastisch. Zwischen seinen Partikeln gibt es keine Interaktion, wie Kräfte anziehend oder abstoßend, außerdem nehmen diese Teilchen keinen Platz ein.
Laut der Kinetische Theorie der Gase, wird der thermodynamische Zustand eines idealen Gases vollständig durch die Variablen von beschrieben Druck, Lautstärke und Temperatur.
Aussehenebenfalls: Kalorimetrie: Mindmap, Formeln und gelöste Übungen
ideales Gaskonzept
Ideale Gase bestehen ausschließlich aus PartikelimMaßepünktlich (von vernachlässigbarer Größe), die in. sind Bewegungchaotisch ist an hochGeschwindigkeit. Bei dieser Gasart sind die Temperatur und die Translationsgeschwindigkeit der Teilchen proportional.
Da zwischen den Teilchen eines idealen Gases keine Wechselwirkung besteht, ist die innere Energie dieses Gases ist immer gleich der Summe der kinetische Energie aller Teilchen, aus denen es besteht.
Was auch immer die idealen Gase sind, sie haben immer die gleichen NummerimPartikel für das gleiche Volumen. Ihre Masse hängt wiederum direkt von Ihrem. ab Molmasse (gemessen in g/mol), zusätzlich 1 mol ideales Gas (ca. 6.0.1023 Teilchen) wird immer a. besetzen Volumen gleich 22,4 l.
Sie GaseReal, wo auftritt von Kollisionenunelastisch zwischen Teilchen, kommen dem Verhalten idealer Gase in Niederdruck- und Hochtemperaturregime. Zufälligerweise sind unter normalen Druck- und Temperaturbedingungen auf der Erde (25 °C und 1 atm) die meisten Gase verhalten sich wie ideale Gase, was die Berechnung von Vorhersagen über das thermodynamische Verhalten erleichtert ihr.
Einige Gase, wie die Wasserdampf, die in der verdünnt wird atmosphärisches Gas, kann nicht als ideale Gase angesehen werden, aber ja GaseReal. Diese Gase haben signifikante Wechselwirkungen zwischen ihren Partikeln, die kondensieren, verursacht sie verflüssigen, wenn es einen gibt Temperaturabfall.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Eigenschaften idealer Gase
Schau es dir an abstrakt, einige Eigenschaften idealer Gase:
- In ihnen treten nur vollkommen elastische Kollisionen zwischen Teilchen auf;
- In ihnen gibt es keine Wechselwirkungen zwischen Teilchen;
- In ihnen haben die Teilchen vernachlässigbare Dimensionen;
- 1 Mol ideales Gas nimmt ein Volumen von 22,4 l ein, unabhängig davon, um welches Gas es sich handelt;
- Reale Gase verhalten sich bei niedrigem Druck und hohen Temperaturen wie ideale Gase;
- Die meisten Gase verhalten sich ähnlich wie ideale Gase.
Ideales Gasgesetz
Die Erforschung von Gasen, die von Wissenschaftlern entwickelt wurden CharlesJunge,JosephLouisschwul-lussac und Robertboyle führte zur Entstehung von drei empirische Gesetze, verwendet, um das Verhalten idealer Gase in Regimen von. zu erklären Temperatur, Druck und VolumenKonstanten, beziehungsweise.
Zusammen bildeten diese Gesetze die notwendige Grundlage für die Entstehung von Ideales Gasgesetz, die die thermodynamischer Anfangszustand eines Gases, definiert durch die Größen P1, T1 und V1, Mit Ihrem thermodynamischer Endzustand (P2, V2 und T2), nachdem ich einiges erlitten hatte Gasumwandlung.
Probier das aus Formel des allgemeinen Gasgesetzes:
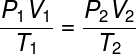
Das allgemeine Gasgesetz besagt, dass die Produkt gibt Druck Pelz VolumenvonGas, geteilt durch die thermodynamische Temperatur in Kelvin ist gleich einer Konstanten. Diese Konstante wiederum wird beschrieben durch die Clapeyron-Gleichung, Uhr:
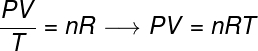
Nein – Molzahl (Mol)
R – universelle Konstante perfekter Gase (0,082 atm.l/mol. K oder 8,31 J/mol. K)
In der Formel, P ist der Druck, den das Gas ausübt, V ist das von diesem Gas eingenommene Volumen und T ist die Temperatur, gemessen in Kelvin. Die Größe Nein bezieht sich auf die Anzahl der Mole, während R ist die universelle Konstante idealer Gase, die oft in der Einheit atm.l/mol gemessen wird. K oder in J/mol. K, wobei letzteres von der übernommen wird SI.
Aussehenebenfalls:Was ist Sonnenwind und wie beeinflusst er die Erdatmosphäre?
Innere Energie des idealen Gases
DAS Energieintern idealer Gase kann man mit dem Produkt zwischen KonstanteimBoltzmann und die thermodynamische Temperatur, beachte:
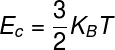
KB – Boltzmann-Konstante (KB = 1,38.10-23 J/K)
Aus der vorherigen Beziehung, die es uns erlaubt, die zu berechnen durchschnittliche kinetische Energie aus den Teilchen eines idealen Gases ziehen wir die folgende Formel, mit der sich berechnen lässt, was die mittlere quadratische Geschwindigkeit von Molekülen eines idealen Gases für eine gegebene Temperatur T beachte:
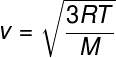
M – Molmasse (g/mol)
Mit dieser Formel können Sie sehen, dass a ZusatzbeimTemperatur eines idealen Gases führt zu einer Zunahme der mittleren quadratischen Geschwindigkeit der Teilchen.
Mehr wissen:Finden Sie heraus, woraus Licht besteht und welche Eigenschaften es hat
Gelöste Übungen zu idealen Gasen
Frage 1) Bei einer Temperatur von 227 °C werden zwei Mol eines idealen Gases bei einem Druck von 1 atm gefunden. Berechnen Sie in Litern das Volumen, das dieses Gas einnimmt.
Daten: R = 0,082 atm.l/mol. K
a) 75 l
b) 82 Liter
c) 15 Liter
d) 27 l
e) 25 l
Vorlage: Buchstabe b
Auflösung:
Um das Volumen dieses Gases zu berechnen, verwenden wir die Clapeyron-Gleichung, jedoch muss vor der Berechnung die Temperatur von 227 °C in Kelvin umgerechnet werden. Dazu addieren wir zu dieser Temperatur den Faktor 273, was eine Temperatur von 500 K ergibt.
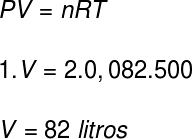
Das vom Gas eingenommene Volumen beträgt laut Auflösung 82 Liter.
Frage 2) Ein ideales Gas nimmt ein Volumen von 20 l ein, wenn es einem Druck von 3 atm ausgesetzt wird, so dass seine Temperatur konstant bleibt, während sich sein Volumen verdreifacht. Berechnen Sie den Enddruck dieses Gases, nachdem es diese Umwandlung durchlaufen hat.
a) 1 atm
b) 3 atm
c) 5 atm
d) 8 atm
e) 9 atm
Vorlage: Buchstabe a
Auflösung:
Um diese Aufgabe zu lösen, verwenden wir das allgemeine Gasgesetz, beachten Sie:
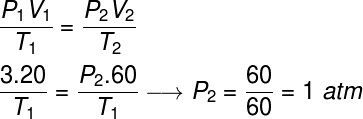
Für die Berechnung musste dem Gas ein Volumen von 60 l zugewiesen werden, da sich sein Volumen bei der Umwandlung verdreifacht hat.
Von Rafael Hellerbrock
Physik Lehrer