Kondensationspolymere, auch Eliminationspolymere genannt, sind solche, bei denen ihre Monomere gleich oder verschieden sind. unter gleichzeitiger Eliminierung von Wassermolekülen oder anderen kleinen Molekülen von Verbindungen, die nicht Teil der Polymer.
Einzige Ausnahme ist Polyurethan: Bei der Kondensationsreaktion, durch die es gewonnen wird, werden keine Moleküle freigesetzt.
Die neben Wasser hauptsächlich freigesetzten Verbindungen sind: Chlorwasserstoff (HCl), Ammoniak (NH3) und Blausäure (HCN).
Die Kondensationspolymere werden immer eine regelmäßige, einheitliche Struktur haben, dh die Polymere werden immer abwechselnd und nicht zufällig auftreten. Copolymere (deren Struktur unregelmäßig ist) können nur gebildet werden, wenn mehr als zwei Monomere zusammenkommen, um das Kondensationspolymer zu bilden.
Betrachtet man Wasser als abgespaltenes Molekül, so ergibt sich folgendes Schema der generischen Kondensationsreaktion zur Bildung dieser Polymere:
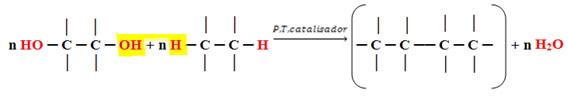
Generische Reaktion zur Bildung von Kondensationspolymeren.
Die wichtigsten und am häufigsten verwendeten Kondensationspolymere in unserer Gesellschaft sind:
• Polyurethan: erhalten durch Kondensation von Paraphenylendiisocyanat mit 1,2-Ethandiol. Es wird in Isolierungen, Raketentreibstoffbindern, Bekleidungsfuttern, Polsterschäumen, Surfbrettern usw. verwendet;

Produkte aus Polyurethan.
• Bakelit: Bakelit bildende Stoffe sind Benzol und Methanol. Es wird in Beschichtungen wie Farben und Lacken, Holzleimen, Topfgriffen, Lichtschaltern, Steckdosen, Steckern, Abdeckungen usw. verwendet;
• Polyester: sie sind Polymere, die aus mehreren Estern bestehen, und zu ihrer Bildung werden eine Säure und ein Alkohol benötigt. Der Hauptpolyester ist PET (Polyethylentereflat), das durch die Vereinigung von Terephthalsäure mit Ethandiol gebildet wird. Es wird bei der Herstellung von Textilfasern wie Tergalgewebe, bei der Herstellung von Softdrinkflaschen und anderen Getränken, Videobändern, Herzgefäße und -klappen, unter anderem als Schutz zur Erleichterung der Wiederherstellung von organischem Gewebe, das Verbrennungen erlitten hat;
• Nylon oder Polyamid: übliche Nylonmonomere (Nylon 66) sind Hexandisäure und 1,6-Hexandiamin. Seine Anwendungen finden sich in schmierfreien Lagern, Getrieben, Verpackungen, Textilfasern, Klettbändern, Bürstenborsten, Angeldrähten und elektrischem Zubehör;

Socken aus Nylon
• Kevlar®: es entsteht durch die Vereinigung von Terephthalsäure und p-Benzoldiamin. Es wird hauptsächlich in schusssicheren Westen sowie in Rennwagenchassis, in Rennfahrerbekleidung, in Feuerwehrbekleidung und in Flugzeugteilen eingesetzt;

Kugelsichere Westen zum Schutz von Soldaten und Polizisten werden aus Kevlar®-Polymer hergestellt
• Polycarbonat: Polycarbonat wird aus Phosgen und p-Isopropylendiphenol gebildet und wird häufig in kugelsicherem Glas, in Sonnenbrillengläsern, CDs und DVDs, Röntgengeräte, Sicherheitsfenster und Strukturen zur Abdeckung bestimmter Bereiche (wie in der Abbildung gezeigt) unten);

Struktur auf Basis von Polycarbonat.
• Silikone: gebildet von Silizium als Hauptelement, dessen Atome sich mit denen des Elements Sauerstoff abwechseln und Silizium an organische Radikale bindet. Das gebräuchlichste Silikon ist Dichlo-Dimethyl-Silan. Die Anwendungen dieser Verbindungen sind: durch plastische Chirurgie eingesetzte Prothesen, Schmierung von Formen, Fensterdichtungen, verkapselte Harze, Kosmetika wie Öle und Hautcremes, u.a Andere.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/polimeros-condensacao.htm