Wenn der Benzolring bereits einen Substituenten hat, beeinflusst dieser Rest alle anderen H-Substitutionen am Ring. Dieser Substituent kann ortho- und para-Director oder meta-Director sein. Aber es stellen sich die Fragen:
| Was bewirkt, dass die an den Benzolring gebundene Gruppe die Richtung und Reaktivität der Substitutionsreaktion beeinflusst? |
| Was macht bestimmte Gruppen zu Zielberatern (deaktivierend) und andere ortho-para (aktivierend)? |
Diese beiden Fragen werden beantwortet, wenn man die Berufungen versteht. elektronische Effekte dass diese Gruppen im Ring trainieren. Dieser Effekt tritt aufgrund der Elektronegativitätsunterschied zwischen den Elementen, da der Substituent polarisieren die Bindungen des aromatischen Kerns, wobei einige Ringkohlenstoffe abwechselnd einen positiven Charakter induzieren, während andere einen negativen Charakter haben.
| Eine neue Substitution wird in den Kohlenstoffatomen auftreten, die Charakter haben Negativ. |
Sehen wir uns an, wie diese elektronischen Effekte im aromatischen Ring auftreten, und bedenken Sie dabei die Reihenfolge der Elektronegativität der Elemente: F > O > N > Cl > Br > S > C > I > H.
1. Fall: Radikal aktivierend oder ortho-to-director:
Im Fall unterhalb des Benzol(Phenol)-Moleküls ist beispielsweise Sauerstoff das elektronegativste Element, also es zieht Elektronen an sich, wodurch der Kohlenstoff eine teilweise positive Ladung hat, die induziert alternierende Ringpolarisation. Die negativen Positionen sind genau die ortho- und para-Positionen. Darum die -OH-Gruppe ist ein aktivierendes Radikal oder ortho-zu-Direktoren. Dies ist in der folgenden Phenolnitrierungsreaktion zu sehen, bei der als Produkte o-Nitrophenol und p-Nitrophenol entstehen:
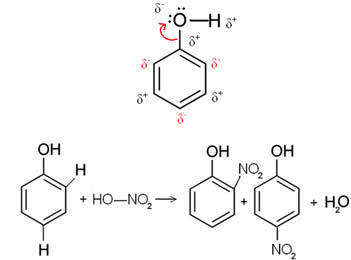
2. Fall: Deaktivierung von Radikalen oder Meta-Leadern:
Betrachten wir nun den Fall von Nitrobenzol:
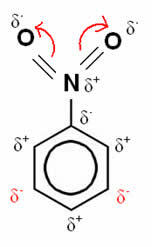
In diesem Beispiel bleibt Sauerstoff das elektronegativste Element, sodass es die mit Stickstoff hergestellten Bindungen an sich zieht. die teilweise positiv geladen ist, was dazu führt, dass das daran gebundene Kohlenstoffatom negativ polarisiert wird und so nacheinander. Somit ist die Position, die negativ wird und am anfälligsten für Substitutionen wird, die Position Tor, also a. sein deaktivieren.
Sehen Sie sich jetzt diesen elektronischen Effekt genauer an, der als bezeichnet wird Resonanzeffekt.
| Resonanzeffekt es ist die Anziehung oder Abstoßung von Elektronen an π(pi)-Bindungen von Doppel- oder Dreifachbindungen, wenn sie mit dem Benzolring selbst in Resonanz treten. |
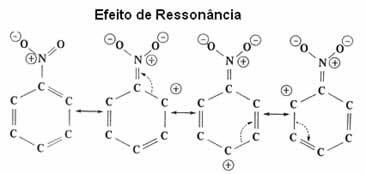
Wie zu sehen ist, deaktiviert die NO2-Gruppe den Ring, da sie ihm Elektronen entzieht und seine Elektronendichte verringert. Somit ist die Gruppe, die angreift und die Substitution (Elektrophil) durchführt, positiv, so dass sie vorzugsweise die Metaposition angreift, die eine negative Ladung erhalten hat.
Diese Tatsache zeigt sich bei der Monochlorierungsreaktion von Nitrobenzol, bei der die Substitution nur in meta-Position erfolgt:
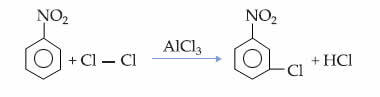
Von Jennifer Fogaça
Abschluss in Chemie
Brasilianisches Schulteam
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/efeitos-eletronicos-radicais-meta-orto-para-dirigentes.htm

