A Zweiter Hauptsatz der Thermodynamik bestimmt, welche Bedingungen dafür gelten Hitze in Wärmekraftmaschinen und Kühlschränken in Arbeit umgewandelt werden. Es befasst sich auch mit der Definition von Entropie als ein Phänomen, das die Desorganisation von Teilchen in physikalischen Systemen messen kann.
Lesen Sie auch: Kalorimetrie – der Zweig der Physik, der den Wärmeaustausch untersucht
Zusammenfassung zum zweiten Hauptsatz der Thermodynamik
Der zweite Hauptsatz der Thermodynamik wird durch die Clausius- und Kelvin-Planck-Aussagen dargestellt.
Die Clausius-Aussage befasst sich mit dem Wärmefluss vom heißeren Körper zum kälteren Körper.
Die Kelvin-Planck-Erklärung befasst sich mit der Unfähigkeit thermischer Geräte, ihre gesamte Wärme in umzuwandeln arbeiten.
Der zweite Hauptsatz der Thermodynamik wird auf Wärmekraftmaschinen und Kühlschränke angewendet.
Der Carnot-Zyklus ist der Zyklus mit dem höchsten Wirkungsgrad, der von Wärmekraftmaschinen erzielt wird.
Der Carnot-Zyklus besteht aus vier Phasen: einer reversiblen isothermen Expansion, einer reversiblen adiabatischen Expansion, einer reversiblen isothermen Kompression und einer reversiblen adiabatischen Kompression.
Der Satz von Carnot bezieht sich auf die Ausbeute von Carnot-Maschinen.
Was ist der zweite Hauptsatz der Thermodynamik?
Der zweite Hauptsatz der Thermodynamik ist a Gesetz, das sich mit den Einschränkungen befasst, die in thermodynamischen Prozessen auftreten. Es wurde von den Physikern Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) und Max Planck (1858-1947) formuliert, wie wir unten sehen werden:
Der Physiker und Mathematiker Rudolf Clausius stellte fest, dass der Wärmeleitungsfluss vom Körper mit höherer Temperatur zum Körper mit niedrigerer Temperatur erfolgt. niedrigere Temperatur, daher ist es nicht natürlich, dass der umgekehrte Prozess auftritt, daher ist es notwendig, daran zu arbeiten System. Damit erklärte er:
Es ist unmöglich, einen Prozess durchzuführen, dessen einzige Wirkung darin besteht, Wärme von einem kälteren Körper auf einen heißeren Körper zu übertragen.|1|
Der mathematische Physiker William Thomson, bekannt als Lord Kelvin, zusammen mit den Beiträgen des Physikers Max Planck, stellte die Unmöglichkeit thermischer Geräte mit einem Wirkungsgrad von 100 % fest, da es immer zu Wärmeverlusten kommt.
Anwendungen des zweiten Hauptsatzes der Thermodynamik
Der zweite Hauptsatz der Thermodynamik wird auf Wärmekraftmaschinen und Kühlschränke angewendet.
Zweiter Hauptsatz der Thermodynamik in Maschinen Thermal-
Zum Thermomaschinen sind in der Lage, Wärme in Arbeit umzuwandeln. Eine heiße Quelle versorgt die Wärmekraftmaschine mit Wärme, die diese in Arbeit umwandelt. Der Rest der Wärme wird an die Kältequelle weitergeleitet, wie im Bild unten dargestellt:
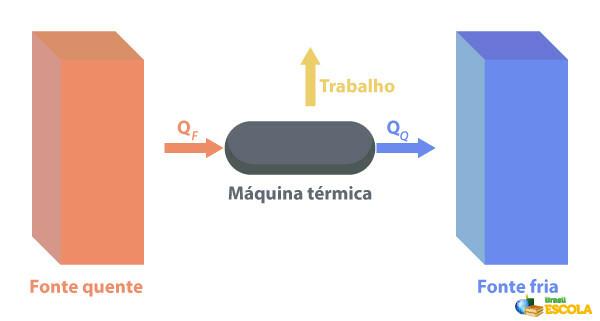
Einige Beispiele für thermische Maschinen sind: Dampf- und Kerosinturbinen in Düsenflugzeugen, Verbrennungsmotoren, thermonukleare Reaktoren.
Zweiter Hauptsatz der Thermodynamik in Kühlschränken
Kühlschränke sind Maschinen, die Sie funktionieren entgegengesetzt zu Wärmekraftmaschinen., wobei sie einer Region Wärme entziehen Temperatur niedrigere Temperatur und liefern es an eine Region mit höherer Temperatur. Da dies nicht natürlich ist, ist es notwendig, dass die Maschine Arbeiten mit elektrischer Energie verrichtet, wie in der Abbildung unten beschrieben:
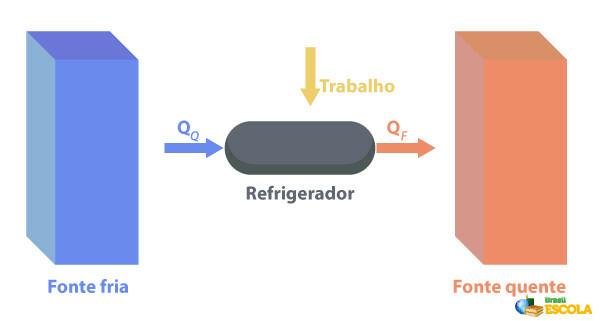
Einige Beispiele für Kühlschränke sind Kühlschränke und Klimaanlagen.
Entropie und der zweite Hauptsatz der Thermodynamik
A Der zweite Hauptsatz der Thermodynamik geht von der Existenz von Entropie aus, eins physikalische Größe Verantwortlich für die Messung des Grades der Desorganisation von Partikeln in einem physikalischen System oder des Grades der Irreversibilität von thermodynamische Prozesse, die an Wärmekraftmaschinen beteiligt sind, da sie ein spontaner, unvermeidlicher, irreversibler und unumkehrbarer Prozess sind expansiv. Damit ist es lediglich möglich, den Grad der Volatilität der Prozesse zu beobachten und einzudämmen. Mit zunehmender Entropie nimmt auch der Grad der Unordnung im System zu.
A Die Entropie-Nomenklatur ist griechischen Ursprungs und bedeutet „Transformation“., „verändern“, wird daher in der verwendet Körperlich um Zufälligkeit und Unordnung anzuzeigen. Die Entropie kann mit der Formel berechnet werden:
\(∆S=\frac{∆U}T\)
\(∆S\) ist die Entropieänderung, gemessen in [J/K].
\(∆U\) ist die Änderung der inneren Energie, gemessen in Joule [J].
T ist die Temperatur, gemessen in Kelvin [K].
Aus statistischer Sicht wird die Entropie nach der Formel berechnet:
\(S=k\cdot ln\ Ω\)
S ist die Entropie, gemessen in [J/K].
k ist die Boltzmann-Konstante, es lohnt sich \(1,4\cdot 10^{-23}\ J/K\).
Ω ist die Anzahl der möglichen Mikrozustände für das System.
Lesen Sie auch: Wärmeausbreitungsprozesse
Formeln des zweiten Hauptsatzes der Thermodynamik
Thermomaschinen und Kühlschränke
\(Q_Q=W+Q_F\)
\(Q_Q\) ist die Wärme der heißen Quelle, gemessen in Joule [J].
W ist die von der Wärmekraftmaschine geleistete Arbeit, gemessen in Joule [J].
\(Q_F\) ist die Wärme der Kältequelle, gemessen in Joule [J].
Es kann dargestellt werden durch:
\(W=Q_Q-Q_F\)
W ist die von der Wärmekraftmaschine geleistete Arbeit, gemessen in Joule [J].
\(Q_Q\) ist die Wärme der heißen Quelle, gemessen in Joule [J].
\(Q_F\) ist die Wärme der Kältequelle, gemessen in Joule [J].
Kühlschränke
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) ist die Effizienz des Kühlschranks.
\(Q_F\) ist die Wärme der Kältequelle, gemessen in Joule [J].
\(Q_Q\) ist die Wärme der heißen Quelle, gemessen in Joule [J].
Es kann wie folgt dargestellt werden:
\(η=\frac{Q_F}W\)
\(η\) ist die Effizienz des Kühlschranks.
\(Q_F\) ist die Wärme der Kältequelle, gemessen in Joule [J].
W ist die von der Wärmekraftmaschine geleistete Arbeit, gemessen in Joule [J].
Beispiele der Anwendung von Formeln
Beispiel 1: Berechnen Sie die Arbeit, die eine Wärmekraftmaschine während eines Zyklus verrichtet, der 500 J Wärme von der heißen Quelle erhält und nur 400 J Wärme an die kalte Quelle überträgt.
Um die Arbeit einer Wärmekraftmaschine zu berechnen, verwenden wir die Formel:
\(W=Q_Q-Q_F\)
Ersetzen der in der Anweisung angegebenen Werte:
\(B=500-400\)
\(W=100\ J\)
Die Arbeit der Wärmekraftmaschine betrug 100 Joule.
Beispiel 2: Wie hoch ist der Wirkungsgrad eines Kühlschranks, der 150 J Wärme von der heißen Quelle aufnimmt und 50 J Wärme an die kalte Quelle überträgt?
Um die Effizienz eines Kühlschranks zu berechnen, verwenden wir die Formel:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
Wenn wir die in der Anweisung angegebenen Werte ersetzen, erhalten wir:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
Multiplikation der Rendite mit 100 %:
\(η=0,5\cdot100%\)
\(η=50\%\)
Der Kühlschrank hat einen Wirkungsgrad von 50 %.
Carnot-Zyklus
Der Carnot-Zyklus war entwickelt vom Wissenschaftler Sadi Carnot (1796-1832), mit dem Ziel, den maximalen Wirkungsgrad zu ermitteln, der von einer Wärmekraftmaschine erreicht werden kann, die zwischen einer heißen Quelle und einer kalten Quelle arbeitet.
Basierend auf seinen Studien stellte Carnot fest, dass dies der Fall ist, um die maximale Effizienz einer Wärmekraftmaschine zu erzielen notwendig, damit sein Prozess reversibel ist, also entwickelte er den Zyklus der maximalen Ausbeute, der als Zyklus bezeichnet wird Carnot und die Die darin arbeitende Wärmekraftmaschine wird Carnot-Wärmekraftmaschine genannt.. Da der Carnot-Zyklus reversibel ist, kann er umgekehrt werden, und so wurden Kühlschränke entwickelt.
Der Carnot-Zyklus besteht unabhängig von der verwendeten Substanz aus vier Prozessen, die in der Druck-Volumen-Grafik (p×V) beschrieben sind, wie wir im Bild unten sehen können:
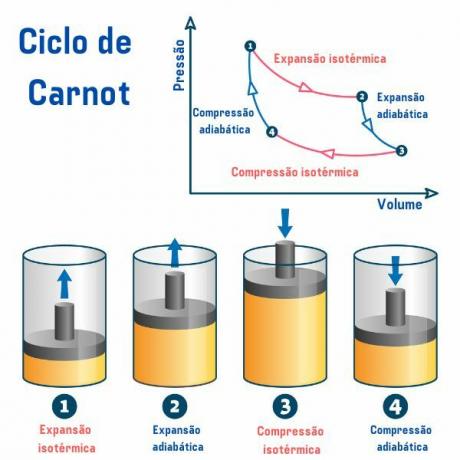
1. Vorgang, von Punkt 1 → 2: Es gibt eine reversible isotherme Expansion (Prozess, bei dem die Temperatur konstant bleibt), bei der das Gas (oder System) arbeitet und eine Wärmemenge von der heißen Quelle aufnimmt.
2. Vorgang, von Punkt 2 → 3: Es gibt eine adiabatische Expansion (Prozess, bei dem ein Wärmeaustausch mit der Außenumgebung stattfindet), reversibel, bei dem kein Wärmeaustausch stattfindet Wärme mit thermischen Quellen, aber das Gas arbeitet und es kommt zu einer Abnahme seiner inneren Energie, was zu einer Abnahme der führt Temperatur.
3. Prozess, von Punkt 3 → 4: Es kommt zu einer reversiblen isothermen Kompression, bei der das Gas Arbeit aufnimmt und eine gewisse Wärmemenge an die Kältequelle abgibt.
4. Prozess, ab Punkt 4 → 1: Es kommt zu einer reversiblen abatischen Verdichtung, bei der kein Wärmeaustausch mit den Wärmequellen stattfindet und das Gas nicht brennt erhitzt, bis es die Temperatur der heißen Quelle erreicht, und wird dann mit dieser in Kontakt gebracht, wodurch die Temperatur beendet wird Zyklus.
Gesetze der Thermodynamik
Die Gesetze der Thermodynamik sind vier Gesetze, die das gesamte Studium der Thermodynamik regeln Thermodynamik, untersuchen Sie die Beziehungen zwischen Volumen, Temperatur und Druck und anderen physikalischen Größen wie Wärme und Energie.
Nullter Hauptsatz der Thermodynamik: ist das Gesetz von thermisches GleichgewichtEs untersucht den Wärmeaustausch zwischen Körpern mit unterschiedlichen Temperaturen.
erster Hauptsatz der Thermodynamik: ist der Energieerhaltungssatz in thermodynamischen Systemen. Er untersucht die Umwandlung von Wärme in Arbeit und/oder innere Energie.
Zweiter Hauptsatz der Thermodynamik: Es ist das Gesetz, das sich mit Wärmekraftmaschinen, Kühlschränken und Entropie befasst.
Dritter Hauptsatz der Thermodynamik: ist das Gesetz von Absoluter NullpunktSie untersucht die Auswirkungen dieser Temperatur.
Lesen Sie auch: Leistung von Wärmekraftmaschinen
Gelöste Übungen zum zweiten Hauptsatz der Thermodynamik
Frage 1 Bestimmen Sie die Temperatur der heißen Quelle eines Carnot-Motors, wobei Sie wissen, dass die Temperatur der kalten Quelle 450 K und ihr Wirkungsgrad 80 % beträgt.
a) 2250K
b) 450.000
c) 1500K
d) 900K
e) 3640K
Auflösung:
Alternative A. Wir berechnen die Temperatur der heißen Quelle anhand der Effizienzformel eines Carnot-Motors:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1-\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
Frage 2 (Cefet-PR) Das 2. Prinzip der Thermodynamik lässt sich wie folgt formulieren: „Es ist unmöglich, eine Maschine zu bauen.“ Wärmeenergie, die in Kreisläufen arbeitet und deren einzige Wirkung darin besteht, einer Quelle Wärme zu entziehen und sie vollständig in sie umzuwandeln arbeiten". Im weiteren Sinne führt uns dieses Prinzip zu folgender Schlussfolgerung:
a) Es ist immer möglich, thermische Maschinen zu bauen, deren Wirkungsgrad 100 % beträgt.
b) Jede Wärmekraftmaschine benötigt nur eine Wärmequelle.
c) Wärme und Arbeit sind keine homogenen Größen.
d) Jede Wärmekraftmaschine entzieht einer heißen Quelle Wärme und gibt einen Teil dieser Wärme an eine kalte Quelle ab.
e) Nur mit einer Kältequelle, die immer auf 0 °C gehalten wird, wäre es einer bestimmten Wärmekraftmaschine möglich, Wärme vollständig in Arbeit umzuwandeln.
Auflösung:
Alternative D. Dieses Prinzip zeigt uns, dass es unmöglich ist, der heißen Quelle die gesamte Wärme zu entziehen und an die kalte Quelle zu übertragen.
Notiz
|1| Grundkurs Physik: Flüssigkeiten, Schwingungen und Wellen, Wärme (Bd. 2).
Von Pamella Raphaella Melo
Physik Lehrer
Quelle: Brasilien-Schule - https://brasilescola.uol.com.br/fisica/segunda-lei-da-termodinamica.htm

