Wir werden in diesem Text sehen, wie a Diagramm von Zustandsänderung zu jedem reine Substanz, wie diese Art von Diagramm zu interpretieren ist und wie das Diagramm von Gemischen dargestellt wird.
Betrachten wir dazu das Beispiel Wasser. Stellen Sie sich vor, wir nehmen ein Glas Eis mit einer Temperatur von –10 °C und starten einen Heizprozess unter einem Druck von 1 atm. Wenn die Temperatur steigt, von -10 ºC auf -9 ºC, auf -8 ºC usw., bleibt das Eis in einem festen Zustand, bis es eine Temperatur von 0 ºC erreicht.
An diesem Punkt beginnt es, in einen flüssigen Zustand überzugehen, dh es beginnt eine Fusion. Die Temperatur steigt nicht wie bisher weiter an, sondern bleibt konstant bei 0°C, bis das gesamte Eis geschmolzen ist:

Nach dem Schmelzen des gesamten Feststoffs wird die Temperatur des Systems weiter ansteigen, bis eine Temperatur von 100 °C erreicht ist. Bei dieser Temperatur beginnt das Wasser, das sich im flüssigen Zustand befand, in den dampfförmigen Zustand überzugehen, dh es wird zu kochen.
So wie es im. passiert ist Schmelzpunkt, am Siedepunkt bleibt die Temperatur ebenfalls konstant, bis die gesamte Flüssigkeit in Dampf übergeht. Wenn wir das System danach weiter heizen, steigt die Temperatur weiter an:
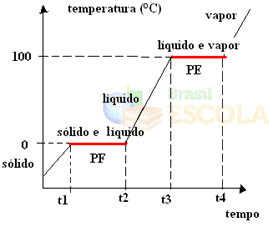
Bereit! Dies ist der Graph oder das Diagramm, das die Änderung des physikalischen Zustands von Wasser oder seiner Heizkurve darstellt. Wäre es der umgekehrte Vorgang, hätten wir die folgende Wasserkühlungskurve:
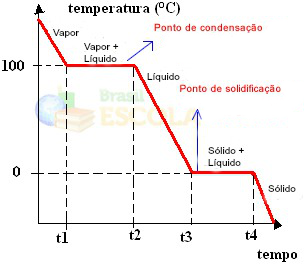
Ein sehr wichtiger Aspekt dieser Graphen ist, dass sie von zwei Ebenen gebildet werden, dh es gibt zwei Punkte, an denen die Temperatur für eine Weile konstant bleibt. Dies geschieht immer bei der Zustandsänderung einer reinen Substanz. Der einzige Unterschied sind die Schmelz- und Siedepunktwerte.
Sauerstoff zum Beispiel ist im Gegensatz zu Wasser keine Flüssigkeit, sondern bei Raumtemperatur (ca. 20 °C) ein Gas. Dies liegt daran, dass sein Schmelzpunkt auf Meereshöhe -223,0 °C und sein Siedepunkt -183,0 °C beträgt. Sehen Sie sich Ihr Diagramm zur Änderung des physischen Zustands an:

Gemeinsame Mix-Grafiken
Wenn wir eine Mischung erhitzen oder abkühlen, haben Schmelzpunkt und Siedepunkt nicht not ermittelten und konstanten Werten, d. h. die beiden in den Diagrammen beobachteten Niveaus werden nicht gebildet über.
Änderungen der physikalischen Zustände treten eher über Temperaturbereiche als über einen festen Betrag auf. Der Schmelzpunkt zum Beispiel beginnt bei einer bestimmten Temperatur und endet bei einer anderen, und das gleiche passiert mit dem Siedepunkt, wie in der folgenden Grafik dargestellt:
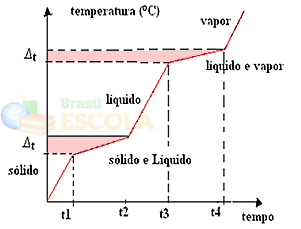
Zwei Ausnahmen sind eutektische und azeotrope Mischungen. Sehen Sie, was mit ihnen passiert:
a) Eutektische Mischung
Das eutektische Gemisch verhält sich beim Aufschmelzen wie ein Reinstoff, dh die Temperatur bleibt dann vom Beginn bis zum Ende der Aggregatzustandsänderung konstant.

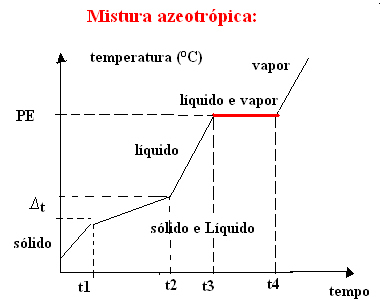
b) azeotrope Mischung
Das azeotrope Gemisch verhält sich beim Sieden wie ein Reinstoff, d. h. an dieser Stelle bleibt die Temperatur vom Beginn bis zum Ende der Aggregatzustandsänderung konstant.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm


