Beim Substanzen sind solche Materialien mit konstanter chemischer Zusammensetzung und die ihre physikalische Eigenschaften gut definiert, wie Schmelz- und Siedepunkte und die Dichte, nicht in gewisser Weise variieren Temperatur und Druck.
Das in Laboratorien verwendete destillierte Wasser ist beispielsweise a reine Substanz nur von H-Molekülen gebildet2O (das ist seine konstante chemische Zusammensetzung) und hat bei einem Druck von 1 atm (auf Meereshöhe) immer einen Schmelzpunkt von 0 °C, einen Siedepunkt von 100 °C und eine Dichte von 1,0 g /ml bei 4°C. Siehe zwei weitere Beispiele:
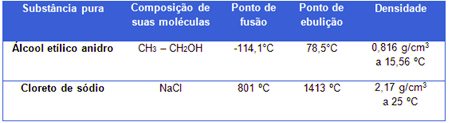
Physikalische Eigenschaften von Alkohol und Natriumchlorid
Es gibt zwei Arten von Substanzen, einfache und zusammengesetzte:
Das) einfache Stoffe
Sind diejenigen, deren Moleküle nur von einer einzigen Art von gebildet werden? Chemisches Element. Die Atome der Elemente können in isolierter Form als monoatomare Substanzen auftreten oder zweiatomige und dreiatomige Moleküle bilden. Beispiele:
Monoatomisch: ist der Fall von Heliumgas (He), a
Primärgas die in der Natur isoliert erscheint, und auch von der Eisen (Fe) und der Aluminium (Al), die sind Metalle. Siehe den Text Metallische Verbindung zu verstehen, wie die Atome dieser Elemente zusammenbleiben;Kieselalgen: das in der atmosphärischen Luft vorhandene Sauerstoffgas besteht aus Molekülen, die jeweils von zwei Sauerstoffatomen gebildet werden, O2, und Wasserstoffgasmoleküle werden von zwei Wasserstoffatomen gebildet, H2;
Triatomie: Ö Ozongas wird von drei Sauerstoffatomen gebildet, O formed3.
B) zusammengesetzte Stoffe
Sind diejenigen, deren Moleküle oder ionische Cluster aus zwei oder mehr chemischen Elementen bestehen oder Ionen. Wasser, Alkohol und Natriumchlorid, die oben erwähnt wurden, werden alle als zusammengesetzte Stoffe klassifiziert oder chemische Verbindungen, da sie aus verschiedenen Elementen bestehen (Wasserstoff, Sauerstoff, Kohlenstoff, Natrium und Chlor).
Weitere Beispiele: Kohlendioxid (CO2), Kohlenmonoxid (CO), Methan (CH4) und Ammoniak (NH3).
Zusammengesetzte Stoffe können in einfache Stoffe zerlegt werden. Wenn wir beispielsweise einen elektrischen Strom über geschmolzenes Natriumchlorid leiten, a redox Reaktion wodurch zwei einfache Substanzen entstehen, metallisches Natrium (Na(s)) und Chlorgas (Cl2(g)). Dieser Vorgang ist bekannt als Eruptivelektrolyse von Natriumchlorid.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/substancias-simples-compostas.htm


