Carbonate sind anorganische Verbindungen, die durch die ionische Bindung eines Metalls oder Halbmetalls mit dem Carbonatanion CO. gebildet werden32-.
Kohlenstoff ist vierwertig, das heißt, er hat vier Elektronen in der Valenzschale und kann vier kovalente Bindungen stabil machen. während Sauerstoff zweiwertig ist, sechs Elektronen in der Valenzschale hat und zwei stabile Bindungen eingehen kann, mit acht Elektronen. Daher besteht eine starke Tendenz für einen Kohlenstoff, an zwei Sauerstoffatome zu binden, die alle stabil sind (O C ═ O → CO2).
Aber auch anderer Sauerstoff kann sich mit Kohlenstoff verbinden, da das Verhältnis der Ionenradien zu einer Koordinationszahl von 3 führt und eine Struktur bildet dreieckig, in dem sich der Kohlenstoff in der Mitte befindet und eine Doppelbindung mit einem der Sauerstoffatome und zwei Einfachbindungen mit den anderen beiden bildet Sauerstoff. Das Ergebnis sind zwei überschüssige Elektronen, da diese beiden Sauerstoffe nicht stabil sind und jeweils ein Elektron aufnehmen müssen:
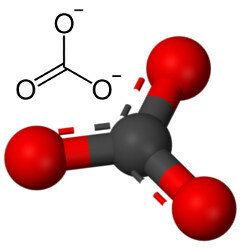
Das Carbonatanion wird durch kovalente Bindungen gebildet, aber seine Verbindungen, die anorganische Salze und Mineralien sind bekannt als Carbonate, sind ionisch, da dieses Radikal zwei Elektronen von einem Metall oder Halbmetall erhält und ein Ionenverbindung.
Diese Verbindungen sind mit Ausnahme von Ammoniumcarbonat ((NH4)2CO3) und mit Alkalimetallen gebildete Carbonate (Elemente der Familie 1: Li, Na, K, Rb, Cs und Fr). Fast alle sind weiße Feststoffe, wie im Bild unten gezeigt:

Die beiden häufigsten und wichtigsten alltäglichen Beispiele für Carbonate sind Natriumcarbonat (Na2CO3) und Calciumcarbonat (CaCO3). Im ersten Fall gehört Natrium zur Familie 1, das ein Elektron in der Valenzschale hat und dazu neigt, dieses Elektron zu verlieren, um stabil zu werden. Da das Carbonatanion zwei Elektronen aufnehmen muss, bindet es an zwei Natriumatome:

Soda ist besser bekannt als Soda oder Soda und wird bei der Herstellung von Seifen, Farbstoffen, Medikamenten, Papieren und bei der Aufbereitung von Schwimmbadwasser verwendet. Seine Hauptanwendung liegt jedoch bei Calciumcarbonat und Sand bei der Glasherstellung.
Calcium gehört zur Familie 2 und hat die Tendenz, zwei Elektronen zu verlieren. So bindet ein Calciumatom an ein Carbonatradikal:

Calciumcarbonat ist in Kalkstein und Marmor enthalten. Beim Stalaktiten und Stalagmiten die in Höhlen existieren, bestehen aus diesem Karbonat; Muscheln, Korallenriffe und Eierschalen. Wenn wir Wände, Baumstämme und andere Stellen tünchen, verwenden wir Calciumhydroxid (Ca(OH)2), das im Laufe der Zeit mit atmosphärischem Kohlendioxid zu Calciumcarbonat reagiert.

Karbonate sind auf der Erdoberfläche sehr verbreitet, ebenso wie Mineralien. Ihre Kristallgitter können sich auf zwei Arten im Raum neu anordnen: die orthorhombische (wie das oben gezeigte Mineral Aragonit zusammen mit der Calciumcarbonat-Formel) und die rhomboedrisch oder trigonal wie Calcit (ein anderes Mineral, das aus Calciumcarbonat besteht).
Carbonate reagieren in Gegenwart von Säuren unter Freisetzung von CO2, die leicht durch ein Aufbrausen zu sehen ist.
Von Jennifer Fogaça
Abschluss in Chemie


