Ö Vinylchlorid es ist ein Kohlenwasserstoff giftige chlorierte und krebserregende Wirkung. Es ist bei Raumtemperatur ein farbloses Gas, leicht entzündlich und hitzeempfindlich.
Es ist das Monomer, das bei der Herstellung von Polyvinylchlorid, einer Substanz namens PVC, verwendet wird. Ö PVC ist (im Gegensatz zu seinem Monomer) ein hitzebeständiger Thermoplast, der in der Industrie zahlreiche Anwendungen findet Alltagsleben, wie zum Beispiel das Beschichten elektrischer Leitungen, den Bau von Rohren und verschiedene Arten von Verpackung.
Lesen Sie auch:Asbest – Naturfaser mit breiter industrieller Anwendung, aber äußerst giftig für den Menschen
Themen dieses Artikels
- 1 - Zusammenfassung über Vinylchlorid
- 2 - Eigenschaften von Vinylchlorid
- 3 - Was ist Vinylchlorid?
- 4 – Eigenschaften von Vinylchlorid
- 5 - Wofür wird Vinylchlorid verwendet?
- 6 – Gewinnung von Vinylchlorid
-
7 – Vorsichtsmaßnahmen mit Vinylchlorid
- Vinylchlorid und Krebs
- 8 – Vorkommen von Vinylchlorid
- 9 – Geschichte von Vinylchlorid
Zusammenfassung zu Vinylchlorid
Vinylchlorid ist ein chlorierter Kohlenwasserstoff mit der Formel H2C=CHCl.
es ist ein Gas farblos, süßlich riechend und leicht entzündlich.
Vinylchlorid ist instabil Hitze, zersetzt sich.
Die Hauptanwendung von Vinylchlorid liegt in der Herstellung von Polyvinylchlorid (PVC).
PVC ist ein Thermoplast mit zahlreichen Anwendungen, wie etwa Rohrleitungen, Teilen, Beschichtungen, Verpackungen usw.
Vinylchlorid ist giftig und hat eine krebserregende Wirkung.
Eigenschaften von Vinylchlorid
Molekularformel: CH2CHCl (C2H3Cl).
Molekulare Masse: 62,498 g/mol.
Körperlicher Status: Gas (farblos und mit starkem Geruch).
Dichte: 0,91 g/ml.
Löslichkeit in Wasser: sehr schwer löslich (0,6 g in 100 ml Wasser, 20 °C).
Schmelztemperatur: -154°C.
Siedetemperatur: -13°C.
Hör jetzt nicht auf... Nach der Veröffentlichung gibt es noch mehr ;)
Was ist Vinylchlorid?
Vinylchlorid ist ein chlorierter Kohlenwasserstoff mit der Formel H2C=CHCl. Bei Raumtemperatur tritt es mit a auf Farbloses und leicht entzündliches Gas.
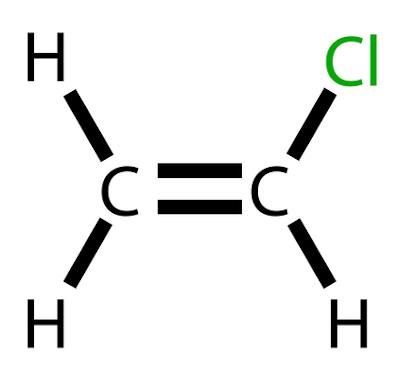
Vinylchlorid, auch Chlorethen oder Vinylchloridmonomer genannt, ist ein chemisches Produkt von großer Bedeutung in Industrie, mit besonderer Anwendung bei der Herstellung von Polymer Polyvinylchlorid, besser bekannt als PVC. Diese Verbindung belegt die Liste der 20 abgeleiteten Produkte Petroleum von größerer industrieller und wirtschaftlicher Bedeutung.
Lesen Sie auch:Benzopyren – krebserregender Kohlenwasserstoff, der in Zigarettenrauch und gegrilltem Fleisch vorkommt
Eigenschaften von Vinylchlorid
Vinylchlorid ist ein Farbloses Gas mit mildem, süßlichem Geruch. Es hat die Eigenschaft, leicht entflammbar zu sein.
Bei Einwirkung von Wärmequellen kann sich zersetzen und giftige Dämpfe freisetzen In Kohlendioxid, Kohlenmonoxid, Chlorwasserstoff und Phosgen. Da es sich um eine organische Verbindung handelt, ist seine Löslichkeit in Wasser äußerst gering, dagegen ist es in Substanzen wie z Ethanol, Benzol und Tetrachlorkohlenstoff.
In Gegenwart von Feuchtigkeit wird Vinylchlorid ätzend und kann das Material angreifen Eisen und das Stahl. Es hat die Fähigkeit, durch eine exotherme Reaktion zu polymerisieren, wenn es Hitze in atmosphärischer Luft ausgesetzt wird. Aus dieser Eigenschaft ergeben sich viele ihrer industriellen Anwendungen.
Vinylchlorid erfordert Aufmerksamkeit, weil es ist giftig und krebserregend.
Wofür wird Vinylchlorid verwendet?
Vinylchlorid ist das Monomer, das zur Herstellung von PVC-Polymer verwendet wird (Polyvinylchlorid) und andere chlorierte Lösungsmittel.
PVC ist ein Thermoplast, der bei der Herstellung von Verpackungen, Schuhen, elektrischen Verbindungen und Kabeln verwendet wird. Rohre, Fenster, Schläuche und Blutentnahmebeutel, Kleidungsstücke und unzählige andere Artikel.

Ö PVC entsteht durch die Polymerisation von Vinylchlorid. Bei diesem chemischen Prozess addieren sich zahlreiche Vinylchloridmoleküle zu einer großen chemischen Struktur.
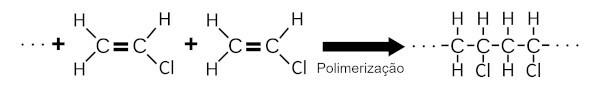
Ö PVC ist schwer entflammbar Aus diesem Grund wird es häufig zur Beschichtung von Drähten, Elektrokabeln und Wohnraumbeschichtungen verwendet.
Obwohl Vinylchlorid eine chemische Verbindung ist, die aufgrund ihrer Toxizität Aufmerksamkeit erfordert thermische Instabilität, sein PVC-Polymer ist sehr stabil gegenüber Wärmequellen, es ist ungiftig und kann gelagert werden mit Sicherheit.
Bis 1974 wurde Vinylchlorid in Aerosolen verwendet. Früher wurde es sogar als Inhalationsnarkotikum eingesetzt. Mit dem Wissen um die Toxizität dieser Verbindung wurden diese Anwendungen eingestellt.
Gewinnung von Vinylchlorid
Die Synthese von Vinylchlorid wird im industriellen Maßstab eingesetzt mit der Verbindung Ethylen bzw. Ethen initiiert (CH2=CH2) und kann auf zwei Wegen erfolgen.
Im ersten Schritt wird Ethylen durch Reaktion mit Chlorgas in 1,2-Dichlorethan umgewandelt. Anschließend wird durch Erhitzen des 1,2-Dichlorethans in Gegenwart eines Katalysators Vinylchlorid als Hauptprodukt erhalten Salzsäure als Nebenprodukt.
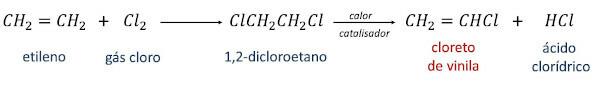
Beim zweiten Reaktionsweg, der sogenannten Oxichlorierung, erfolgt die Reaktion zwischen Ethylen, Salzsäure und Sauerstoff aus der Atmosphäre selbst, in Gegenwart von Wärme und einem Katalysator, wodurch Vinylchlorid und Wasser als Produkte entstehen.

Typischerweise ist ein Vinylchlorid-Produktionszentrum so gebaut, dass beide Herstellungsprozesse möglich sind. zitiert, so dass die bei der ersten Methode erzeugte Salzsäure als Reagens für die Durchführung der zweiten fungiert Route.
Vorsichtsmaßnahmen mit Vinylchlorid
Vinylchlorid ist eine giftige Verbindung. Da es sich um ein Gas handelt, Die Hauptkontaminationsform erfolgt durch Inhalation.Deshalb muss die Handhabung immer mit geeigneter Ausrüstung, wie z. B. Gasmasken, erfolgen.
Die Exposition gegenüber dieser Substanz beeinflusst die nervöses System peripher und zentral, was zu Schäden am führt Leber. A Kontinuierliche Belichtung kann das Raynaud-Phänomen auslösenHierbei handelt es sich um eine Reihe von Symptomen, zu denen Gelenk- und Muskelschmerzen sowie Hautveränderungen gehören, die zu einem vollständigen Verlust der Hautelastizität führen und sogar die Haut beeinträchtigen können Organe innere Organe und Blutgefäße.
Weitere Auswirkungen sind Euphorie, Orientierungslosigkeit, Fehlgeburten und Geburtsfehler. Auch Verletzungen des Augengewebes werden erfasst.
Die Symptome hängen von der Höhe der Substanzexposition ab und reichen von Schwindel, Übelkeit, Sehstörungen, Kopfschmerzen und Ataxie bei akuter Exposition (von 1000 bis 1000). 8000 ppm Vinylchlorid in der Luft), bei Exposition gegenüber Werten über 12000 zu narkotischer Wirkung, Herzrhythmusstörungen und tödlichem Atemversagen ppm.
Vinylchlorid und Krebs
Ö Vinylchlorid ist ein krebserregender Stoff, verbunden mit einem hohen Risiko, an Leberkrebs zu erkranken, was zum Auftreten von Leberkrebs beitragen kann Hirntumor und Lunge sowie Krebs des Lymphsystems.
Lesen Sie auch:Ammoniumnitrat – eine in der Landwirtschaft verwendete Verbindung, die Explosionen verursachen kann
Vorkommen von Vinylchlorid
das Vinylchlorid entsteht spontan in der Umwelt durch die Zersetzung einiger enthaltender Verbindungen Chlordurch die Wirkung von Mikroorganismen. Daher kann es insbesondere in angrenzenden Regionen als Luft- und Wasserverunreinigung angesehen werden Deponien.
Das größte Vorkommen von Vinylchlorid erfolgt jedoch, wie bereits erwähnt, auf synthetischen Wegen, die mit der chemischen Industrie in Zusammenhang stehen.
Geschichte von Vinylchlorid
Vinylchlorid war 1835 entdeckt vom deutschen Chemiker Justus von Liebig bei der Reaktion von Dichlorethan mit Kaliumhydroxid in einer alkoholischen Umgebung.
Später, im Jahr 1872, beobachtete der Chemiker Eugen Baumann zum ersten Mal die Polymerisation von Vinylchlorid, wodurch PVC entstand, nachdem er versehentlich einen Behälter mit der Substanz der Sonne ausgesetzt hatte.
Im Jahr 1926 entdeckte der amerikanische Erfinder Waldo Semon chemische Zusätze, die PVC mehr Elastizität und Formbarkeit verliehen und damit die Anwendungsmöglichkeiten dieses Stoffes erweiterten. Um 1950 begann der industrielle Einsatz von PVC. Derzeit ist PVC einer der am häufigsten verwendeten Thermoplaste weltweit.
Von Ana Luiza Lorenzen Lima
Chemielehrer
Haben Sie schon einmal vom chemischen Element Chlor gehört? Klicken Sie hier und erfahren Sie mehr über seine Eigenschaften, Eigenschaften, Beschaffung, Anwendungen und Geschichte.
Kennen Sie die chemische Zusammensetzung, Produktionsquellen und Anwendungen vieler organischer Verbindungen, wie unter anderem Aceton, Alkohol, Ether.
Erfahren Sie mehr über die Eigenschaften, Typen, Nomenklatur und wo Kohlenwasserstoffe vorkommen.
Lernen Sie die chemische Beschaffenheit von PVC-Polymer (Polyvinylchlorid) kennen, das häufig bei der Herstellung von Rohren und Kunstledermaterialien verwendet wird.


