Zum Sauerstofffunktion sind eine Gruppe von organische Verbindungen an deren Kohlenstoffkette Sauerstoffatome hängen. Sind sie:
Alkohol;
Keton;
Aldehyd;
Carbonsäure;
Ester;
Äther.
Lesen Sie auch:Kohlenwasserstoffe – Verbindungen aus Kohlenstoff und Wasserstoff
Zusammenfassung zur Sauerstofffunktion
Sauerstofffunktionen sind eine Gruppe von Verbindungen, die ein Sauerstoffatom enthalten. Sauerstoff direkt an die Kohlenstoffkette gebunden.
Die verschiedenen Sauerstofffunktionen zeichnen sich durch eine spezifische strukturelle Anordnung aus Atome, Funktionsgruppe genannt.
Die funktionellen Gruppen sind für die Eigenschaften jeder organischen Funktion verantwortlich.
Die Sauerstofffunktionen sind: Alkohol, Keton, Aldehyd, Carbonsäure, Ester und Ether.
Videolektion zur Sauerstofffunktion
Was sind die Sauerstofffunktionen?
Mit Sauerstoff versorgte Körperfunktionen sind solche, die haben ein Sauerstoffatom, das an ein Sauerstoffatom gebunden ist Kohlenstoff der Kohlenstoffkette.
Die Sauerstofffunktionen sind:
Alkohol;
Keton;
Aldehyd;
Carbonsäure;
Ester;
Äther.
Die organischen Funktionen werden durch ihre Funktionsgruppe identifiziert, Hierbei handelt es sich um eine strukturelle Anordnung von Atomen oder Bindungen, die für die charakteristischen Eigenschaften dieser Gruppe von Verbindungen verantwortlich ist.
Bedeutung von Sauerstofffunktionen
Das Vorhandensein von Sauerstoff funktioniert in organischen Verbindungen ist in der Lage, die Eigenschaften von Verbindungen zu verändern, im Vergleich zum jeweiligen Kohlenwasserstoff, mit gleicher Anzahl an Kohlenstoffen.
Sauerstofffunktionen zeichnen sich durch das Vorkommen von Hydroxyl-, Carbonyl- oder Carboxylgruppen aus. A Das Vorhandensein des Sauerstoffatoms verstärkt den polaren Charakter Verbindungen, wodurch sie hydrophiler werden, d. h. ihre Affinität zu erhöht Wasser.
Vorkommen von Sauerstofffunktionen ist auch für die Art verantwortlich intermolekulare Kraftzwischen Molekülen wirken. Die Art und Intensität intermolekularer Kräfte beeinflussen die Löslichkeit und die Schmelz- und Siedetemperaturen.
Die folgende Tabelle vergleicht einige Eigenschaften von drei Verbindungen, die die gleiche Anzahl an Kohlenstoffatomen haben, sich aber durch das Vorhandensein sauerstoffhaltiger funktioneller Gruppen unterscheiden.
Bio-Kompost | |||
Butan (C4H10) |
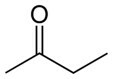
Butanon (C4H8Ö) |
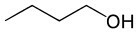
Butanol (C4H10Ö) |
|
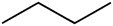 |
 |
 |
|
organische Funktion |
Kohlenwasserstoff |
Keton (Sauerstofffunktion) |
Alkohol (Sauerstofffunktion) |
Polarität |
apolar |
Polar |
Polar |
Schmelztemperatur |
-138,3°C |
-86°C |
-89°C |
Siedetemperatur |
-0,5°C |
80°C |
118°C |
Vorherrschende intermolekulare Kraft |
Induzierten Dipol |
permanenter Dipol |
Wasserstoffbrücken |
Alkohol
Die organische Funktion Alkohol hat eine Hydroxylgruppe (-OH), die direkt an gesättigten Kohlenstoff gebunden ist, also das Kohlenstoffatom, das nur Einfachbindungen eingeht.
Funktionelle Gruppe von Alkoholen: R-OH (Hydroxyl).
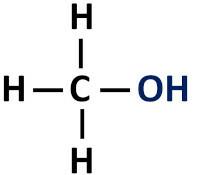
Alkohole sind klassifiziert nach der Art des Kohlenstoffs, an den die Hydroxylgruppe gebunden ist. Bei primären Alkoholen ist die Hydroxylgruppe an den primären Kohlenstoff gebunden. Bei sekundären Alkoholen ist die Hydroxylgruppe an einen sekundären Kohlenstoff gebunden, bei tertiären Alkoholen ist die -OH-Gruppe an tertiäre Kohlenstoffe gebunden.
Eine organische Verbindung, die nur eine Hydroxylgruppe hat, wird Monoalkohol genannt. Besitzt es zwei Hydroxylgruppen, spricht man von einem Dialkohol. Darüber hinaus werden die Moleküle Polyalkohole genannt.
A Nomenklatur für Alkohole folgt der Empfehlung von Iupac (International Union of Pure and Applied Chemistry) und betrachtet die Zusammensetzung der Namen chemischer Strukturen in drei Teilen:
Präfix – bezieht sich auf die Anzahl der Kohlenstoffe.
Infix – bezieht sich auf die Art der chemischen Bindung zwischen Kohlenstoffatomen.
Suffix – bezogen auf die Funktionsgruppe. Im Falle von Alkoholen lautet das verwendete Suffix -Hallo.
Siehe Beispiele:
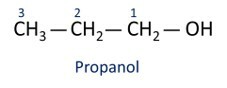
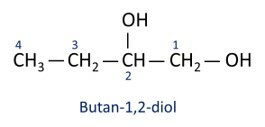
Ö Hauptalkohol ist Ethanl (CH3CH2OH), wird als Kraftstoff, in alkoholischen Getränken, als chemisches Lösungsmittel, Reinigungsmittel und Desinfektionsmittel verwendet.
Keton
Die organische Ketonfunktion entspricht der Carbonylfunktionelle Gruppe (C=O), die sich zwischen zwei Kohlenstoffatomen befindet der Kohlenstoffkette.
Funktionelle Gruppe von Ketonen: R1–(C=O)–R2.

Ketone sind nach der Anzahl der Carbonylgruppen klassifiziert:
Monoketone – haben eine einzelne Carbonylgruppe.
Diketone – haben zwei Carbonylgruppen.
Polytone – haben mehr als zwei Carbonylgruppen.
A Nomenklatur für Ketone folgt den Iupac-Regeln, jedoch mit einer unterschiedlichen Schreibweise des Suffixes. Ketone werden durch das Suffix identifiziert -auf einen.
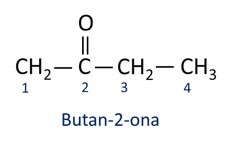
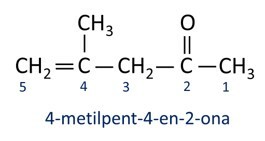
Im Allgemeinen finden Ketone Anwendung bei der Herstellung anderer Chemikalien und Pharmazeutika. In der Industrie werden Ketone als Lösungsmittel für Farben, Farben und Lacke verwendet. Eines der bekanntesten Ketone ist Propanon, das im Volksmund als Aceton bekannt ist. Zum Entfernen von Nagellack werden Acetonlösungen verwendet.
Lesen Sie auch:Amide – Verbindungen, an deren Carbonyl ein Stickstoff gebunden ist
Aldehyd
Die organische Aldehydfunktion ist gekennzeichnet durch das Vorhandensein der funktionellen Carbonylgruppe, dessen Kohlenstoffatom eine Wasserstoffbrücke aufweist.
Funktionelle Gruppe von Aldehyden: H–C=O (Formyl).
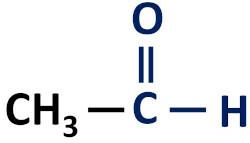
Aldehyde stehen immer am Ende von Kohlenstoffketten, da ihr Kohlenstoffatom an mindestens ein Wasserstoffatom gebunden sein muss.
A Nomenklatur für Aldehydverbindungen folgt den IUPAC-Regeln und unterscheidet sich durch das Suffix. Aldehyde werden durch das Suffix identifiziert -al.
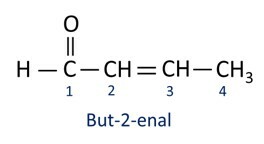
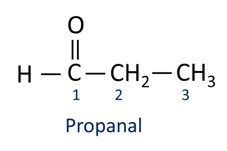
Aldehyde werden industriell bei der Herstellung von Parfüms und Parfüms verwendet Aroma, da sein Geruch und Geschmack je nach Länge der Kohlenstoffkette variieren. Aldehydverbindungen werden unter anderem auch bei der Herstellung von Reinigungsmitteln, Medikamenten und Polymeren verwendet. Als Konservierungsmittel können Aldehyde mit kurzer Kohlenstoffkette verwendet werden, wie zum Beispiel das berühmte Formalin, ein Aldehyd namens Methanal.

Carbonsäure
Die organische Carbonsäurefunktion wird durch das Vorhandensein der Carboxylfunktionsgruppe (-COOH) identifiziert.
Funktionelle Gruppe von Carbonsäuren: –(C=O)OH oder –COOH.

Verbindungen dieser organischen Funktion sind schwache Säuren, da sie leicht H-Ionen freisetzen+ in wässriger Lösung.
A Nomenklatur für Carbonsäuren folgt den Iupac-Regeln, jedoch erscheint der Begriff „Säure“ vor dem Präfix, das die Kohlenstoffzahl angibt, und das verwendete Suffix ist -oic.
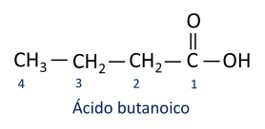
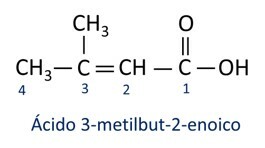
Ö Die häufigste Carbonsäure im Alltag ist die Essigsäure, im Essig enthaltener Stoff. Vitamin C, das in vielen Zitrusfrüchten reichlich vorhanden ist, ist ein organisches Molekül namens Ascorbinsäure.
Ester
Die organische Esterfunktion wird durch das Vorhandensein der funktionellen Carbonylgruppe identifiziert, dessen Kohlenstoffatom einen Sauerstoffliganden trägt.
Funktionelle Estergruppe: –R–(C=O)O–R'.
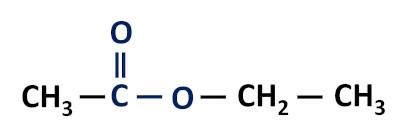
Die Ester sind Derivate von CarbonsäurenSie unterscheiden sich von diesen dadurch, dass sie anstelle des Wasserstoffatoms einen Alkylrest am Sauerstoffatom tragen.
Moleküle, die zur Esterfunktion gehören, entstehen durch die Reaktion zwischen einer Carbonsäure und einem Alkohol, einer Reaktion, die als bekannt ist Veresterung.
Die Regeln für Nomenklatur der Ester Nach der Definition von Iupac geht man davon aus, dass das Molekül aus zwei Teilen besteht:
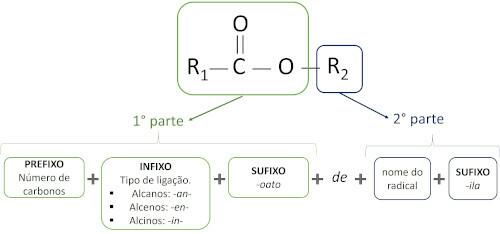
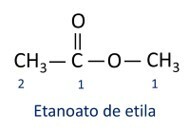
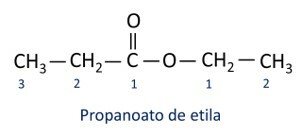
Das Hauptmerkmal von Estern ist ihr Fähigkeit, Geschmack und Aroma zu simulieren natürlicher Lebensmittel, entsprechend der Länge der Kohlenstoffketten (R1 und R2). Aus diesem Grund werden Ester häufig als Aromastoffe in der Lebensmittelindustrie, bei der Herstellung von Arzneimitteln, Parfüms und Kosmetika verwendet.
Äther
Die organische Ätherfunktion ist dadurch gekennzeichnet, dass sich zwischen zwei Kohlenstoffketten ein Sauerstoffatom befindet.
Funktionelle Gruppe der Ether: R–O–R.

Ether sind leicht entzündliche Stoffe mit einem charakteristischen und starken Geruch.
A offizielle Iupac-Nomenklatur für Ether folgt der Reihenfolge Präfix + Infix + Suffix. Allerdings erhält die Seite des Moleküls, die weniger Kohlenstoffe enthält, das Suffix -oxy, während die längere Kohlenstoffkette wie ein Kohlenwasserstoff benannt wird und das Suffix -o erhält.
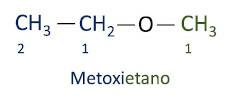
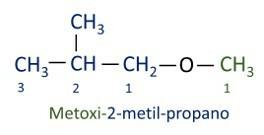
Die Äther sind werden als Lösungsmittel für Farben, Harze, Öle und Fette verwendet. Daher werden sie in verschiedenen industriellen und pharmazeutischen Prozessen eingesetzt. Äther wurde einst als Anästhetikum verwendet und wird heutzutage durch andere, sicherere Substanzen ersetzt.
Lesen Sie auch:Nitroverbindungen – Verbindungen, deren Molekül Nitrogruppen (NO2) enthält
Übungen zu Sauerstofffunktionen gelöst
Frage 1
(Uece) In der organischen Chemie wird eine funktionelle Gruppe als eine Molekülstruktur definiert, die Substanzen ein ähnliches chemisches Verhalten verleiht. Die Gesamtheit der Verbindungen mit derselben funktionellen Gruppe wird als organische Funktion bezeichnet. Markieren Sie die Option, die die Verbindung und die organische Funktion, zu der sie gehört, korrekt darstellt.

Auflösung:
Buchstabe C
Unter den Alternativen ist Element C die einzige, die die funktionelle Gruppe im Namen der chemischen Funktion korrekt ausdrückt. Die organische Esterfunktion wird durch die funktionelle Carbonylgruppe definiert, deren Kohlenstoffatom auch über einen Sauerstoffliganden verfügt.
In Punkt A wird die funktionelle Ethergruppe ausgedrückt.
In Punkt B wird die funktionelle Ketongruppe ausgedrückt.
In Punkt D wird die funktionelle Amidgruppe ausgedrückt. Amine Es ist Amide gehören zu den Stickstofffunktionen.
Frage 2
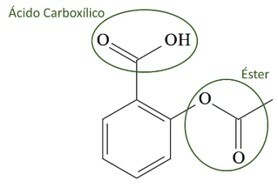
(UCS-RS) Im 5. Jahrhundert v. Chr. C., Hippokrates, griechischer Arzt, schrieb, dass ein Weidenrindenprodukt Schmerzen linderte und Fieber senkte. Dasselbe Produkt, ein Säurepulver, wird sogar in Texten der alten Zivilisationen des Nahen Ostens, Sumers, Ägyptens und Assyriens erwähnt. Die amerikanischen Ureinwohner nutzten es auch gegen Kopfschmerzen, Fieber, Rheuma und Zittern. Dieses Medikament ist eine Vorstufe von Aspirin, dessen chemische Struktur unten dargestellt ist.
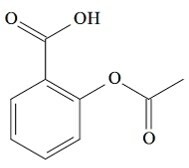
Die oben dargestellten organischen Funktionen in der Struktur von Aspirin sind:
a) Carbonsäure und Ester.
b) Alkohol und Äther.
c) Amin und Amid.
d) Amin und Ether.
e) Aminosäure und Alkohol.
Auflösung:
Buchstabe a
Von Ana Luiza Lorenzen Lima
Chemielehrer
Quelle: Brasilien-Schule - https://brasilescola.uol.com.br/quimica/funcoes-oxigenadas.htm
