DAS Rutherfordium ist ein synthetisches Element mit der Ordnungszahl 104 und gehört zur Gruppe 4 der Periodensystem, das das erste Mitglied der Transactinid-Reihe ist. Seine erste Entdeckung stammt aus dem Jahr 1964 in den berühmten Labors der Stadt Dubna. Wie andere Transactinide war auch der offizielle Name des Elements 104 in einen Konflikt zwischen den Sowjets und den Amerikanern verwickelt, in ein Stück Chemiegeschichte aus dem Kalten Krieg.
das Rutherfordium hat keine praktische Anwendung, da sein stabilstes Isotop etwa zweieinhalb Stunden hat Halbwertszeit. Untersuchungen in gasförmigen Systemen und Lösungen belegen jedoch seine chemische Ähnlichkeit mit den anderen Elementen der Gruppe 4, wie Zirkonium und Hafnium.
Lesen Sie auch: Seaborgium – synthetisches Element, benannt nach dem Wissenschaftler Glenn Seaborg
Zusammenfassung von Rutherfordium
- Es ist ein synthetisches chemisches Element, das sich in Gruppe 4 des Periodensystems befindet.
- Es wurde erstmals 1964 am Joint Institute for Nuclear Research in Dubna, Russland, synthetisiert.
- Es ist ein radioaktives ElementOma.
- Wie andere Transactinide leidet Rutherfordium an geringer Stabilität und es ist schwierig, beträchtliche Proben für Studien zu synthetisieren.
- Sein Name wurde erst 1997 offiziell, nach mehreren Jahren des Streits zwischen den Amerikanern und den Sowjets.
Rutherfordium-Eigenschaften
- Symbol: Rf
- Ordnungszahl: 104
- Atommasse: 267 Kubikmeter
- Elektronische Konfiguration: [Rn] 7s2 5f14 6d2
- stabilste Isotop: 267Rf (2,5 ± 1,5 Stunden Halbwertszeit)
- chemische Reihe: Gruppe 4, Transactinide, superschwere Elemente
Eigenschaften von Rutherfordium
Wie alle Transactinide, also Elemente direkt nach Laurence (Lr), ist Rutherfordium ist ein radioaktives Element. Sein stabilstes Isotop wurde 2004 nachgewiesen und seine Halbwertszeit (die Zeit, die für die Menge des Radioisotop um die Hälfte fallen) beträgt zweieinhalb Stunden, mit einer Fehlerspanne von mehr oder weniger eineinhalb Stunden.
Die große Schwierigkeit, die chemischen Eigenschaften von Rutherfordium und anderen festzustellen Transactinide ist im Allgemeinen die Tatsache, dass es eine niedrige Produktionsrate gibt, entweder in Menge oder in Geschwindigkeit. Bei diesen Elementen ist es zum Beispiel sehr üblich, nur ein einziges chemisch zu bewerten Atom, was in gewisser Weise rechnerische Anpassungen erfordert, da die meisten Gleichungen für Systeme mit mehr als einem Atom aufgestellt werden. Außerdem oft die Isotope haben sehr kurze Halbwertszeiten, was ein tiefergehendes Studium erschwert oder gar unmöglich macht.
Im konkreten Fall von Rf konnten Wissenschaftler bereits nachweisen, dass es sich in flüssiger Phase ähnlich verhält wie andere Elemente. leichtere Gruppe 4, Zirkonium und Hafnium, wie bei der Bildung von Fluoriden in Lösung mit anschließender Extraktion in Ionenaustauscherharzen. Dieses Verhalten trug dazu bei, das Vorhandensein von Rutherfordium in Gruppe 4 des Periodensystems zu festigen.
Lies auch: Neue chemische Elemente – die vier fehlenden Elemente in der 7. Periode
Rutherfordium erhalten
Transactinide benötigen für ihre Herstellung eine große Infrastruktur. Alle mit synthetisiert werden Teilchenbeschleuniger, bei dem ionische Spezies mit schweren Elementen kollidieren. Auch der Nachweis dieser Elemente ist nicht einfach und unkompliziert.
Wenn es gebildet wird, beginnt das radioaktive Element naturgemäß zu zerfallen und Emissionen wie Alpha- und Betateilchen zu zeigen. Oft ist es notwendig, die zu beurteilen radioaktiver Zerfall des entstandenen Atoms oder gar atomare Spezies identifizieren, die aus diesen Kernreaktionen wie in einem Puzzle entstehen können.
Hinzu kommt, dass die Halbwertszeiten von Transactinid-Isotopen oft kurz sind und im Bereich von liegen Sekunden, was es nur möglich macht, eine Menge im Bereich von wenigen Atomen oder sogar einem einzigen zu erhalten Atom.
Im Fall von Rf umfasste die erste Synthese, über die für dieses Element berichtet wurde, die Kollision von Plutoniumisotopen, Pu, mit Ionen des Neonisotops 22, Hm.
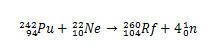
Es können jedoch andere Isotope von Rutherfordium hergestellt werden, indem die Arten, die kollidieren, modifiziert werden. Beispielsweise kann das Isotop 261 durch die Reaktion zwischen Sauerstoff-18 und Curium-248 hergestellt werden, wobei fünf Neutronen entstehen.
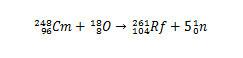
Hör es dir in unserem Podcast an: Wie funktioniert ein Teilchenbeschleuniger?
Vorsichtsmaßnahmen mit Rutherfordium
Da Rutherfordium nicht einmal in nennenswertem Umfang produziert werden kann, sind die mit diesem Element verbundenen Risiken mit dem verbunden Effekte von Strahlung. In einem kontrollierten Labor werden diese Risiken jedoch antizipiert und somit minimiert.
Geschichte von Rutherfordium

Alle Transactinide waren in den 1960er und 1970er Jahren an einem Wettlauf um ihre Entdeckung beteiligt. Diese Episode wird als die gemeldet War of Transfers, ein Stück der Kalter Krieg in der Geschichte der Chemie. Obwohl es so genannt wird, was darauf hindeutet, dass die Streitigkeiten über Elemente nach Fermium, einem Element, stattfanden Ordnungszahl 100, die direkt beteiligten Elemente waren 104 bis 109, die neu entdeckten Transactinide.
Im Falle von Rutherfordium begann der Streit 1964., als sowjetische Forscher am Joint Institute for Nuclear Research in der Stadt Dubna Russland, berichtete über die Entdeckung von Element 104 Isotop 260 durch Beschuss von Plutonium-242 mit Ionen neon-22. Aber die Dubna-Forscher legten nur einen Beweis vor, nämlich den Nachweis eines Isotops die spontan zerfallen ist, ohne ihre Masse und ihre Zeit eindeutig zu identifizieren Halbwertszeit. Infolgedessen wurde die Entdeckung mit Argwohn betrachtet.
Fünf Jahre später, 1969, führte ein Team amerikanischer Wissenschaftler das Lawrence Berkeley National Laboratory in Berkeley, Kalifornien, durch Albert Ghiorso, sagte, er habe ausreichende Beweise für die Entdeckung des Isotops 257 von Element 104 geliefert, indem er mit Californium-249 kollidierte Kohlenstoff-12. Dieselben Wissenschaftler waren später in der Lage, das Isotop 259 des Elements 104 herzustellen. 1973 bestätigten Wissenschaftler des Oak Ridge National Laboratory dies unabhängig voneinander Ordnungszahl 104 für das in Berkeley produzierte Isotop der Masse 257.
Die folgenden Jahre waren von großen Auseinandersetzungen zwischen den Wissenschaftlern beider Länder geprägt, bis 1985 der für Reine und Angewandte Chemie (IUPAC) und die Internationale Union für Reine und Angewandte Physik (IUAP) bilden a gemischte Kommission aus neun Wissenschaftlern, genannt Transfers Working Group (Transfermium-Arbeitsgruppe oder TWG). Die TWG wurde gegründet, um zu entscheiden, wer tatsächlich für die Entdeckungen der Elemente von 101 bis 112 verantwortlich war.
Trotzdem waren die Entscheidungen der TWG nicht immer unumstritten. Im Fall von Element 104 entschied die Arbeitsgruppe, dass die Die Anerkennung sollte zwischen sowjetischen und amerikanischen Wissenschaftlern geteilt werden, etwas, das die Berkeley-Wissenschaftler überhaupt nicht mochten.
1991 behaupteten Ghiorso und Seaborg vom Berkeley-Team sogar, dass die Identifizierung von Element 104 durch die Dubna-Wissenschaftler erfolgte eindeutig falsch und leugnete an einem Punkt die Gültigkeit der Schlussfolgerungen von TWG, da sie sie als Bärendienst für die Gemeinschaft betrachteten wissenschaftlich.
Kein Wunder, drin In den frühen 1990er Jahren waren die Namen für die neuen Elemente noch kein Konsens.. Es gab dann Verhandlungen zwischen deutschen, russischen und amerikanischen Wissenschaftlern, die sich als frustrierend herausstellten. Dort schlug die deutsche Laborgesellschaft für Schwerionenforschung (GSI) 1992 Namen für die Elemente 102 bis 109 vor, wobei Meitnerium für Element 104 eingesetzt wurde.
Trotzdem wurde die Liste trotz Lob von den beteiligten Wissenschaftlern nicht akzeptiert. Die Entscheidung könnte 1994 während der Konferenz der Iupac Inorganic Compound Nomenclature Commission (CNIC) getroffen werden. Darin wurde der Name Dubnium für das Element 104 gewählt, die American Chemical Society übernahm jedoch im selben Jahr den Namen Rutherfordium für das Element 104. Element 104, in einem Moment der Diskreditierung seitens der Amerikaner, die kamen, um die Autorität der IUPAC in Frage zu stellen, um neue zu formalisieren Namen.
erst 1997, auf der IUPAC-Generalkonferenz in Genf, ist das Element 104 wurde schließlich offiziell als Rutherfordium bezeichnet, nachdem das ACS in der Nomenklatur anderer nahe gelegener Elemente nachgegeben hatte.
Auf Rutherfordium gelöste Aufgaben
Frage 1
Rutherfordium ist ein synthetisches Element und eine der Hauptschwierigkeiten bei seiner Untersuchung ist die Tatsache, dass es nicht möglich ist, große Mengen davon zu synthetisieren.
Unter den möglichen Faktoren, die zu dieser Schwierigkeit beitragen, können wir Folgendes angeben:
(A) Rutherfordium hat Isotope mit langer Halbwertszeit in der Größenordnung von Millionen von Jahren.
(B) Rutherfordium zerfällt spontan und sehr schnell, was den Nachweis seiner makroskopischen Mengen verhindert.
(C) Es gibt keine Technologien, die in der Lage sind, Rutherfordium zu synthetisieren, da ihre Daten streng theoretisch und ohne wissenschaftliche Grundlage sind.
(D) Die Gesetze der Chemie besagen, dass es unmöglich ist, Elemente zu synthetisieren, deren Ordnungszahl die von Lawrence, 103, übersteigt.
(E) Während der Synthese von Rutherfordium werden leichtere Elemente seiner Gruppe chemisch priorisiert.
Antwort: Buchstabe b
Transactinid-Elemente wie Rf sind radioaktiv und zerfallen spontan mit hoher Geschwindigkeit, da ihre Halbwertszeit kurz ist. Somit sind am Ende des Experiments nur noch wenige Atome der synthetischen Spezies übrig.
Frage 2
1964 behaupteten Forscher aus Dubna, das Isotop 260 von Rutherfordium (Z = 104) synthetisiert zu haben. Wie groß ist bei diesem Isotop die Anzahl der Neutronen?
(A) 104
(B) 260
(C) 151
(D) 156
(E) 161
Antwort: Buchstabe D
Die Zahl der Neutronen (n) kann unter Verwendung der Massenzahl (A) und der Ordnungszahl (Z) durch die folgende Gleichung berechnet werden:
A = Z + n
Einsetzend haben wir:
260 = 104 + n
n = 260 - 104
n = 156
Bildnachweis
[1] Rosen-Abbas / Shutterstock
Von Stefano Araújo Novais
Chemielehrer
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/rutherfordio-rf.htm

