Polymerisation ist der Name des chemischen Prozesses, der durch die Kombination kleinerer Moleküle, den Monomeren, zur Bildung von Makromolekülen (großen Molekülen), den Polymeren, führt.
die Reaktion von Polymerisation es kommt in der Natur sehr häufig vor, wie wir in Kohlenhydraten (wie Stärke) und Proteinen (wie Kasein in Milch) sehen können. Es kommt auch synthetisch vor, da die allermeisten Polymere, die der Mensch im täglichen Leben verwendet, künstlich hergestellt werden.
Das erste Polymer hergestellt aus Polymerisation synthetisch war Bakelit im Jahr 1909 vom belgischen Chemiker Leo Hendrik Baekeland.
Im Allgemeinen wird ein Monomer mit einem anderen (gleich oder verschieden) in einer Reaktion von Polymerisation, ist die Existenz einer freien Valenz (chemische Bindung, die ausgeführt werden soll) in beiden Monomeren erforderlich.
Diese Valenzen entstehen durch das Aufbrechen von Bindungen, durch den Einsatz von Katalysatoren (wie Nickel), äußere Bedingungen wie Licht und Wärme, oder durch das Phänomen der Resonanz in der Struktur (Elektronenverschiebung).
Bei der Bildung von Polypropylen (PP-Polymer), das beispielsweise in Haushaltsutensilien und Spielzeug verwendet wird, pi-link (π) in jedem Molekül wird wie folgt aufgeschlüsselt:
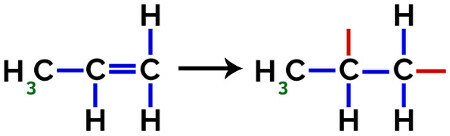
Bruch der pi-Bindung in Propylen
Somit kann sich jedes Propylenmonomer mit zwei anderen Propylenmonomeren verbinden und das Polymer PP oder Polypropylen bilden (das Präfix poly weist auf mehrere Monomereinheiten hin). Die häufigste Darstellungsweise eines Polymers ist das Monomer in Klammern und außen der Buchstabe n, der auf mehrere Monomere hinweist, wie wir beim PP-Polymer sehen können:
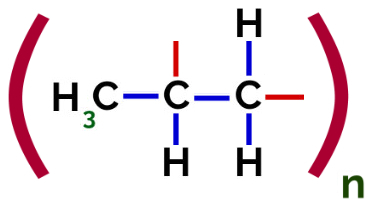
Darstellung von PP-Polymer
die Reaktion von Polymerisation kann auf unterschiedliche Weise erfolgen, wie wir unten sehen werden:
a) Reaktion von Additionspolymerisation
In diesem Polymerisation, kommt es immer zu einem Bruch einer pi-Bindung im Monomer, wodurch zwei freie Valenzen in der Struktur auftreten, wie bei der Bildung des Polyethylen, Polymer, das in pharmazeutischen Verpackungen weit verbreitet ist.
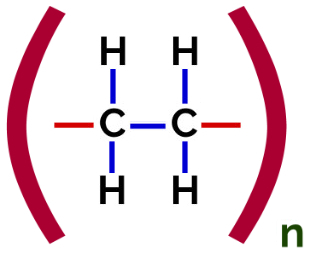
Strukturformel des Polyethylen-Additionspolymers
Bei Polymerisation von Polyethylen werden als Monomer Moleküle des Ethylens (Ethen) verwendet, die eine pi-Bindung zwischen den beiden Kohlenstoffatomen aufweisen. Wenn diese Bindung gebrochen wird, erscheinen zwei freie Valenzen, eine an jedem Kohlenstoffatom, das an der pi-Bindung beteiligt war. In jeder dieser Wertigkeiten vereinigen sich die Monomere genau, dh die Wertigkeit des einen ist mit der Wertigkeit des anderen verknüpft und so weiter.
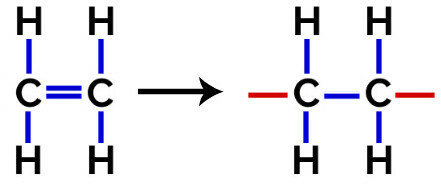
Polyethylenbildungsgleichung
b) Additionspolymerisationsreaktion 1.4
Bei dieser Polymerisation weisen die Monomere zwei alternierende Doppelbindungen auf (eine Pi und eine Sigma), was das Phänomen begünstigt Resonanz (Wechsel der Position der Pi-Elektronen der Pi-Bindung), wie bei der Bildung von synthetischem Gummi (Polybutadien)

Strukturformel von Polybutadien
Die Monomereinheit dieses Polymers ist Butadien, das zwei alternierende Doppelbindungen aufweist. Bei Resonanz hat die Struktur eine Doppelbindung zwischen den Kohlenstoffen 2 und 3 und zwei freie Valenzen an den Kohlenstoffen 1 und 4. Genau in diesen freien Valenzen der Kohlenstoffe 1 und 4 vereinigen sich die Monomere.

Butadien-Resonanz
c) Reaktion von Kondensationspolymerisation oder Beseitigung
Es ist eine Reaktion von Polymerisation bei denen zwingend zwei Monomere (gleich oder verschieden) gleichzeitig Atome oder Gruppen verlieren, wodurch in jedem von ihnen zwei freie Valenzen entstehen. Auf diese Weise erfolgt immer die Abspaltung von Wasserstoff aus einem Monomer, das sich dann mit einem Halogen (F, Cl, Br, I), OH, NH. verbindet2, oder zum CN des anderen Monomers.
Also, im Polymerisation durch Eliminierung entsteht immer Wasser, Halogensäure (HCl, HI, HF, HBr), Ammoniak (NH3) oder Blausäure (HCN) zusätzlich zum Polymer. Siehe zum Beispiel die Darstellung der Bildung von Polyester, einem Material, das als Gewebe verwendet wird:

Polyesterbildungsgleichung
Polyesterbildende Monomere sind p-Benzoldisäure und Ethan-1,2-diol. Das können wir dabei beobachten Polymerisation die Abspaltung von Wassermolekülen erfolgt, da die beiden Monomere zwei Hydroxyle aufweisen. Dabei verliert die Säure die beiden Hydroxyle und der Dialkohol nur den Wasserstoff aus seinen Hydroxylen:

Polyesterstruktur
Polyestermonomere werden durch den Sauerstoff im Alkohol und den Kohlenstoff in der Carbonsäure verbunden.
Von mir. Diogo Lopes Dias
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-polimerizacao.htm
