Unter den intermolekularen Kräften sind die induzierte dipolinduzierte Dipolkräfte sie sind die einzigen, die der niederländische Physiker Johannes Diederik Van der Waals (1837-1923) nicht untersucht hat. Sie wurden von dem deutschen Physiker Fritz Wolfgang London (1900-1954) aufgeklärt, daher werden diese Kräfte auch genannt Londoner Streitkräfte oder Londoner Dispersionskräfte. Ein anderer Name für diese Kräfte ist sofortiger dipolinduzierter Dipol.
Diese Art von Kraft tritt auf in unpolare Stoffe, wie unter anderem H2, O2, F2, Cl2, CO2, CH4 und C2H6. Und sie können auch zwischendurch auftreten Edelgasatome, wenn sie sich nähern, was eine Abstoßung zwischen ihren Elektrosphären verursacht. Auf diese Weise reichern sich die Elektronen aufgrund des negativen Ladungsmangels auf einer bestimmten Seite an, die negativ gepolt ist und auf der gegenüberliegenden Seite positiv.
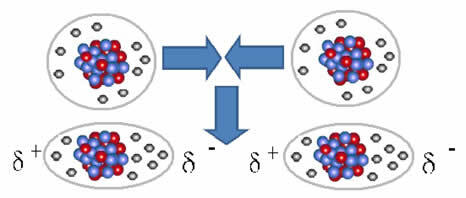
Unpolare Moleküle können von einem gasförmigen Zustand – in dem sie sehr weit voneinander entfernt sind und es keine Wechselwirkung gibt, da es keine Pole gibt – in einen flüssigen und festen Zustand übergehen. In diesen Aggregatzuständen sind sich die Moleküle näher und die elektronische Anziehung oder Abstoßung zwischen ihren Elektronen und Atomkerne können kurzzeitig zu einer Verformung ihrer Elektronenwolken führen, die positive und negative Pole entstehen vorübergehend.
Sofortige Dipole können eine Polarisation benachbarter Moleküle induzieren, was zu Anziehungskräften führt.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Diese Induktion kann auch erfolgen. zwischen verschiedenen Molekülen und allgemein diese Kräfte sind schwächer als die Dipol-Dipol- und Wasserstoffbindungsstärken. Daher werden Feststoffe mit dieser Wechselwirkungsstärke wie Trockeneis (Kohlendioxid - CO2) und Jod (I2), die sich im festen Zustand befinden, sublimiert (in den gasförmigen Zustand übergehen); weil die Energie, die benötigt wird, um ihre Interaktionen zu unterbrechen, gering ist.
Ein Beispiel für intermolekulare Kräfte zwischen polaren und unpolaren Molekülen tritt zwischen Sauerstoffgas (unpolar) und Wasser (polar) auf. Es stellt sich heraus, dass sich das negative Ende des Wassers dem O2 nähert, sich selbst abstößt und damit die Elektronenwolke des unpolaren Moleküls entfernt. Der Sauerstoff wird dann kurzzeitig polarisiert und beginnt mit dem Wasser zu interagieren und sich darin zu lösen.
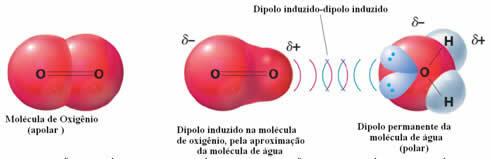
Da diese Kräfte schwach sind, ist die Löslichkeit dieses Gases in Wasser gering. Trotzdem ist seine Anwesenheit wichtig, um das Leben verschiedener Wasserorganismen zu erhalten.
Diese Wechselwirkungskraft tritt auch in der Natur auf und sorgt für eine Haftung zwischen den Pfoten der Geckos und der Oberfläche, auf der sie laufen. Deshalb können sie Wände und Decken begehen, ohne zu fallen oder zu kleben.
Von Jennifer Fogaça
Abschluss in Chemie
Brasilianisches Schulteam
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
FOGAÇA, Jennifer Rocha Vargas. "Induzierter Dipol-induzierter Dipol oder Londoner Dispersionskräfte"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/quimica/forcas-dipolo-induzido-dipolo-induzido-ou-dispersao-london.htm. Zugriff am 27. Juli 2021.