Anorganische Funktionen sind Gruppen anorganischer Verbindungen mit ähnlichen Eigenschaften.
Eine grundlegende Klassifizierung in Bezug auf chemische Verbindungen ist: organische Verbindungen sind solche, die Kohlenstoffatome enthalten, während organische Verbindungen Kohlenstoffatome enthalten. Anorganische Verbindungen sie werden von den anderen chemischen Elementen gebildet.
Es gibt Ausnahmen wie CO, CO2 und weiter2CO3, die trotz Kohlenstoff in der Strukturformel Eigenschaften von anorganischen Substanzen aufweisen.
Die vier wichtigsten anorganischen Funktionen sind: Säuren, Basen, Salze und Oxide.
Diese 4 Hauptfunktionen wurden von Arrhenius definiert, einem Chemiker, der Ionen in Säuren, Basen und Salzen identifizierte.
Säuren
Säuren sie sind kovalente Verbindungen, das heißt, sie teilen Elektronen in ihren Bindungen. Sie haben die Fähigkeit, in Wasser zu ionisieren und Ladungen zu bilden, wobei H. freigesetzt wird+ als einziges Kation.
Einstufung von Säuren
Säuren können nach der Menge an Wasserstoff klassifiziert werden, die in eine wässrige Lösung freigesetzt wird und ionisiert und mit Wasser reagiert, um das Hydroniumion zu bilden.
| Anzahl ionisierbarer Wasserstoffe |
|---|
|
Monosäuren: sie haben nur einen ionisierbaren Wasserstoff. Beispiele: HNO3, HCl und HCN |
|
Disäuren: haben zwei ionisierbare Wasserstoffatome. Beispiele: H2NUR4, H2S und H2MnO4 |
|
Trisäuren: haben drei ionisierbare Wasserstoffatome. Beispiele: H3STAUB4 und H3BO3 |
|
Tetrasäuren: haben vier ionisierbare Wasserstoffatome. Beispiele: H4P7Ö7 |
Die Stärke einer Säure wird durch den Ionisationsgrad gemessen. Je höher der Wert von stärker ist die Säure, denn:
| Ionisationsgrad |
|---|
|
stark: einen Ionisierungsgrad von mehr als 50 % aufweisen. |
|
mäßig: einen Ionisierungsgrad zwischen 5 % und 50 % haben. |
|
schwach: einen Ionisierungsgrad unter 5 % haben. |
Säuren können in ihrer Struktur das Element Sauerstoff enthalten oder nicht, also:
| Anwesenheit von Sauerstoff |
|---|
|
Hidracids: haben keine Sauerstoffatome. Beispiele: HCl, HBr und HCN. |
|
Sauerstoffsäuren: Das Element Sauerstoff ist in der Säurestruktur vorhanden. Beispiele: HClO, H2CO3 und HNO3. |
Säurenomenklatur
Die allgemeine Formel einer Säure kann beschrieben werden als HxDAS, wobei A das Anion darstellt, aus dem die Säure besteht, und die erzeugte Nomenklatur kann sein:
| Anionentermination | Säureterminierung |
|---|---|
|
Ethos Beispiel: Chlorid (Cl-) |
hydrisch Beispiel: Salzsäure (HCl) |
|
Handlung Beispiel: Chlorat |
ich Beispiel: Chlorsäure (HClO3) |
|
sehr Beispiel: Nitrit |
Knochen Beispiel: Salpetrige Säure (HNO2) |
Eigenschaften von Säuren
Die Hauptmerkmale von Säuren sind:
- Sie schmecken sauer.
- Sie führen elektrischen Strom, da es sich um Elektrolytlösungen handelt.
- Sie bilden Wasserstoffgas, wenn sie mit Metallen wie Magnesium und Zink reagieren.
- Bei der Reaktion mit Calciumcarbonat Kohlendioxid bilden.
- Sie verändern die Säure-Basen-Indikatoren auf eine bestimmte Farbe (blaues Lackmuspapier wird rot).
Hauptsäuren
Beispiele: Salzsäure (HCl), Schwefelsäure (H2NUR4), Essigsäure (CH3COOH), Kohlensäure (H2CO3) und Salpetersäure (HNO3).
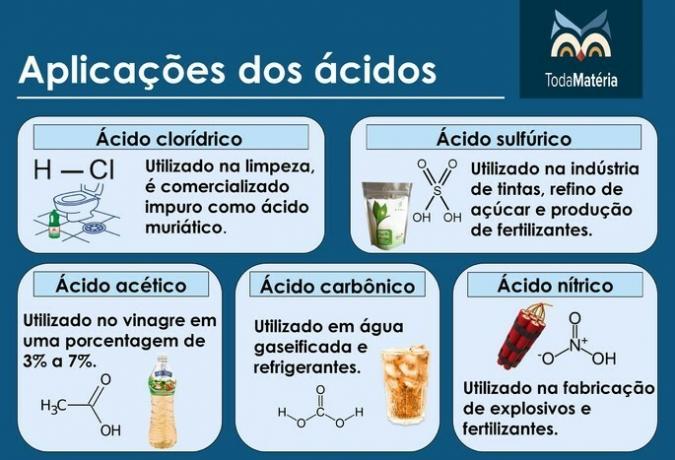
Obwohl Essigsäure eine Säure aus der organischen Chemie ist, ist es aufgrund ihrer Bedeutung wichtig, ihre Struktur zu kennen.
Basen
Basen sind ionische Verbindungen, die von Kationen, meist Metallen, gebildet werden, die in Wasser dissoziieren und das Hydroxid-Anion (OH-).
Basisklassifizierung
Basen können nach der Anzahl der in Lösung freigesetzten Hydroxyle klassifiziert werden.
| Anzahl der Hydroxyle |
|---|
|
Monobasen: sie haben nur ein Hydroxyl. Beispiele: NaOH, KOH und NH4Oh |
|
Dibases: haben zwei Hydroxylgruppen. Beispiele: Ca(OH)2, Fe(OH)2 und Mg(OH)2 |
|
Tribases: haben drei Hydroxylgruppen. Beispiele: Al(OH)3 und Fe(OH)3 |
|
Tetrabasen: haben vier Hydroxylgruppen. Beispiele: Sn(OH)4 und Pb(OH)4 |
Basen sind im Allgemeinen ionische Substanzen und die Stärke einer Base wird durch den Dissoziationsgrad gemessen.
Je höher der Wert von stärker ist die Basis, denn:
| Dissoziationsgrad |
|---|
|
stark: haben fast 100% Dissoziationsgrad. Beispiele:
|
|
schwach: einen Dissoziationsgrad von weniger als 5% haben. Beispiel: NH4OH und Zn(OH)2. |
| Löslichkeit in Wasser |
|---|
|
Löslich: Alkalimetall- und Ammoniumbasen. Beispiele: Ca(OH)2, Ba(OH)2 und NH4Oh. |
|
Schwach löslich: Erdalkalimetallbasen. Beispiele: Ca(OH)2 und Ba(OH)2. |
|
praktisch unlöslich: andere Basen. Beispiele: AgOH und Al(OH)3. |
Basisnomenklatur
Die allgemeine Formel einer Base kann beschrieben werden als , wobei B den positiven Rest darstellt, aus dem die Base besteht, und y die Ladung ist, die die Anzahl der Hydroxylgruppen bestimmt.
Die Nomenklatur für Fundamente mit fester Last ist gegeben durch:
| Basen mit fester Last | ||
|---|---|---|
Alkali Metalle |
Lithiumhydroxid |
LiOH |
| Erdalkalimetalle | Magnesiumhydroxid |
Mg(OH)2 |
Silber |
Silberhydroxid |
AgOH |
| Zink | Zinkhydroxid | Zn(OH)2 |
| Aluminium | Aluminiumhydroxid | Al(OH)3 |
Wenn die Basis eine variable Last hat, kann die Nomenklatur auf zwei Arten erfolgen:
| Böden mit variabler Belastung | |||
|---|---|---|---|
| Kupfer | Arsch+ | Kupferhydroxid I | CuOH |
| Kupfer(I)hydroxid | |||
| Arsch2+ | Kupferhydroxid II | Cu(OH)2 | |
| Kupferhydroxid | |||
| Eisen | Vertrauen2+ | Eisenhydroxid II | Fe(OH)2 |
| Eisenhydroxid | |||
| Vertrauen3+ | Eisenhydroxid III | Fe(OH)3 | |
| Eisenhydroxid |
Eigenschaften der Basen
- Die meisten Basen sind in Wasser unlöslich.
- Leiten Sie elektrischen Strom in wässriger Lösung.
- Sie sind rutschig.
- Sie reagieren mit Säure zu Salz und Wasser als Produkte.
- Sie verändern die Säure-Basen-Indikatoren auf eine bestimmte Farbe (rotes Lackmuspapier wird blau).
Hauptbasen
Basen werden häufig in Reinigungsmitteln und auch in Prozessen der chemischen Industrie verwendet.
Beispiele: Natriumhydroxid (NaOH), Magnesiumhydroxid (Mg (OH)2), Ammoniumhydroxid (NH4OH), Aluminiumhydroxid (Al(OH)3) und Calciumhydroxid (Ca(OH)2).

Salze
Salze sind ionische Verbindungen mit mindestens einem anderen Kation als H+ und ein anderes Anion als OH-.
Ein Salz kann in einer Neutralisationsreaktion erhalten werden, bei der es sich um die Reaktion zwischen einer Säure und einer Base handelt.
Die Reaktion von Salzsäure mit Natriumhydroxid erzeugt Natriumchlorid und Wasser.
Das gebildete Salz besteht aus dem Säureanion (Cl-) und durch das Basenkation (Na+).
Klassifizierung von Salzen
Im Folgenden haben wir die Hauptfamilien von Salzen, die nach Wasserlöslichkeit und pH-Änderung der Lösung wie folgt klassifiziert werden können:
| Wasserlöslichkeit der gängigsten Salze | |||
|---|---|---|---|
| Löslich | Nitrate | Ausnahmen: Silberacetat. |
|
| Chlorate | |||
Acetate |
|||
| Chloride | Ausnahmen: |
||
| Bromide | |||
| Jodide | |||
| Sulfate |
Ausnahmen: |
||
| Unlöslich | Sulfide |
Ausnahmen: Erdalkali und Ammonium. |
|
| Karbonate | Ausnahmen: Die von Alkalimetallen und Ammonium. |
||
| Phosphate |
| pH | |
|---|---|
| neutrale Salze |
In Wasser gelöst verändern sie den pH-Wert nicht. Beispiel: NaCl. |
| saure Salze |
Wenn sie in Wasser gelöst werden, liegt der pH-Wert der Lösung unter 7. Beispiel: NH4Kl. |
| basische Salze |
Wenn sie in Wasser gelöst werden, erhöhen sie den pH-Wert der Lösung über 7. Beispiel: CH3COONa. |
Zusätzlich zu den Salzfamilien, die wir zuvor gesehen haben, gibt es noch andere Arten von Salzen, wie in der folgenden Tabelle gezeigt.
| Andere Arten von Salzen | |
|---|---|
| Wasserstoffsalze | Beispiel: NaHCO3 |
| Hydroxysalze | Beispiel: Al(OH)2Cl |
| Doppelsalze | Beispiel: KNaSO4 |
| hydratisierte Salze | Beispiel: CuSO4. 5 Stunden2Ö |
| Komplexsalze | Beispiel: [Cu (NH3)4]NUR4 |
Nomenklatur der Salze
Im Allgemeinen folgt die Nomenklatur eines Salzes der folgenden Reihenfolge:
| Anionenname | kationsname | Name des Salzes |
|---|---|---|
|
Cl- Chlorid |
Vertrauen3+ Eisen III |
FeCl3 Eisenchlorid III |
|
Sulfat |
Beim+ Natrium |
Beim2NUR4 Natriumsulfat |
|
Nitrit |
K+ Kalium |
KNO2 Kaliumnitrit |
|
br- Bromid |
Hier2+ Kalzium |
CaBr2 Calciumbromid |
Eigenschaften von Salzen
- Sie sind ionische Verbindungen.
- Sie sind fest und kristallin.
- Sie leiden unter Sieden bei hohen Temperaturen.
- Leiten Sie elektrischen Strom in Lösung.
- Sie schmecken salzig.
Hauptsalze
Beispiele: Kaliumnitrat (KNO3), Natriumhypochlorit (NaClO), Natriumfluorid (NaF), Natriumcarbonat (Na2CO3) und Calciumsulfat (CaSO4).

Oxide
Oxide sind binäre Verbindungen (ionisch oder molekular), die aus zwei Elementen bestehen. Sie enthalten Sauerstoff in ihrer Zusammensetzung, der ihr elektronegativstes Element ist.
Die allgemeine Formel für ein Oxid ist , wobei C das Kation ist und seine Ladung y zu einem Index im Oxid wird, das die Verbindung bildet:
Klassifizierung von Oxiden
| Nach chemischen Bindungen | |
|---|---|
| ionisch |
Kombination von Sauerstoff mit Metallen. Beispiel: ZnO. |
| Molekular |
Kombination von Sauerstoff mit nichtmetallischen Elementen. Beispiel: Betriebssystem2. |
| Nach Eigenschaften | |
|---|---|
| Grundlagen |
In wässriger Lösung verändern sie den pH-Wert auf über 7. Beispiel: Ich lese2O (und andere Alkali- und Erdalkalimetalle). |
| Säuren |
In wässriger Lösung reagieren sie mit Wasser und bilden Säuren. Beispiele: CO2, NUR3 und nein2. |
| Neutrale |
Einige Oxide, die nicht mit Wasser reagieren. Beispiel: CO. |
| Peroxide |
In wässriger Lösung reagieren sie mit Wasser oder verdünnten Säuren und bilden Wasserstoffperoxid H2Ö2. Beispiel: Na2Ö2. |
| Amphoter |
Sie können sich wie Säuren oder Basen verhalten. Beispiel: ZnO. |
Nomenklatur der Oxide
Im Allgemeinen folgt die Nomenklatur eines Oxids der folgenden Reihenfolge:
| Name nach Art des Oxids type | |
|---|---|
| ionische Oxide |
Beispiele für Oxide mit fester Ladung: CaO - Calciumoxid Al2Ö3 - Aluminiumoxid |
|
Beispiele für Oxide mit variabler Ladung: FeO - Eisenoxid II Vertrauen2Ö3 - Eisenoxid III | |
| molekulare Oxide |
Beispiele: CO - Kohlenmonoxid Nein2Ö5 - Distickstoffpentoxid |
Oxideigenschaften
- Sie sind binäre Substanzen.
- Sie entstehen durch die Bindung von Sauerstoff mit anderen Elementen außer Fluor.
- Metalloxide bilden bei Reaktion mit Säuren Salz und Wasser.
- Nichtmetallische Oxide bilden bei der Reaktion mit Basen Salz und Wasser.
Hauptoxide
Beispiele: Calciumoxid (CaO), Manganoxid (MnO2), Zinnoxid (SnO2), Eisenoxid III (Fe2Ö3) und Aluminiumoxid (Al2CO3).

Übungen zur Aufnahmeprüfung
1. (UEMA/2015) NEIN2und das Betriebssystem2 sind Gase, die atmosphärische Verschmutzungen verursachen, die unter den verursachten Schäden zur Bildung von von saurem Regen, wenn diese Gase mit in Wolken vorhandenen Wasserpartikeln reagieren und dabei HNO3 und H2NUR4.
Diese Verbindungen verursachen, wenn sie von atmosphärischen Niederschlägen getragen werden, Störungen wie Trinkwasserverschmutzung, Korrosion von Fahrzeugen, historischen Denkmälern usw.
Die im Text genannten anorganischen Verbindungen entsprechen jeweils den Funktionen:
a) Salze und Oxide
b) Basen und Salze
c) Säuren und Basen
d) Basen und Oxide
e) Oxide und Säuren
Richtige Alternative: e) Oxide und Säuren.
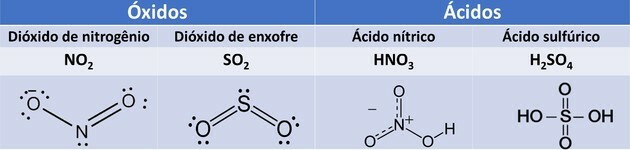
Oxide sind Verbindungen, die von Sauerstoff und anderen Elementen außer Fluor gebildet werden.
Säuren werden bei Kontakt mit Wasser ionisiert und produzieren das Hydronium-Ion. Für die fraglichen Säuren haben wir folgende Reaktionen:
die HNO3 es ist Monosäure, weil es nur einen ionisierbaren Wasserstoff enthält. das H2NUR4 es ist eine Disäure, weil es zwei ionisierbare Wasserstoffatome hat.
Die anderen in den Fragen vorhandenen anorganischen Funktionen entsprechen:
Basen: Hydroxylionen (OH-) mit Metallkationen ionisch gebunden.
Salze: Produkt der Neutralisationsreaktion zwischen einer Säure und einer Base.
Lerne mehr überchemische Funktionen.
2. (UNEMAT/2012) In unserem täglichen Leben verwenden wir verschiedene chemische Produkte wie Magnesiummilch, Essig, Kalkstein und Natronlauge.
Es ist richtig festzustellen, dass diese genannten Stoffe jeweils zu den chemischen Funktionen gehören:
a) Säure, Base, Salz und Base
b) Base, Salz, Säure und Base
c) Base, Säure, Salz und Base
d) Säure, Base, Base und Salz
e) Salz, Säure, Salz und Base
Richtige Alternative: c) Base, Säure, Salz und Base.
Magnesiummilch, Kalkstein und Natronlauge sind Beispiele für Verbindungen, die anorganische Funktionen in ihren Strukturen enthalten.
Essig ist eine organische Verbindung, die von einer schwachen Carbonsäure gebildet wird.
In der folgenden Tabelle können wir die Strukturen jedes einzelnen von ihnen und die chemischen Funktionen, die sie charakterisieren, beobachten.
| Produkt | Magnesiummilch | Essig | Kalkstein | Ätznatron |
|---|---|---|---|---|
| Chemischer Kompost | Magnesiumhydroxid | Essigsäure | Kalziumkarbonat | Natriumhydroxid |
| Formel | ||||
| chemische Funktion | Base | Carbonsäure | Salz- | Base |
Magnesiummilch ist eine Suspension von Magnesiumhydroxid zur Behandlung von Magensäure, da sie mit Salzsäure aus dem Magensaft reagiert.
Essig ist aufgrund seines Aromas und Geschmacks ein weit verbreitetes Gewürz, das hauptsächlich in der Lebensmittelzubereitung verwendet wird.
Kalkstein ist ein Sedimentgestein, dessen Haupterz Calcit ist, der große Mengen an Calciumcarbonat enthält.
Ätznatron ist der Handelsname für Natriumhydroxid, eine starke Base, die in vielen industriellen Prozessen und im Haushalt verwendet wird, um Rohre aufgrund einer Ansammlung von Ölen und Fetten zu reinigen.
3. (UDESC/2008) Bezüglich Salzsäure lässt sich sagen:
a) in wässriger Lösung ermöglicht es den Durchgang von elektrischem Strom
b) ist eine Disäure
c) ist eine schwache Säure
d) hat einen geringen Ionisierungsgrad
e) ist eine ionische Substanz
Richtige Alternative: a) in wässriger Lösung erlaubt es den Durchgang von elektrischem Strom.
Salzsäure ist eine Monosäure, da sie nur einen ionisierbaren Wasserstoff enthält.
Es ist eine molekulare Verbindung mit einem hohen Ionisierungsgrad und daher eine starke Säure, die beim Kontakt mit Wasser ihr Molekül wie folgt in Ionen zerlegt:
Wie Arrhenius in seinen Experimenten beobachtete, wandern die bei der Ionisation gebildeten positiven Ionen zum Minuspol, während die negativen Ionen zum Pluspol wandern.
Auf diese Weise fließt elektrischer Strom in die Lösung.
Weitere Probleme mit der kommentierten Lösung finden Sie unter: Übungen zu anorganischen Funktionen.