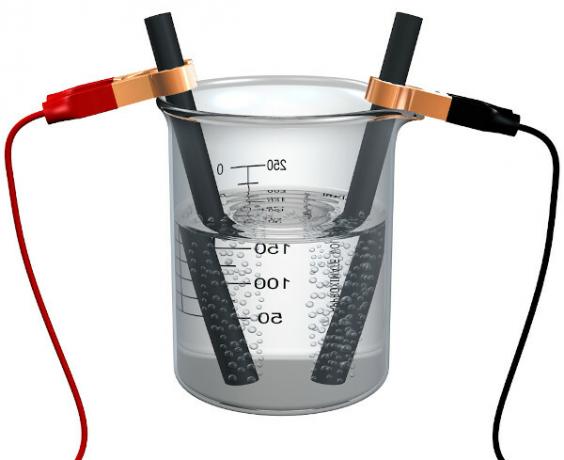
Einige Metalle kommen in der Natur nicht frei vor und müssen durch Laborverfahren gewonnen werden. Eine der effektivsten und wirtschaftlichen Methoden zur Reinigung von Metallen ist die Elektrolyse. Die Elektrolyse findet in Elektrolysezellen statt, wobei zwei Elektroden an die Klemmen eines Gleichstromgenerators angeschlossen sind.
Es ist bekannt, dass es in einer Elektrolysezelle eine Kathode und eine Anode gibt, siehe die jeweilige Definition:
Kathode: Es ist die negative Elektrode, die Kationen anzieht, und hier findet die Kationenreduktion statt.
Anode: Die positive Elektrode, die Anionen anzieht und daher hier das Anion oxidiert.
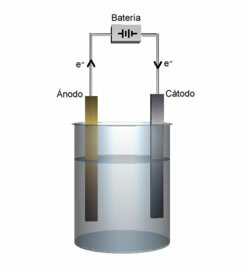
Anoden- und Kathodenvorführung.
Kupferreinigung
Kupfer, wie es in der Natur vorkommt, hat Verunreinigungen wie Silber, Eisen, Gold, Zink. Durch Elektrolyse ist es möglich, dieses Metall zu isolieren, um es in reiner Form zu erhalten, folgen Sie dem Verfahren:
- Unreines Kupfer dient als Anode und eine wässrige Lösung von Kupfersulfat als Elektrolyt, die sich in der Elektrolysezelle befindet. Die Kathode der Zelle ist Kupfer selbst in hoher Reinheit.
- Kupfer wird von der Anode zur Kathode übertragen, während die Verunreinigungen in Lösung bleiben. Kupfer im reinen Zustand reichert sich an der Kathode an und kann somit verwendet werden.
Von Líria Alves
Abschluss in Chemie
Brasilianisches Schulteam
Mehr sehen!
Elektrolysereaktionen
Elektrolyseprodukte
Elektrolyse - Physikochemische - Chemie - Brasilien Schule
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/purificacao-metais-atraves-eletrolise.htm