Ein Halogenid ist eine organische Verbindung mit mindestens einem Halogenatom. – also chemische Elemente der Familie 17 oder VII des Periodensystems (F, Cl, Br, I oder allgemein: X) – an eine von einem Kohlenwasserstoff abgeleitete Gruppe gebunden.
RX (wobei X = F, Cl, Br oder I)
Einige Halogenide sind unten aufgeführt:

Jod ist von allen am reaktivsten und Fluor am wenigsten, da die Bindungsenergie zwischen Halogen und Kohlenstoff von Jod zu Fluor zunimmt.
Ein weiterer Punkt ist, dass die Reaktivität auch in diesem Sinne zunimmt:

Diese Reaktivität tritt daher bei tertiären Kohlenstoffhalogeniden aufgrund des Charakters, den der an das organische Halogenid gebundene Kohlenstoff erworben hat, leichter auf:

Somit wird die Substituentengruppe, wie das OH, das den Alkohol bildet, stärker vom tertiären Kohlenstoff angezogen, der einen positiven Charakter hat (1+), und die Substitution ist einfacher.
Halogenide können Reaktionen eingehen, die es uns ermöglichen, praktisch alle anderen organischen Funktionen zu erhalten (Alkohol, Ether, Alkin, Cyanid oder Nitril, Amin ua). Dies ist jedoch in der Praxis nicht durchführbar, da Halogenide sehr teure Verbindungen sind.
Um beispielsweise einen Alkohol herzustellen, wird ein Halogenid mit einer starken Base, wie beispielsweise Natriumhydroxid, in einem wässrigen Medium umgesetzt. Sehen wir uns unten ein Beispiel an, in dem aus der alkalischen Hydrolyse von Ethylchlorid (Chlorethan) Ethanol entsteht:
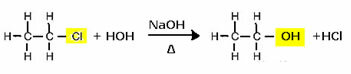
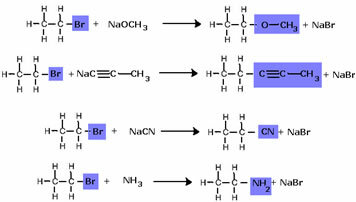
Beachten Sie, dass die Halogenidgruppe durch das OH, die funktionelle Alkoholgruppe, ersetzt wurde. Das gleiche Schema wird für die Bildung anderer Gruppen befolgt, wobei nur das Reagenz unterschieden wird:
Von Jennifer Fogaça
Abschluss in Chemie
Brasilianisches Schulteam
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/reacoes-substituicao-haletos-organicos.htm
