Volumetrische Analyse oder Volumetrie es ist ein Laborverfahren, bei dem wir ein bestimmtes Volumen an a. verwenden Lösung im Konzentration bekannt, die Konzentration einer anderen Lösung zu bestimmen. Das Volumen der Lösung bekannter Konzentration wird bestimmt, wenn sie vollständig mit der Lösung unbekannter Konzentration reagiert, dh die beteiligten Lösungen müssen miteinander reagieren.
Die am häufigsten verwendeten Instrumente zur Messung eines bestimmten Volumens sind:
- Pipette

Beispiel einer Pipette für die Volumenmessung
- Bürette

Die Bürette ist ein wichtiges volumetrisches Messgerät
Die Volumenmessung erfolgt durch Auswertung der Höhe des sogenannten Meniskus, das ist nichts anderes als der Oberflächenbereich der Flüssigkeit, der je nach Dicke des Behälters eine rechteckige oder gewölbte Form (Tropfenform) aufweist. Je breiter der Behälter, desto rechteckiger ist der Meniskus; je dünner der Behälter, desto konvexer wird er. Um den Meniskus zu beurteilen, muss das Auge genau in seiner Höhe sein und wir müssen den unteren Bereich als Referenz verwenden, wenn der Meniskus rechteckig ist, oder die Spitze, wenn er vorgewölbt ist. Sehen Sie sich eine Darstellung einer Bewertung an:
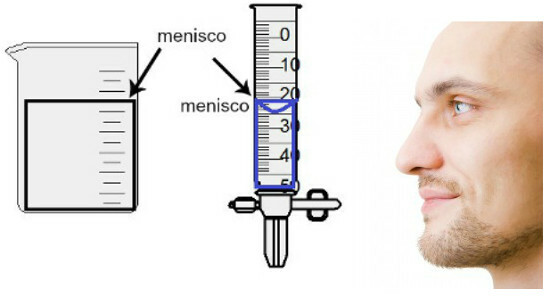
Um einen Meniskus zu beurteilen, ist es wichtig, dass Ihre Augen darauf gerichtet sind.
In der volumetrischen Analyse ist die Bürette das am häufigsten verwendete Gerät. Denn da es sich bei der Methode um chemische Reaktionen handelt und diese schnell verarbeitet werden können, ermöglicht die Bürette die Flüssigkeit wird an ihrer Spitze in Tropfen freigesetzt, wodurch wir verhindern können, dass die Flüssigkeit mehr austritt kontrolliert.
Eines der am häufigsten verwendeten Verfahren in der Volumetrie ist die Titration. Es ist eine volumetrische Analyse, die das Auftreten einer Reaktion zwischen einer Säure und einer Base oder umgekehrt beinhaltet. Die für die Realisierung erforderliche Ausrüstung ist im Bild unten dargestellt:
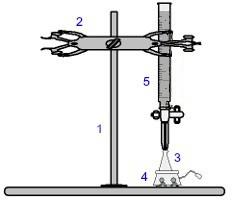
Darstellung der bei einer Titration verwendeten Ausrüstung equipment
Die Zahlen in Blau bedeuten:
1) Universelle Unterstützung;
2) Klaue (zum Halten der Bürette);
3) Erlenmeyer (erhält die Lösung unbekannter Konzentration);
4) Magnetrührer (zum Rühren der im Erlenmeyerkolben vorhandenen Lösung);
5) Bürette (erhält die Lösung bekannter Konzentration).
Ein Volumen der Lösung unbekannter Konzentration mit dem Phenolphthalein-Indikator wird in den Erlenmeyerkolben gegeben (die Lösung verfärbt sich sofort rosa). In die Bürette wird ein bestimmtes Volumen der Lösung bekannter Konzentration eingebracht. Anschließend wird die Säurelösung aus der Bürette direkt in die basische Lösung im Erlenmeyerkolben getropft. Dieser Tropfen dauert so lange, bis die Basenlösung farblos wird, an diesem Punkt nennen wir den Wendepunkt, der anzeigt, dass die gesamte in der Lösung vorhandene Base vollständig mit der Säure reagiert hat.
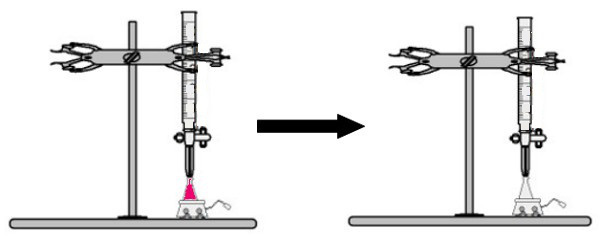
Am Wendepunkt ist die Lösung nicht mehr rosa und wird farblos
Überwachung: Wenn die Lösung unbekannter Konzentration sauer ist, wird sie beim Empfang des Phenolphthalein-Indikators farblos. Der Wendepunkt in der Titration wird also sein, wenn die saure Lösung rosa wird, wenn sie die basische Lösung aus der Bürette erhält.
Um schließlich die Konzentration der basischen Lösung zu bestimmen, verwenden Sie einfach die folgende Gleichung:
Ma.Va = Mb.Vb
Ma = Säuremolarität;
Va = Säurevolumen;
Mb = Basenmolarität;
Vb = Grundvolumen.
Folgen Sie nun einem Beispiel, wie die Berechnung einer Lösung mit unbekannter Molarität durchgeführt wird.
1.) 30 ml einer unbekannten Basenlösung wurden in einen Erlenmeyerkolben gegeben, um eine Titration zur Bestimmung der Konzentration (Molarität) durchzuführen. In die Bürette wurden 50 ml einer Säurelösung mit einer Konzentration von 0,2 mol/l gegeben. Nach dem Zutropfen der Säurelösung und bis die basische Lösung titriert war, wurde beobachtet, dass 20 ml der Säurelösung bei der Titration verwendet wurden. Bestimmen Sie die Molarität der verwendeten Basislösung.
Übungsdaten:
Vb = 30 ml
MB = ?
Ma = 0,2 mol/L
Va = 20 ml
Da die Molarität der Säure und ihr Volumen 0,2 mol/l bzw. 20 ml betragen und das Volumen der verwendeten Base 30 ml beträgt, verwenden Sie einfach die Titrationsformel:
Ma.Va = Mb.Vb
0.2.20 = Mb.30
4 = Mb.30
4 = MB
30
Mb = 0,133 mol/L
Von mir. Diogo Lopes Dias
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/analise-volumetrica.htm

