Änderungen des physikalischen Zustands hängen von einigen Faktoren ab, die mit Temperatur, Druck und der am Prozess beteiligten Energiemenge zusammenhängen.
In der Natur gibt es drei physikalische Aggregatzustände: fest, flüssig und gasförmig. Und physische Zustandsänderungen repräsentieren die fünf Prozesse der Änderung von einem Zustand in einen anderen.
Die Veränderungen sind: Kondensation oder Verflüssigung, Erstarrung, Verschmelzung, Verdampfung und Sublimation. Jede Art von Änderung hat einige Besonderheiten und hängt mit den Qualitäten der Materie zusammen.
Kondensation
Kondensation stellt den Übergang des Staates dar gasförmig bis flüssig.
Dies geschieht aufgrund der Abkühlung eines Gases, das dazu neigt, zu kondensieren und flüssig zu werden.
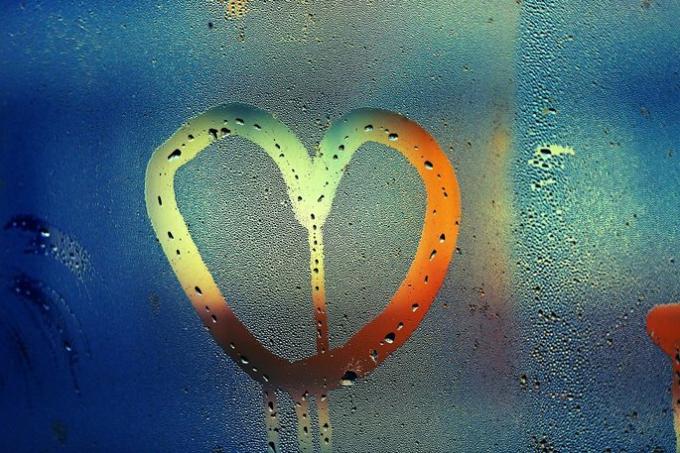
Erstarrung
Erstarrung ist der Durchgang von flüssig bis fest.
Ein Stoff in flüssigem Zustand neigt beim Abkühlen dazu, fest zu werden. Bei Wasser erfolgt die Erstarrung bei 0 °C

Verschmelzung
Die Fusion ist der Durchgang der fest zu flüssig.
Die Moleküle jedes Stoffes benötigen eine bestimmte Menge an Energie, um sich zu bewegen. Wenn weniger Energie vorhanden ist, neigen sie dazu, sich weniger zu bewegen und das Material neigt dazu, fest zu werden.
Wenn sie Energie von einer Wärmequelle (Heizung) erhalten, werden sie unruhiger und können ihren Zustand ändern.

Verdampfung
Verdampfung ist der Durchgang von flüssig bis gasförmig. Dies kann auf zwei Arten geschehen:
- Sieden: schnelle Erwärmung.
- Verdunstung: langsames Aufheizen.
Von 1 °C bis 100 °C ist es flüssig.

Sublimation
Sublimation ist der Durchgang von fest bis gasförmig Es ist von gasförmig bis fest (Resublimation).
Diese Art der Änderung erfolgt in Abhängigkeit von bestimmten Druck- und Temperaturbedingungen. Jedes Element hat seine Phasendiagramm, wo sich seine Fusions-, Verdampfungs- und Sublimationskurven befinden.

Physikalische Zustände von Wasser
Wasser ist in seinen drei physikalischen Zuständen leicht zu finden: fest, flüssig und gasförmig.
Jeder physikalische Zustand von Wasser ist je nach Temperatur- und Druckschwankungen möglich.
Bei Normaldruck (1 atm) schmilzt Wasser bei 0 °C und siedet bei 100 °C.
Wassermoleküle bei -1 °C sind in einem festen Zustand und bei 0 °C erfolgt die Änderung (Schmelzpunkt) von Eis bei 0 °C zu Wasser bei 0 °C.
Wenn es eine Temperatur von 100 °C erreicht, durchläuft es eine neue Zustandsänderung (Verdampfung), die vom flüssigen in den gasförmigen Zustand übergeht.
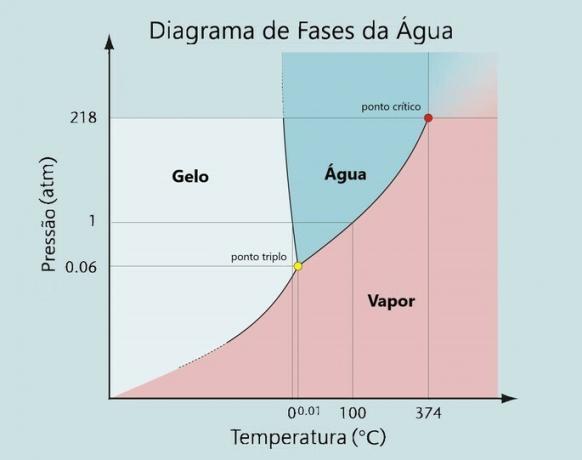
Wie aus seinem Phasendiagramm ersichtlich ist:
Um mehr über dieses Thema zu erfahren, lesen Sie auch:
- Physikalische Zustände von Wasser
- Physikalische Zustände der Materie
- Physikalische und chemische Umwandlungen
- Physikalische und chemische Phänomene