Allotropie ist ein Phänomen, das auftritt, wenn das gleiche chemische Element die Eigenschaft hat, mehr als eine einfache Substanz zu bilden.. Diese allotropen Sorten können sich durch die Anzahl der Atome des Elements, die in einem Molekül miteinander verbunden sind, oder durch die Anordnung der Atome im Kristallgitter unterscheiden.
Eines der Elemente, die allotrope Sorten aufweisen, ist Phosphor (P), das häufigste ist das weißer Phosphor es ist das roter Phosphor. Diese beiden Phosphorallotrope unterscheiden sich nicht durch ihre unterschiedliche räumliche Anordnung, da beide im Wesentlichen aus tetraedrischen Molekülen bestehen, sondern die Menge an Phosphoratomen ist bei jedem unterschiedlich.
Siehe die Zusammensetzung und die Hauptmerkmale von weißem und rotem Phosphor:
- Weißer Phosphor:
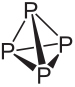
Die Summenformel von weißem Phosphor lautet P4, was bedeutet, dass seine Moleküle aus vier Phosphoratomen bestehen.

Diese Art von Leuchtstoff ist extrem reaktiv, hauptsächlich aufgrund der Spannung in den 60°-Winkeln zwischen seinen Bindungen. Es ist so reaktiv, dass es in Wasser gelagert werden muss, damit es nicht mit der Luft in Kontakt kommt und explodiert. Bei der Handhabung ist große Vorsicht geboten, da es beim Verschlucken zu schweren Hautverbrennungen und Vergiftungen führt (die Aufnahme von nur 0,1 g weißer Phosphor kann zum Tod führen).
Wie Sie unten sehen können, ist weißer Phosphor ein weißer wachsartiger Feststoff.

Weißer Phosphor in Wasser gelagert, um nicht mit Luft in Kontakt zu kommen*
Beim Erhitzen unter Luftabschluss verwandelt sich weißer Phosphor in roten Phosphor.
- roter Phosphor:
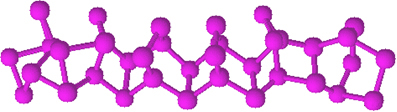
Roter Phosphor hat keine bestimmte Struktur, aber es gibt Hinweise darauf, dass es sich um Makromoleküle handelt, die durch die Bindung der erwähnten tetraedrischen Strukturen (P4), vertreten durch PNein.
Es ist viel weniger reaktiv als weißer Phosphor, kann sich jedoch beim Reiben entzünden. Deshalb wird es auf den Seitenflächen von Streichholzschachteln verwendet. Wenn wir den Zahnstocher an der Oberfläche der Schachtel reiben, entzündet sich das Streichholz und entzündet wiederum das leicht entzündliche Material am Zahnstocherkopf.
In einigen Ländern wird das Streichholz in Form von P auf den Kopf des Zahnstochers gelegt.4so3.
Roter Phosphor ist ein amorphes Pulver, dh es hat keine kristalline Struktur und hat eine dunkelrote Farbe, wie unten gezeigt:

Rotes Phosphorpulver.
* Bildurheberschaft liegt bei W. Oelen und sie sind zu finden hier.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/alotropia-fosforo.htm

