Die Konzepte reversibler und irreversibler Prozesse lassen sich mathematisch mit dem Konzept der Entropie beschreiben. Aber bevor wir zur Definition der Entropie kommen, kommen wir zu den Konzepten der reversiblen und irreversiblen Prozesse. wir nennen reversibler Prozess eine, in der das System spontan in die ursprüngliche Situation (oder den ursprünglichen Zustand) zurückkehren kann. Irreversibler Prozess ist jemand, dessen System nicht spontan in seinen ursprünglichen Zustand zurückkehren kann.
Da die Konzepte der Prozesstypen bereits erwähnt wurden, gehen wir zur Definition der Entropie über. DAS Entropie eines Systems (S) ist ein Maß für seinen Desorganisationsgrad. Je größer die Organisation, desto geringer die Entropie. Entropie ist ein Merkmal des thermodynamischen Zustands, ebenso wie die innere Energie, das Volumen und die Molzahl.
Wenn wir uns die Container in der obigen Abbildung ansehen, sehen wir, dass Container 1 a Entropie kleiner als das andere. Wenn wir den Behälter nehmen und schütteln, überprüfen wir, ob die „Kugeln“ verwechselt bzw. unorganisiert sind. Wenn wir Behälter 2 überprüfen, werden wir nach dem Schütteln feststellen, dass es für die Kugeln nicht möglich ist, spontan zu ihrer ursprünglichen Organisation zurückkehren, wenn wir weiter an der rütteln Container.
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
Bei reversiblen isothermen (dessen Temperatur immer gleich bleibt) reversiblen Prozessen definieren wir Entropie als das Verhältnis von Wärme (geliefert oder empfangen) zu Temperatur. Somit stellen wir die Entropie bei isothermen Prozessen wie folgt dar:
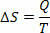
Im Internationalen Einheitensystem messen wir die Entropie in Joule/Kelvin. Basierend auf dem von uns beschriebenen Konzept zur Entropie können wir den zweiten Hauptsatz wie folgt formulieren:

Die Entropieänderung eines isolierten Systems ist immer positiv oder null. Die Gleichheit ΔS = 0 tritt ein, wenn Prozesse reversibel sind: Reversible Prozesse erhöhen die Entropie nicht. Isolierte Systeme, die weder Wärme aufnehmen noch an die Umgebung abgeben, können nur ihre Entropie erhöhen oder konstant halten.
Von Domitiano Marques
Abschluss in Physik
Brasilianisches Schulteam
Möchten Sie in einer schulischen oder wissenschaftlichen Arbeit auf diesen Text verweisen? Aussehen:
SILVA, Domitiano Correa Marques da. "Entropie und der zweite Hauptsatz"; Brasilien Schule. Verfügbar in: https://brasilescola.uol.com.br/fisica/entropia-segunda-lei.htm. Zugriff am 27. Juni 2021.



