Im Text "geometrisches Isomer oder cis-trans“ wurde gezeigt, wie geometrische räumliche Isomerie oder cis-trans. Kurz gesagt, das Isomer cis entspricht Verbindungen, deren gleiche Liganden an jedem Kohlenstoffatom in derselben Ebene liegen; schon im Isomer trans, sie sind auf gegenüberliegenden seiten.
Dies wird durch den Ursprung dieser Begriffe identifiziert, die aus dem Lateinischen stammen, wobei cis bedeutet "neben" und trans "über".
Diese Nomenklatur ist sehr nützlich, wenn zwei Kohlenstoffe jeweils nur zwei verschiedene Liganden haben. Diese Begriffe können jedoch mehrdeutig sein, wenn sie sich auf Alkene beziehen, deren Doppelbindungs-Kohlenstoffatome mehr als zwei verschiedene Liganden im Satz haben.
Betrachten Sie zum Beispiel die folgende Verbindung:

Beachten Sie, dass auf Kohlenstoff x der Ligand mit der niedrigsten Ordnungszahl ist CH3, und auf Kohlenstoff ja ist der h. Aber wenn wir sagen würden, dass diese Verbindung das Isomer ist cis, könnte sich folgende Frage stellen:
wie ist er so cis wenn die Verbindungsgruppen gleich sind (CH3) befinden sich auf gegenüberliegenden Seiten?Um diese Mehrdeutigkeit zu vermeiden, ist es daher in diesen Fällen richtiger, die Nomenklatur E-Z zu verwenden, wobei der Buchstabe E vom deutschen Wort stammt entgegen, was „Gegensätze“ bedeutet und Z kommt vom deutschen Wort zusammen, was „gemeinsam“ bedeutet. Diese Nomenklatur folgt der folgenden Regel:

Wenden wir diese Prioritätsregel auf 2-Chlorbu-2-en an, so haben wir die in Kohlenstoff x der Ligand mit der höchsten Ordnungszahl ist Cl, und auf Kohlenstoff ja ist die CH3. Somit haben wir die folgenden Isomere:
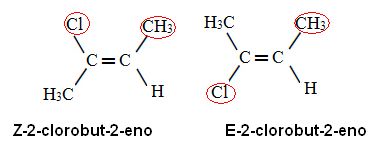
Im ersten Fall befinden sich die Liganden mit den höchsten Ordnungszahlen auf derselben Seite der Ebene (Z) und im zweiten auf gegenüberliegenden Seiten (E).
Dies tritt auch bei zyklischen Verbindungen auf. Es ist wichtig, sich daran zu erinnern, dass es nicht richtig ist, die Begriffe cis und Z sowie trans und E in Beziehung zu setzen, da es sich um unterschiedliche Namenssysteme handelt.
Von Jennifer Fogaça
Abschluss in Chemie
Quelle: Brasilien Schule - https://brasilescola.uol.com.br/quimica/isomeria-e-z-no-lugar-cis-trans.htm

