Elektrolyse ist ein physikalisch-chemischer Prozess, der elektrische Energie aus einer beliebigen Quelle (wie z Batterie oder Batterie), um das Auftreten einer chemischen Reaktion zu erzwingen, um einfache oder zusammengesetzte Stoffe zu erzeugen, die in der Natur nicht oder nicht in großen Mengen vorkommen.
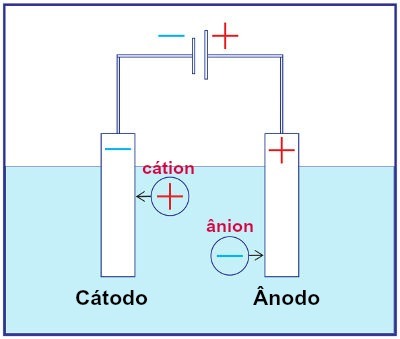
Darstellung der Montage einer beliebigen Elektrolyseanlage
Bei der Elektrolyse wird ein Kation an der Kathode reduziert und ein Anion an der Anode oxidiert. Dies geschieht durch elektrische Entladung, die von einer externen Quelle bereitgestellt wird. Somit haben wir bei der Elektrolyse eine nicht-spontane Oxidations- und Reduktionsreaktion.
Verstehen Sie nun die zwei Arten, auf denen die Elektrolyse abläuft:
Bei dieser Art der Elektrolyse verwenden wir a ionische Substanz im flüssigen Zustand in einem elektrolytischen Bottich. Wenn die ionische Substanz (XY) fusioniert, durchläuft sie den Prozess der Dissoziation, wie unten dargestellt:
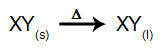

Dann, wenn die Stromquelle eingeschaltet wird, wird das Kation (X+) bewegt sich zur Kathode, und die Anionen (Y-) in Richtung Anode bewegen. Damit:
An der Kathode: die Kationen nehmen Elektronen auf (sie werden reduziert) und wandeln sich in eine stabile Substanz (X) um, ein Prozess, der durch die folgende Gleichung dargestellt wird:
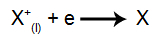
An der Anode: Anionen verlieren Elektronen (sie werden oxidiert) und werden zu einer stabilen Substanz (X), ein Prozess, der durch die folgende Gleichung dargestellt wird:

a) Beispiel einer magmatischen Elektrolyse
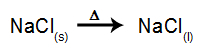
Als Beispiel sei nun die magmatische Elektrolyse des Natriumchlorid (NaCl). Wenn Natriumchlorid (NaCl) fusioniert, durchläuft es den Dissoziationsprozess, wie unten gezeigt:
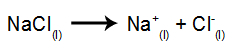
Dann, wenn die Stromquelle eingeschaltet wird, wird das Kation (Na+) bewegt sich zur Kathode, und die Anionen (Cl-) in Richtung Anode bewegen. Damit:
An der Kathode: die Kationen in+ sie erhalten Elektronen (sie werden reduziert) und werden zu einer stabilen Substanz (Na, einem festen Metall), ein Prozess, der durch die folgende Gleichung dargestellt wird:

An der Anode: die Cl-Anionen- sie verlieren Elektronen (sie werden oxidiert) und werden zu einer stabilen Substanz (Cl2, das gasförmig ist), Prozess, der durch die folgende Gleichung dargestellt wird:

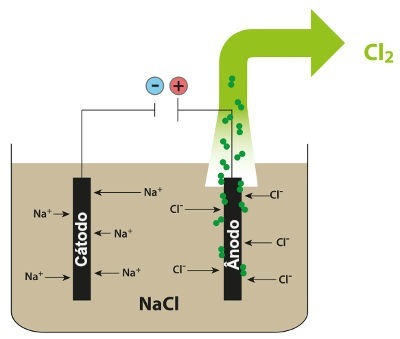
Schema der magmatischen Elektrolyse von NaCl
So haben wir bei der magmatischen Elektrolyse von Natriumchlorid die Bildung von metallischem Natrium (Na) und Chlorgas (Cl2).
Bei dieser Art der Elektrolyse verwenden wir eine in Wasser gelöste ionische Substanz im Elektrolyttank. Bevor wir die Elektrolyse durchführen, mischen wir also zuerst die Substanz (normalerweise ein Salz anorganisch) in Wasser, um seine Dissoziation (Freisetzung eines Kations und eines Anions) zu bewirken, wie gezeigt unten:
Hör jetzt nicht auf... Nach der Werbung kommt noch mehr ;)
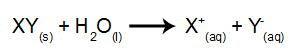
Der Unterschied zur magmatischen Elektrolyse besteht darin, dass wir neben den Ionen aus der Dissoziation auch Ionen aus der Selbstionisierung von Wasser haben. Wasser produziert bei seiner Selbstionisierung ein Hydronium-Kation (H+) und ein Hydroxid-Anion (OH-), wie in der folgenden Gleichung:
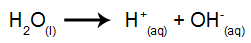
So haben wir in der Elektrolytwanne das Vorhandensein von zwei Kationen (eines aus der Substanz ionisch und eines aus Wasser) und zwei Anionen (eins aus der ionischen Substanz und das andere aus der Wasser).
Um zu wissen, welches Kation zur Kathode und welches Anion zur Anode wandert, ist es notwendig, die Entladungsreihenfolge von Kationen und Anionen zu kennen.
Für Kationen:
Au>Pt>Hg>Ag>Cu>Ni>Cd>Pb>Fe>Zn>Mn>Hydronium>IIIA-Familie> IIA-Familie > IA-Familie
für Anionen
Nicht mit Sauerstoff angereicherte Anionen und HSO4 > Hydroxid > Oxygenierte Anionen und F
Dann wird beim Einschalten der Stromquelle ein Kation (X+) bewegt sich zur Kathode, und eines der Anionen (Y-) bewegt sich in Richtung der Anode.
An der Kathode: die Kationen nehmen Elektronen auf (sie werden reduziert) und wandeln sich in eine stabile Substanz (X) um, ein Prozess, der durch die folgende Gleichung dargestellt wird:

An der Anode: Anionen verlieren Elektronen (sie werden oxidiert) und verwandeln sich in eine stabile Substanz (Y), ein Prozess, der durch die folgende Gleichung dargestellt wird:
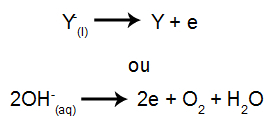
a) Beispiel einer wässrigen Elektrolyse
Als Beispiel verwenden wir die wässrige Elektrolyse von Natriumchlorid (NaCl). Wenn Natriumchlorid (NaCl) in Wasser gelöst wird, durchläuft es den Dissoziationsprozess, wie unten gezeigt:
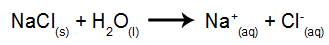
Neben der Dissoziation von NaCl haben wir die Selbstionisierung von Wasser:
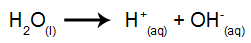
Wir haben also die H-Kationen+ und weiter+ und die OH-Anionen- und Cl-. Wenn dann die Stromquelle eingeschaltet wird, haben wir Folgendes:
an der Kathode: die H-Kationen+ Elektronen aufnehmen (reduziert) und zu einer stabilen Substanz (H2, das ist ein Gas). Dies liegt daran, dass Hydronium Entladungspriorität gegenüber den Elementen der IA-Familie (in diesem Fall Na) hat. Der Prozess wird durch die folgende Gleichung dargestellt:
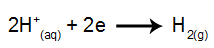
an der Anode: die Cl-Anionen- sie verlieren Elektronen (sie werden oxidiert) und werden zu einer stabilen Substanz (Cl2, das gasförmig ist). Dies liegt daran, dass die Cl- es ist ein nicht mit Sauerstoff angereichertes Anion und hat Entladepriorität gegenüber Hydroxid, ein Prozess, der durch die folgende Gleichung dargestellt wird:


Schema der wässrigen Elektrolyse von NaCl
So haben wir bei der wässrigen Elektrolyse von Natriumchlorid die Bildung von Wasserstoffgas (H2) und Chlorgas (Cl2).
Von mir. Diogo Lopes Dias
Chemie

Anwendungen der Elektrolyse, Galvanik, Vernickelung, Verchromung, Nickel, Chrom, Kathode, Natrium, Aluminium, Chlor, Ätznatron, Wasserstoffgas, magmatische Elektrolyse, wässrige Elektrolyse, Alkalimetalle, Erdalkali, Gas Chlor.