Kapaciteten, som forbindelserne har til at tiltrække elektriske ladninger, defineres som polaritet, som får en anden karakter afhængigt af den forbindelse, hvor den er til stede.
Med hensyn til den ioniske og kovalente binding gør sidstnævnte molekylet upolært. Molekylet, hvor den ioniske binding er ansvarlig for at holde atomer sammen, har polaritet.
Den dominerende binding mellem organiske forbindelser er kovalent, så de bliver for det meste ikke-polære forbindelser. De lange kulstofkæder, der findes i organiske stoffer, tillader dem ingen anden karakter end ikke-polaritet.
Forklaringen kommer af, at forbindelsen opstår mellem lige elementer (Ç-Ç), derfor har de samme elektronegativitetsskala. Se et eksempel:

ikke-polært molekyle
Butanen repræsenteret af strukturen ovenfor er en gas, bemærk at bindingsatomer er de samme (4 carbonatomer bundet sammen).
Men det betyder ikke, at enhver organisk forbindelse er upolær, tilstedeværelsen af andre atomer mellem carbonatomer giver molekylet en polær karakter. Se eksemplet:
Stop ikke nu... Der er mere efter reklamen;)
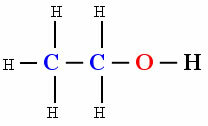
polært molekyle
Tilstedeværelsen af hydroxyl Åh (Oxygen forbundet med brint) fik molekylet af den organiske forbindelse Ethanol til at vise polaritet.
Butan bruges som gas til lightere, og etanol er den såkaldte almindelige alkohol.
Af Líria Alves
Uddannet i kemi
Brazil School Team
Se mere!
Egenskaber ved organiske forbindelser
Polaritet – Find ud af, hvorfor elektronegativitet påvirker ledningens polaritet.
Polaritet af ioniske og kovalente bindinger
Organisk kemi - Kemi - Brasilien skole
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
SOUZA, Líria Alves de. "Polaritet af organiske forbindelser"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/polaridade-dos-compostos-organicos.htm. Adgang til 28. juni 2021.

