DET enkel destillation er intet mere end en metode til adskillelse af blandinger, specielt brugt når vi har en homogen blanding dannet af et fast stof opløst i en væske, såsom natriumchlorid (NaCl) i vand.

Natriumchlorid kan opnås ved simpel destillation
Det er nødvendigt at forstå det i enkel destillation, der forekommer altid to grundlæggende fysiske tilstandstransformationer, den fordampning (passage fra væske til gas) og kondensation (passage fra damp til væske).
I laboratoriet for at udføre en enkel destillation, kræves følgende udstyr:
Bunsenbrænder eller varmeplade (1): udstyr, der bruges til opvarmning af blandingen
Destillationskolbe (2): beholder, hvor blandingen er pakket til opvarmning
Universalstøtte (3): udstyr, der bruges til at fastgøre kloen;
Klo (4): udstyr, der bruges til at holde destillationskolben
Termometer (5): udstyr, der bruges til at måle temperaturen under eksperimentet
Stopper (*): træmateriale til at lukke den øvre ende af destillationskolben;
Vandudløb (6): sti, gennem hvilket det opvarmede vand kommer ud;
Vandindløb (7): sti gennem hvilken koldt vand kommer ind;
Kondensator (8): udstyr, hvor der opstår kondens under eksperimentet
Erlenmeyer eller bægerglas (9): beholder, hvor den destillerede væske opsamles.
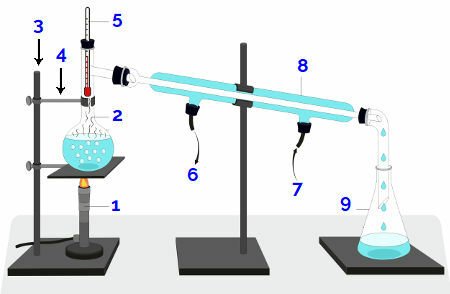
Skematisk gengivelse af en destilleri
Under udførelsen af en enkel destillation, har vi følgende begivenheder:
Først: destillationsudstyret er organiseret
Sekund: blandingen (f.eks. vand og natriumchlorid) tilsættes til destillationskolben
Tredje: opvarmningen af blandingen startes i destillationskolben ved hjælp af Bunsen-brænderen eller varmepladen;
Værelse: vandet begynder at fordampe inde i destillationskolben
Femte: vanddampen trænger nødvendigvis ind i destilleriet, da den øverste del af ballonen er lukket og igen bliver til væske;
Sjette: Den kondenserede væske opsamles derefter i bægerglasset eller erlenmeyer-kolben.

Repræsentation af den destillerede væske
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-destilacao-simples.htm

