DET oprindelse af Periodiske system opstod i det tidlige 19. århundrede, omkring 1829, da kemikere på det tidspunkt besluttede at foreslå måder at organisere kemiske grundstoffer kendt indtil da.
I begyndelsen af det 19. århundrede havde kemikere viden om flere egenskaber (massefylde, atommasse, reaktivitet, smeltepunkt, kogepunkt, fysisk tilstand) af tredive kemiske grundstoffer. Denne viden tjente som udgangspunkt for oprindelsen til det periodiske system.
I løbet af 200 år forsøgte flere kemikere at foreslå måder at organisere de kemiske grundstoffer på, dvs. Det periodiske system, vi kender i dag, havde faktisk forskellige oprindelser, som gennem historien mange forsøg var udført.
Mind Map: Oprindelsen til det periodiske system
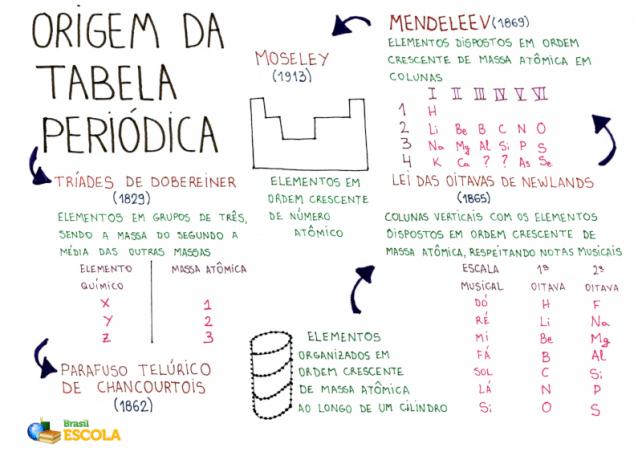
* For at downloade dette mind map, Klik her!
Her er nogle af de kemikere, der har udmærket sig i at forsøge at organisere elementerne i et bord.
Dobereiner triader

Illustration af Johann Wolfgang Dobereiner *
I år 1829 organiserede den tyske kemiker Johann Wolfgang Dobereiner det første periodiske system i historien. Det indeholdt de tredive kemiske grundstoffer, der var kendt indtil da, og blev af ham udnævnt til Dobereiner-triaderne.
DET Dobereiner periodisk tabel det blev kaldt en triade, fordi elementerne var organiseret i grupper på 3. Hver gruppe havde grundstoffer, der havde lignende kemiske egenskaber.
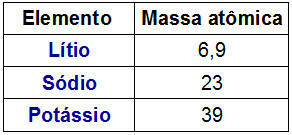
Repræsentation af en Dobereiner-triade
En interessant kendsgerning om Dobereiner triader er, at atommasse af det centrale element i triaden var nøjagtigt resultatet af det aritmetiske gennemsnit mellem atommasserne af de to andre elementer i triaden.

Tellurisk skrue af Alexandre de Chancourtois
I året 1862 var den franske geolog og mineralog Alexandre de Chancourtois han besluttede at foreslå en organisation af de kemiske grundstoffer, der var kendt på det tidspunkt, for at lette deres anvendelse i mineralogi. DET Chancourtois bord det blev kaldt tellurskrue.

Repræsentation af Chancourtois tellurisk skrue
Chancourtois fordelte de kemiske grundstoffer (mørke pletter på billedet) i stigende rækkefølge af atommassen langs et spiralbånd, der findes i en cylinder. Med denne organisation observerede Chancourtois, at elementer placeret på den samme lodrette linje havde lignende kemiske egenskaber.
Oktaveloven
Lov om oktaver var det navn, der blev foreslået af den engelske kemiker J.A.R. Newlands, i året 1865 til det periodiske system. Fordi Newlands også er musiker, satte han bordet op i overensstemmelse med de musikalske noter (do, there, re, mi, fa, sol, there, si).
Newlands organiserede de 61 kemiske grundstoffer, der var kendt på det tidspunkt, i stigende rækkefølge efter atommassen og placerede dem i lodrette søjler. Hver af de lodrette søjler havde syv elementer.
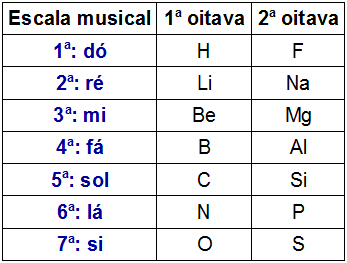
To oktav repræsentation af Newlands
Newlands observerede, at kemiske grundstoffer, der findes i den samme vandrette linje af forskellige oktaver, havde lignende kemiske egenskaber. Således havde det første element i en oktav lignende egenskaber som det første element i den anden oktav osv.
Mendeleevs periodiske system

Illustration af kemikeren Mendeleev **
MendeleevUnder sit arbejde med de kemiske grundstoffer havde han for vane at skrive egenskaberne for hver enkelt af dem ned på kort. På et tidspunkt, i året 1869, besluttede han at placere disse poletter i stigende rækkefølge af atommassen.
Lige efter at have arrangeret elementerne i stigende rækkefølge efter atommassen, holdt Mendeleev mønsteret, men anbragte elementerne i vandrette og lodrette søjler under hensyntagen til karakteristika og ligheder ved elementer.
Moseley periodiske system
I året 1913 var den engelske kemiker HenryMoseley, baseret på den af Mendeleev foreslåede tabel, samlede det periodiske system i de mønstre, vi kender i dag.
I modsætning til Mendeleev arrangerede Moseley elementerne i stigende rækkefølge af Atom nummer, holdt organisationen i vandrette og lodrette søjler, men placerede elementerne med de samme kemiske egenskaber i de samme lodrette søjler.
nuværende periodiske system
Efter 1913 gennemgik det periodiske system, der blev foreslået af Moseley, ingen større ændringer, faktisk gennemgik det nogle opdateringer, da nogle kemiske grundstoffer blev opdaget.
Sammenlignet med den aktuelle tabel viste Moseley-tabellen ikke for eksempel de kemiske grundstoffer med atomnumre mellem 110 og 118. Desuden var actinidserien placeret over lanthanidserien.
DET sidste ændring udført i det periodiske system var i 2016, da elementerne 113, 115, 117 og 118 officielt blev en del af det.
* Billedkredit: Yangchao/ shutterstock. Inc
** Billedkredit: Olga Popova/ shutterstock. Inc
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/origem-tabela-periodica.htm


