Nogle forbindelser behøver ikke at have otte elektroner i valensskallen for at opnå stabilitet, så de betragtes som undtagelser fra oktetreglen. Lær nu, hvorfor nogle elementer undgår forpligtelsen til at have en oktet af elektroner i den sidste skal.
Beryllium (Være)
Det er en undtagelse fra oktetreglen, fordi den er i stand til at danne forbindelser med to enkeltbindinger, så den stabiliseres med kun fire elektroner i valensskallen. 
Da brint (H) skal opgive to elektroner for at danne bindingen (H - Nå - H), deler Beryllium (Be) -atomet sine elektroner og opnår stabilitet.
Aluminium (Al)
Det er en undtagelse fra oktetreglen, fordi den opnår stabilitet med seks elektroner i valensskallen. Aluminiumatomet har en tendens til at donere sine elektroner og kan således danne tre enkeltbindinger med andre atomer: 
I dette tilfælde dannede aluminium (Al) tre bindinger med tre fluoratomer (F).
Bor (B)
Det danner molekylære stoffer med tre enkeltbindinger. 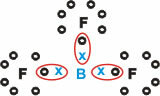
Bemærk, at Bor (B) har tendens til at donere sine elektroner til fluor (F) -atomer, som adlyder oktetreglen, hvilket kræver otte elektroner i valensskallen. Da bor opgiver sine elektroner, stabiliserer fluor sig med den dannede oktet.
Af Líria Alves
Uddannet i kemi
Brazil School Team
Se mere!
Oktetteori
Generel kemi - Kemi - Brasilien skole
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm
