DET opløselighed eller opløselighedskoefficient, det er en fysisk egenskab af stof, der altid bestemmes praktisk i laboratoriet. Det er relateret til den kapacitet, som et materiale kaldes opløst stof, gaver, der skal opløses af en anden, den opløsningsmiddel.
Med hensyn til opløselighed kan opløste stoffer klassificeres som følger:
Opløselige stoffer: dem, der opløses i opløsningsmidlet. Natriumchlorid (opløst stof) er for eksempel opløseligt i vand (opløsningsmiddel);
Let opløselig: dem, der har svært ved at opløse i opløsningsmidlet. Dette er tilfældet med calciumhydroxid [Ca (OH)2] (opløst stof) i vand;
Uopløselige: disse opløses ikke i opløsningsmidlet. Sand (opløst stof) er for eksempel uopløselig i vand.
DET opløselighed er meget forbundet med forberedelsen af løsninger (homogene blandinger), da det for at opnå en opløsning er væsentligt, at det anvendte opløste stof er opløseligt i opløsningsmidlet.
Faktorer, der påvirker opløselighed
Selv når det opløste stof er opløseligt i opløsningsmidlet, er der nogle faktorer, der kan påvirke opløsningsmidlets opløsningsevne. Er de:
a) Forholdet mellem mængden af opløst stof og opløsningsmiddel
Opløsningsmidlet har altid en grænse for opløst stof, det kan opløses. Hvis vi øger mængden af opløsningsmiddel, mens vi opretholder mængden af opløst stof, har opløsningsmidlet tendens til at opløse al den opløste opløsningsmiddel.
B) Temperatur
Temperatur er den eneste fysiske faktor, der er i stand til at ændre et opløsningsmiddels opløselighed i forhold til en given opløsningsmiddel. Denne ændring afhænger af opløsningsmidlets art, som vi vil se nedenfor:
endoterm opløst stof: er den, at det lykkes os at opløse en større masse, så længe opløsningsmidlet har en temperatur, der er højere end stuetemperatur. Jo varmere opløsningsmidlet, desto mere opløses det.
Eksempel: Det er muligt at opløse en større mængde malet kaffe, når vandet er varmt.
Eksoterm opløsningsmiddel: er den, at det lykkes os at opløse en større masse, så længe opløsningsmidlet har en temperatur, der er lavere end stuetemperatur. Jo koldere opløsningsmidlet er, desto mere opløses det.
Eksempel: Det er muligt at opløse en større mængde kuldioxid, når sodavand er koldt.
Måder til bestemmelse af opløselighed
Da opløseligheden er en egenskab, der bestemmes på en eksperimentel måde, har materialerne generelt fået deres opløselighed vurderet i de mest forskellige opløsningsmidler. Således kan vi få adgang til opløseligheden af et opløst stof i et bestemt opløsningsmiddel som følger:
a) Analyse af en tabel
Ofte kan den studerende støde på opløselighed fra fortolkningen af et bord. Se følgende eksempel:
Eksempel: (UEPG - tilpasset) Tabellen nedenfor viser opløseligheden af Li-salt2CO3 i 100 gram vand.

Tabellen viser masseværdierne i gram Li2CO3 som kan opløses i 100 gram vand, fra 0 OC til 50 OÇ. Vi kan se, at jo varmere vandet er, jo mindre Li2CO3 opløses. Derfor Li2CO3 det er en eksoterm opløsningsmiddel (den opløses mere, hvis vandet er koldt).
b) Analyse af en graf
Opløselighed kan vurderes ved at fortolke en graf. For at gøre dette skal du blot bestemme temperaturen, dreje den til kurven og derefter dreje kurven til y-aksen, hvilket er massen i gram opløst stof, der opløses.
Eksempel: (UFTM - tilpasset) Grafen viser opløselighedskurven for et AX-salt2.
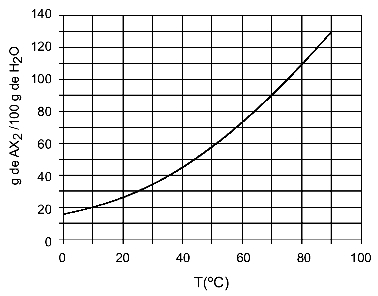
Grafen siger, at mængden af vand (opløsningsmiddel) på y-aksen er 100 gram. Til opløst AX2, vil vi bestemme mængden af vand ved følgende temperaturer:
30OÇ: Når vi tænder temperaturen 30OC til kurven og derefter kurven til y-aksen, vi har, at 100 gram vand ved denne temperatur kan opløse ca. 35 gram opløst AX2.
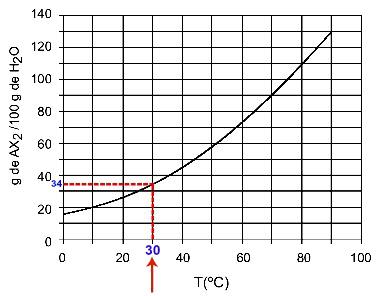
Bestemmelse af AX-opløselighed2 kl. 30OÇ
40OÇ: Når vi tænder temperaturen 40OC til kurven og derefter kurven til y-aksen, vi har, at ved denne temperatur kan de 100 gram vand opløse ca. 45 gram opløst AX2.
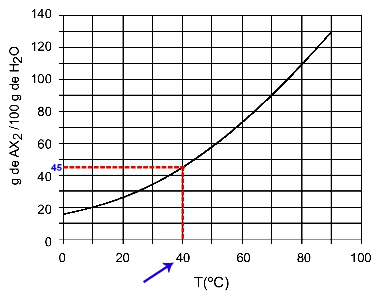
Bestemmelse af AX-opløselighed2 ved 40OÇ
Da den opløste mængde opløst stof er større med hver temperaturforøgelse, har vi, at AX2 det er en endoterm opløsningsmiddel.
c) tekstfortolkning
Se følgende eksempel:
Eksempel: (PUC-MG) Visse stoffer er i stand til at danne homogene blandinger med andre stoffer. Det stof, der er i den største mængde, kaldes et opløsningsmiddel, og det stof, der er i den mindste mængde, kaldes et opløst stof. Natriumchlorid (NaCl) danner en homogen opløsning med vand, hvor det er muligt at opløseliggøre ved 20 ° C 36 g NaCl i 100 g vand.
Teksten siger, at hvis vi har 100 gram vand (opløsningsmiddel) ved en temperatur på 20 OC, er det muligt at opløse op til 36 gram NaCl.
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm

