Nitrocompound er en organisk forbindelse afledt af den kemiske reaktion mellem salpetersyre (HNO)3) det er en alkan (åben mættet carbonhydrid) eller en aromatisk. Når salpetersyre reagerer med alkan eller aromatisk, forekommer en substitutionsreaktion, hvor syren mister en hydroxylgruppe (OH), og den organiske forbindelse mister et hydrogen:
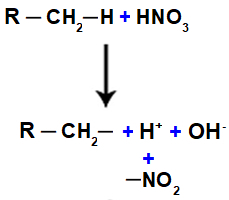
Dernæst har vi dannelsen af et vandmolekyle, der er resultatet af foreningen mellem OH og H, mens INGEN gruppe2 (som er tilbage fra syren) binder til alkanen eller aromaten og danner nitroforbindelse.
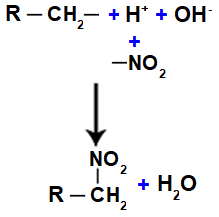
Repræsentation af dannelse af vand og nitrocompound
Således er det vigtigste strukturelle træk ved en nitroforbindelse er tilstedeværelsen af en eller flere nitrogrupper (VED2) bundet til en alkan eller en aromatisk.
ejendomme
Med respekt for ejendomme fysisk, kan vi fremhæve:
Generelt er de tyktflydende væsker ved stuetemperatur (med undtagelse af nitroforbindelser med lav molær masse, som er flydende væsker);
De har høje smelte- og kogepunkter;
De er tættere end vand;
Generelt er de uopløselige i vand med undtagelse af nitromethan og nitroethan;
Når de dannes af en alifatisk kæde, har de en behagelig aroma og er ikke giftige. Hvis de nu er dannet af en aromatisk kæde, er de giftige og har en ubehagelig aroma;
O type intermolekylær kraft der forener dets molekyler er permanent dipol, da de har polære egenskaber.
Med hensyn til kemiske egenskaber skal vi vide, at nitroforbindelser de er meget reaktive, dvs. de bruges i forskellige organiske reaktioner, såsom substitutionsreaktioner.
Den officielle nomenklaturregel, foreslået af IUPAC (International Union of Pure and Applied Chemistry), for nitroforbindelser é:
Nitro + præfiks + infix + o
Bemærk: Præfikset er relateret til antallet af carbonatomer til stede i nitroforbindelseskæden. Infixet er relateret til typen af bindinger, der findes mellem kulstoffer.
Eksempler:
Nomenklatur for en normalkædet nitroforbindelse

Oprindeligt er det interessant at nummerere strengen af nitroforbindelse (altid fra det kulstof, der er tættest på det kulstof, der har nitrogruppen):
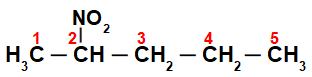
Ved at nummerere strengen på nitroforbindelse, vi har, at der er fem kulstofatomer (præfiks pent), kun enkeltbindinger mellem kulstofferne (infix an) og nitrogruppen på carbon 2. Navnet på denne struktur er 2-nitropentan.
Nomenklatur for en normalkædet nitroforbindelse
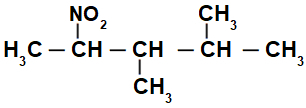
Strukturformel for en forgrenet nitroforbindelse
Oprindeligt er det interessant at nummerere strengen af nitroforbindelse (altid fra det kulstof, der er tættest på det kulstof, der har nitrogruppen), til den ende, der har det højeste antal kulhydrater til hovedkæden:
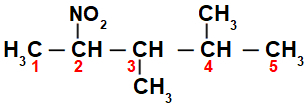
Ved at nummerere strengen på nitroforbindelse, vi har, at der er 5 kulstofatomer (præfiks pent), kun enkeltbindinger mellem kulstofferne (infiks an), to methylradikaler (på kulstoftal 3 og 4) og nitrogruppen på kulstof 2. Navnet på denne struktur er 3,4-dimethyl-2-nitropentan.
Anvendelser
Du nitroforbindelser, generelt kan de anvendes til fremstilling af pesticider, farvestoffer, anilin, baktericider, fungicider, additiver, opløsningsmidler; de fungerer også som sprængstoffer og i olieraffinering.
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-nitrocomposto.htm

