Forskydningsreaktioner, også kaldet substitutionsreaktionereller stadig fra enkel udveksling, er dem, der opstår, når et simpelt stof (dannet af et enkelt element) reagerer med et sammensat stof og "fortrænger" sidstnævnte til et nyt simpelt stof.
Generelt kan vi definere det som følger:
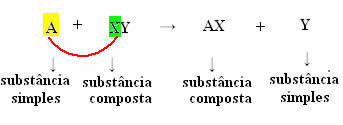
Men for at dette skal ske, det enkle stof, i det tilfælde symboliseret ved A, skal være mere reaktivt end det element, der vil blive fortrængt fra forbindelsentransformerer sig selv til et nyt simpelt stof (Y).
Lad os se på et eksempel, hvor denne reaktion opstår:
Overhold eksperimentet nedenfor, hvor et ark zink (Zn) placeres i en vandig opløsning af kobbersulfat (CuSO4). Over tid bemærkes det, at kobbersulfatopløsningen skifter fra en blå farve til en mindre intens blå, da den misfarves, og der var en aflejring af kobber på zinkpladen.

Vi kan repræsentere denne reaktion ved hjælp af følgende kemiske ligning:

Bemærk, at zink har fortrængt kobber, hvilket betyder, at zink er det mest reaktive.
Da begge er metaller, kan vi kontrollere, om den enkle udvekslingsreaktion vil forekomme eller ikke ved at analysere
metalreaktivitetskø vist nedenfor:
Bemærk, at kobber faktisk er mindre reaktivt end zink, så hvis vi besluttede at gøre det modsatte af det forrige eksperiment og læg et kobberark i en zinksulfatopløsning, reaktionen ville ikke forekomme, da kobber ikke ville være i stand til at fortrænge zink.
Forskydningsreaktioner er en type redoxreaktion, da der er en overførsel af elektroner fra det enkle stof til kompositten. I den ovenfor forklarede proces var zink oprindeligt i sin neutrale form, som er metallisk, og blev en del af en forbindelse, hvor den har en ladning på 2+, dvs. hvert zinkatom har mistet to elektroner. Med kobber sker det modsatte, det modtager to elektroner til at passere til den metalliske, faste tilstand.
I tilfælde af en simpel udvekslingsreaktion med ikke-metaller overvejes det: reaktionen finder kun sted, hvis det mest reaktive ikke-metal er det enkle stof, der kan fortrænge et andet mindre reaktivt ikke-metal. Reaktiviteten af ametaler er vist nedenfor:

Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/reacoes-deslocamento-substituicao-ou-simples-troca.htm
