Vand alene kan ikke fjerne fedt fra materialer. Dette er fordi Detvand er polært, som vist på billedet nedenfor, på grund af forskellen i elektronegativitet, der findes mellem hydrogen- og iltatomerne i deres molekyler. På den anden side, fedtet er ikke-polært og vand opløser derfor ikke fedt.
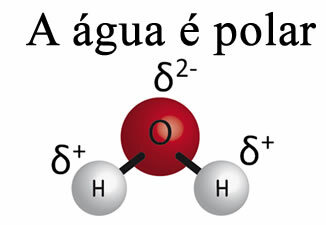
Derudover har vand noget, der hedder overfladisk spænding. Du kan forstå dette bedre i teksten. Overfladespænding af vand, men dybest set er det en slags elastisk film eller membran, der dannes på overfladen af vand, som forhindrer den i at trænge ind i stoffer og andre materialer for at fjerne snavs. Vandmolekyler tiltrækker hinanden i alle retninger igennem hydrogenbindinger, men overflademolekyler interagerer kun med molekyler på siden og under, hvilket skaber en forskel i samhørighedskræfter, hvilket får overflademolekylerne til at trække sig sammen og danne denne overfladespænding.
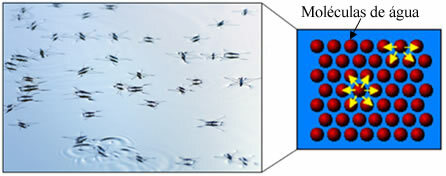
Det er her sæber og vaskemidler kommer ind (fra latin afgift = klar), som også kaldes overfladeaktive stoffer, da de har evnen til at reducere overfladespændingen af vand og derudover interagere med både vand og fedt.
Hvordan sker dette?Sæber og vaskemidler har fedtsyresalte, som er lange molekyler dannet af en ikke-polær del (hvad er hydrofob – hydro = vand; fobes = aversion) og en polar ende (hydrofil – hydro = vand; phyla = ven). Nedenfor har vi en typisk struktur af en sæbe:
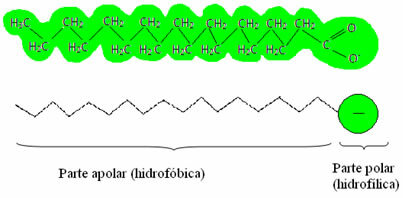
Generelt er vaskemidler salte af langkædede sulfonsyrer:
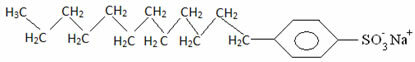
Således interagerer den ikke-polære del af disse molekyler i sæber og vaskemidler med fedtet, mens den polære ende interagerer med vand og grupperer sig i små kugler, ringede fra miceller, hvor de hydrofile dele vender ud mod micellen i kontakt med vandmolekylerne, og fedt forbliver på indersiden, i kontakt med den ikke-polære eller hydrofobe del, en proces svarende til den, der er vist på billedet a følge efter:
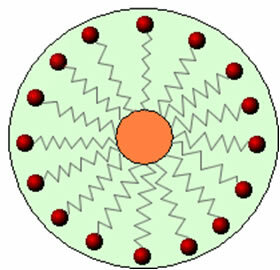
På denne måde fanges det fedtede snavs i midten af micellerne og kan fjernes. Et andet punkt er, at vaskemidler og sæber har evnen til at sænke vandets overfladespænding, fordi mindske interaktionerne mellem dets molekyler, hvilket gør det lettere for det at trænge igennem forskellige materialer for at fjerne det smuds.
Af Jennifer Fogaça
Uddannet i kemi
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm


