ionisering er det kemiske fænomen, hvor et surt stof (hvis generelle formel er HX), når det er opløst i vand, giver anledning til to ioner: en hydroniumkation (H3O+ eller H+) og enhver anion (X-). Fænomenet er repræsenteret fra en ligning. Se:
HX + H2O → H3O+ + X-
Under en ionisering er kun de ioniserbare hydrogener fra syre de omdannes til hydronium-kationer, en faktor, der også afhænger af denne syres ioniseringskapacitet, dvs. af graden af ionisering (α). Således danner ikke alt hydrogen hydronium, medmindre syren har en ioniseringsgrad lig med 100%.
Men når vi er opbygning af en ioniseringsligning, vi tager ikke højde for graden af ionisering af syren, men mængden af ioniserbare hydrogener som han præsenterer.
Som en generel regel betragter vi ioniserbart hydrogen som alt hydrogen til stede i en hydracid. I tilfælde af oxysyrer er kun hydrogener bundet til carbonatomer ioniserbare, som det kan ses i strukturformlen vist nedenfor:
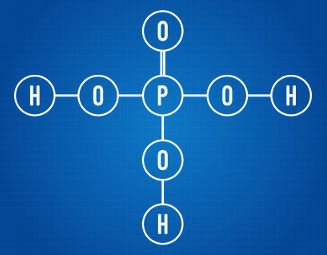
Phosphorsyre har tre ioniserbare hydrogener
Når vi analyserer strukturformlen ovenfor, kan vi se, at den pågældende syre har tre hydrogenatomer bundet til iltatomer. Som sådan har den i alt tre ioniserbare hydrogener.
Se nogle eksempler på samlingen af ioniseringsligning af nogle syrer:
Eksempel 1: Hydrobromsyre (HBr)
HBr + H2O → H3O+ + Br-
Hydrobromsyre er et hydracid med kun et hydrogen i dets sammensætning. Da alt brint i en hydracid kan ioniseres, dannes det kun, når det opløses i vand en mol hydroniumkation Det er bromidanion (Br-).
Eksempel 2: Hydrogensulfid (H2S)
H2Y + 2 H2O → 2 H+ + S-2
Hydrogensulfid er et hydracid med to hydrogener i dets sammensætning. Da alt brint i en hydracid kan ioniseres, dannes det, når det opløses i vand, to mol hydronium kationer Det er sulfidanion (S-2). Til dette brugte vi to mol vand.
Eksempel 3: mangansyre (H2MnO4)
H2MnO4 + 2 H2O → 2 H3O+ + MnO4-2
Mangansyre er en oxy syre med to hydrogener i sammensætningen. Som i oxysyrer er kun det hydrogen, der er bundet til et ilt, ioniserbart - i tilfælde af mangansyre er de to hydrogener - det vil dannes, når det opløses i vand, to mol hydronium kationer Det er manganatanion (MnO4-2). Til dette brugte vi to mol vand.
Eksempel 4: Phosphorsyre (H3STØV3)
H3STØV3 + 2 H2O → 2 H3O+ + HPO3-2
Phosphorsyre er en oxy syre med tre hydrogener i dens sammensætning. Som i oxysyrer er kun det hydrogen, der er bundet til et ilt, ioniserbart - i tilfælde af phosphorsyre er de to hydrogener - det vil dannes, når det opløses i vand, to mol hydronium kationer Det er phosphitanion (HPO3-2). Til dette brugte vi to mol vand.
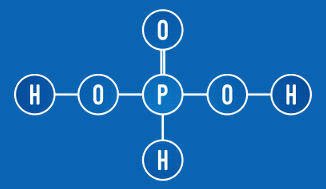
Fosforsyre har to ioniserbare hydrogener (OH-gruppe)
Eksempel 5: Borsyre (H3BO3)
H3BO3 + 3 H2O → 3 H+ + BO3-3
Borsyre er en oxy syre med tre hydrogener i dens sammensætning. Som i oxysyrer er kun det hydrogen, der er bundet til et ilt, ioniserbart - i tilfælde af borsyre er de tre hydrogener - det vil dannes, når det opløses i vand, tre mol hydronium kationer Det er boratanion (BO3-3). Til dette brugte vi tre mol vand.
Eksempel 6: Pyrophosphorsyre (H4P2O7)
H4P2O7 + 4 H2O → 4 H3O+ + P2O7-4
Pyrophosphorsyre er en oxy syre med fire hydrogener i sammensætningen. Som i oxysyrer er kun det hydrogen, der er bundet til et ilt, ioniserbart - i tilfælde af borsyre er de fire hydrogener - det vil dannes, når det opløses i vand, fire mol hydronium kationer Det er anionpyrophosphat (P2O7-4). Til dette brugte vi fire mol vand.
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/equacoes-ionizacao-dos-acidos.htm

