O vinylchlorid det er en kulbrinte giftig kloreret og kræftfremkaldende virkning. Det er en farveløs gas ved stuetemperatur, som er meget brandfarlig og følsom over for varme.
Det er den monomer, der bruges til fremstilling af polyvinylchlorid, et stof kendt som PVC. O PVC er en varmebestandig termoplast (i modsætning til sin monomer), der har adskillige anvendelser i hverdag, såsom belægning af elektriske ledninger, konstruktion af rør og forskellige typer af emballage.
Læs også:Asbest — naturfiber med bred industriel anvendelse, men ekstremt giftig for mennesker
Emner i denne artikel
- 1 - Resumé om vinylchlorid
- 2 - Vinylchlorids egenskaber
- 3 - Hvad er vinylchlorid?
- 4 - Karakteristika for vinylchlorid
- 5 - Hvad bruges vinylchlorid til?
- 6 - Indhentning af vinylchlorid
-
7 - Forholdsregler med vinylchlorid
- Vinylklorid og kræft
- 8 - Forekomst af vinylchlorid
- 9 - Vinylchlorids historie
Resumé om vinylklorid
Vinylchlorid er et chloreret carbonhydrid med formlen H2C=CHCI.
Det er en gas farveløs, sødt lugtende og meget brandfarlig.
Vinylchlorid er ustabilt overfor varmeundergår nedbrydning.
Den vigtigste anvendelse af vinylchlorid er i fremstillingen af polyvinylchlorid (PVC).
PVC er en termoplast med mange anvendelsesmuligheder, såsom rør, dele, belægninger, emballage osv.
Vinylchlorid er giftigt og har en kræftfremkaldende effekt.
vinylchlorid egenskaber
molekylær formel: CH2CHCI (C2H3Cl).
Molekylmasse: 62,498 g/mol.
fysisk tilstand: gas (farveløs og med en stærk lugt).
Massefylde: 0,91 g/ml.
Opløselighed i vand: meget lidt opløselig (0,6 g i 100 ml vand, 20 °C).
smeltetemperatur: -154°C.
Kogetemperatur: -13°C.
Stop ikke nu... Der er mere efter reklamen ;)
Hvad er vinylklorid?
Vinylchlorid er et chloreret carbonhydrid med formlen H2C=CHCI. Ved stuetemperatur sker det med en Farveløs og meget brandfarlig gas.
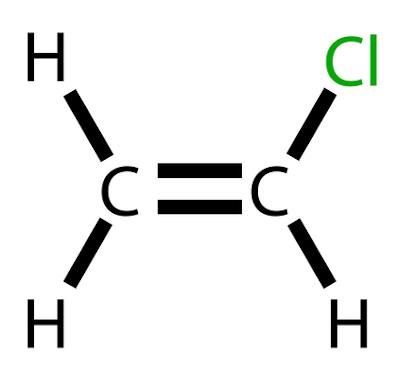
Vinylchlorid, også kaldet chlorethen eller vinylchloridmonomer, er en kemisk produkt af stor betydning i industri, der har særlig anvendelse ved fremstilling af polymer polyvinylchlorid, bedre kendt som PVC. Denne forbindelse indtager listen over de 20 produkter, der stammer fra Petroleum af større industriel og økonomisk relevans.
Læs også:Benzopyren - kræftfremkaldende kulbrinte fundet i cigaretrøg og grillet kød
Egenskaber af vinylklorid
Vinylchlorid er en Farveløs gas med en mild, sød lugt. Det har den egenskab, at det er meget brandfarligt.
Når de udsættes for varmekilder, kan undergå nedbrydning og udsende giftige dampe i carbondioxid, carbonmonoxidhydrogenchlorid og phosgen. Fordi det er en organisk forbindelse er dens opløselighed i vand ekstremt lav, til gengæld er den opløselig i stoffer som f.eks. ethanol, benzen og carbontetrachlorid.
I nærvær af fugt bliver vinylchlorid ætsende og kan angribe jern og stål. Det har kapacitet til at polymerisere, når det udsættes for varme i atmosfærisk luft, gennem en eksoterm reaktion. Denne ejendom har mange af sine industrielle anvendelser.
Vinylklorid kræver opmærksomhed pga det er giftigt og kræftfremkaldende.
Hvad bruges vinylchlorid til?
Vinylchlorid er monomer, der bruges til fremstilling af PVC-polymer (polyvinylchlorid) og andre klorerede opløsningsmidler.
PVC er en termoplast, der anvendes til fremstilling af emballage, fodtøj, elektriske forbindelser og kabler, piber, vinduer, rør og blodopsamlingsposer, tøj, blandt utallige andre genstande.

O PVC dannes ved polymerisation af vinylchlorid. I denne kemiske proces føjes et stort antal vinylchloridmolekyler til hinanden og danner en stor kemisk struktur.
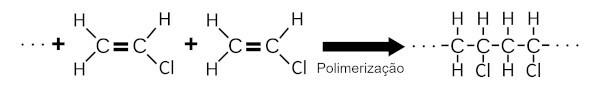
O PVC er flammehæmmende og af denne grund er det meget brugt til belægning af ledninger, elektriske kabler og boligbelægninger.
Selvom vinylchlorid er en kemisk forbindelse, der kræver opmærksomhed på grund af sin toksicitet og termisk ustabilitet, dens PVC-polymer er meget stabil over for varmekilder, den er ikke-giftig og kan opbevares med sikkerhed.
Indtil 1974 blev vinylchlorid brugt i aerosoler. Tidligere blev det endda brugt som inhalationsbedøvelse. Med kendskab til denne forbindelses toksicitet blev disse anvendelser afbrudt.
Indhentning af vinylklorid
Syntesen af vinylchlorid anvendt i industriel skala er initieret med forbindelsen ethylen eller ethen (CH2=CH2) og kan forekomme ad to veje.
I den første omdannes ethylen til 1,2-dichlorethan ved reaktion med klorgas. Ved at opvarme 1,2-dichlorethanen i nærværelse af en katalysator opnås derefter vinylchlorid som hovedprodukt og saltsyre som et sekundært produkt.
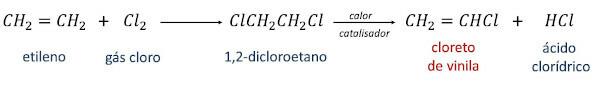
I den anden reaktionsvej, kendt som oxychlorering, er reaktionen mellem ethylen, saltsyre og ilt fra selve atmosfæren, i nærvær af varme og en katalysator, der genererer vinylchlorid og vand som produkter.

Typisk er et vinylchloridproduktionscenter bygget til at rumme begge fremstillingsprocesser. citeret, således at saltsyren dannet i den første metode fungerer som et reagens til at udføre den anden rute.
Forholdsregler med vinylklorid
Vinylchlorid er en giftig forbindelse. Da det er en gas, Den vigtigste form for forurening er ved indånding., hvorfor dens håndtering altid skal ske med brug af egnet udstyr, såsom gasmasker.
Eksponering for dette stof påvirker nervesystem perifere og centrale, hvilket forårsager skade på lever. EN Kontinuerlig eksponering kan udløse Raynauds fænomen, som er et sæt af symptomer, der omfatter led- og muskelsmerter og hudforandringer, som kan udvikle sig til et fuldstændigt tab af hudens elasticitet, endda påvirke organer indre organer og blodkar.
Andre effekter omfatter eufori, desorientering, abort og fosterskader. Skader på øjenvæv registreres også.
Symptomer afhænger af eksponeringsniveauet for stoffet, lige fra svimmelhed, kvalme, synsforstyrrelser, hovedpine og ataksi ved akut eksponering (fra 1000 til 8000 ppm vinylchlorid i luft), til narkotisk effekt, hjertearytmi og dødelig respirationssvigt i tilfælde af eksponering for niveauer over 12000 ppm.
Vinylklorid og kræft
O vinylchlorid er et kræftfremkaldende stof, forbundet med en høj risiko for at udvikle leverkræft, som kan bidrage til forekomster af hjernekræft og lunge, samt kræft i lymfesystemet.
Læs også:Ammoniumnitrat — forbindelse brugt i landbruget, der kan forårsage eksplosioner
Forekomst af vinylklorid
vinylchloridet genereres spontant i miljøet gennem nedbrydning af nogle forbindelser indeholdende klorgennem påvirkning af mikroorganismer. Derfor kan det betragtes som en luft- og vandforurenende stof, især i regioner tæt på lossepladser.
Imidlertid er den højeste forekomst af vinylchlorid ad syntetiske veje, relateret til den kemiske industri, som tidligere diskuteret.
Vinylchlorids historie
Vinylchlorid var opdaget i 1835 af den tyske kemiker Justus von Liebig, når dichlorethan omsættes med kaliumhydroxid i et alkoholholdigt miljø.
Senere, i 1872, observerede kemikeren Eugen Baumann for første gang polymeriseringen af vinylchlorid, der stammer fra PVC, efter at have forladt en beholder med stoffet udsat for solen ved et uheld.
I 1926 opdagede den amerikanske opfinder Waldo Semon kemiske tilsætningsstoffer, der gav større elasticitet og formbarhed til PVC, hvilket udvidede anvendelsesmulighederne for dette stof. Omkring 1950 begyndte PVC at blive brugt i industriel skala. I øjeblikket er PVC en af de mest brugte termoplaster i verden.
Af Ana Luiza Lorenzen Lima
Kemi lærer
Har du nogensinde hørt om det kemiske grundstof klor? Klik her og lær om dens karakteristika, egenskaber, opnåelse, applikationer og historie.
Kend den kemiske sammensætning, produktionskilder og anvendelser af mange organiske forbindelser, såsom acetone, alkohol, ether, blandt andre.
Lær mere om egenskaber, typer, nomenklatur og hvor kulbrinter kan findes.
Lær den kemiske sammensætning af PVC-polymer (polyvinylchlorid), der er meget udbredt i produktionen af rør og syntetiske lædermaterialer, at kende.