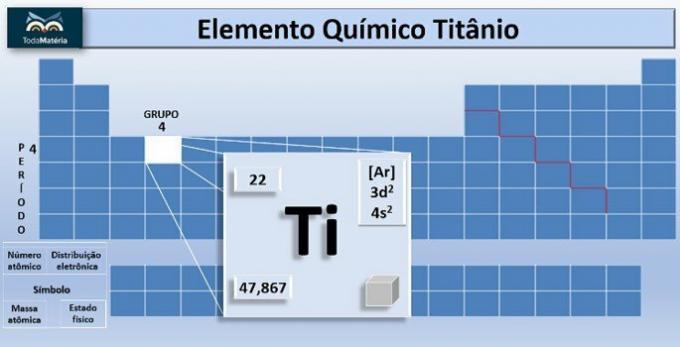
O titanium er det kemiske grundstof med symbol Ti og atomnummer, det vil sige antal protoner lig med 22. Dette metal er placeret i gruppe 4 og 4 i det periodiske system.
Grundstoffets atommasse er 47.867 u, og fordi det har 22 elektroner i atomets elektroner, er dets elektronfordeling 1s2 2s2 2 p6 3s2 3 s6 4s2 3d2.
Titanium har ønskværdige egenskaber til adskillige anvendelser, da det er så stærkt som stål og meget lettere.
Fordi det er et duktilt, ildfast, korrosionsbestandigt metal, udviser det mekanisk modstand, termisk stabilitet og lav reaktivitet tilsættes det til metallegeringer, så de har en høj ydeevne. Dens biokompatibilitet og ikke-toksicitet gør den også nyttig til fremstilling af knogleproteser.
De vigtigste egenskaber ved titanium er:
- Smeltepunkt: 1668 °C
- Kogepunkt: 3287 °C
- Massefylde: 4,5 g/cm3
- Farve: sølvgrå
- Fysisk tilstand ved 20 °C: fast
- Isotoper: Ti46, dig47, dig48, dig49 og dig50
Dette kemiske grundstof blev opdaget af englænderen William Gregor i 1791 og dets navn stammer fra det græske titaner, blev senere tilskrevet af Martin Heinrich Klaproth.
Titanium er det niende mest udbredte grundstof på planeten og findes i jordskorpen i malme som rutil (TiO)2) og ilmenit (FeTiO3). Derfor er minedrift den vigtigste metode til at opnå dette metal.
Hvad bruges titan til?
Fordi det er kemisk ureaktivt ved stuetemperatur, let støbes, har høj mekanisk og korrosionsbestandighed, bruges titanium som et strategisk metal.
Luftfarts- og rumfartsindustrien er hovedbrugerne af titanium til fremstilling af dele, såsom turbine- og skrogkomponenter. Andre anvendelser er fremstilling af tandproteser, kirurgiske implantater og smykker.
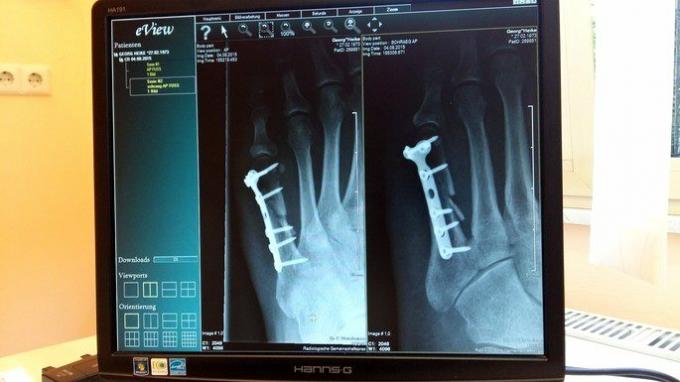
I medicin er titanium meget nyttigt på grund af dets kompatibilitet med menneskeligt væv, lethed og styrke. Det bruges til fremstilling af implantater til kropsdele, såsom fikseringsskruer, udskiftning af knæled, humerusproteser, hofteproteser m.fl.
Titandioxid (TiO2) er en af hovedforbindelserne af dette grundstof, der bruges som blegemiddel. Generelt bruger hvidt blæk af høj kvalitet det til at forbedre det visuelle udseende af farve og glans. Andre produkter, såsom tandpastaer og solcremer, bruger også pigmentet. Der er også anvendelse som fødevarefarve tilsat i mejeriprodukter, slik og drikkevarer.
I arkitekturen kan vi se brugen af titanium til at dække buede strukturer på Guggenheim-museet i Bilbao, det nordlige Spanien.

I hverdagen kan vi finde adskillige produkter, der har titanium i deres sammensætning, såsom cykelstel, briller og tennisketchere.
I den kemiske industri bruges titanium som katalysator for reaktioner. På den måde gør det muligt at styre reaktionshastigheden og reducere tiden for produktdannelse uden at påvirke sammensætningen af stofferne.
Bilindustrien har undersøgt inkorporeringen af titanium i fremstillingen af biler for at reducere deres masse og dermed reducere brændstofforbruget og øge deres acceleration.
Få mere viden om indholdet:
- Kemiske grundstoffer
- Periodiske system
- Hvad er metaller?
Bibliografiske referencer
ATKINS, P.W.; JONES, L. Principper for kemi: stille spørgsmålstegn ved det moderne liv og miljøet. 3.udg. Porto Alegre: Bookman, 2006.
FELTRE, R. Fundamentals of Chemistry: vol. enkelt. 4. udg. Sao Paulo: Moderna, 2005.
Lee, J. D. Ikke så kortfattet uorganisk kemi. Oversættelse af 5. udg. Engelsk. Udgiver Edgard Blucher Ltd. 1999.

