DET periodisk klassificering af grundstoffer blev foreslået i 1913 af Henry Monseley (1887-1915), som identificerede den periodiske variation af mange egenskaber med jævne mellemrum i henhold til antallet af protoner i kernen af et grundstofs atom kemisk.
På grund af Lov om periodicitet, kriteriet, der bruges til at organisere elementerne i det aktuelle periodiske system, er den stigende rækkefølge af atomnummer (Z).
De 118 kemiske grundstoffer er arrangeret i grupper og perioder i det periodiske system. Efter de fysiske og kemiske egenskaber er det muligt at skelne mellem metaller, ikke-metaller (ikke-metaller) og halvmetaller (metalloider).

De lodrette linjer er 18 grupper tabellen og samle grundstoffer med lignende kemiske egenskaber. De vandrette linjer svarer til 7 perioder og præsenterer elementerne med det samme antal elektroniske lag.
Brint er et grundstof, der er placeret over gruppe 1 på grund af dets elektroniske distribution, men det har ingen egenskaber til fælles med dem.
Tjek ud Periodiske system komplet og opdateret.
metaller
De fleste kemiske grundstoffer i det periodiske system er klassificeret som metaller. De vigtigste egenskaber ved metaller er:
- De har en karakteristisk glans;
- De er tætte, formbare og duktile;
- De er gode ledere af elektricitet og varme;
- De er til stede under omgivende forhold i fast tilstand, med undtagelse af kviksølv.
De metalliske grundstoffer i det periodiske system er:
alkalimetaller (gruppe1): lithium, natrium, kalium, rubidium, cæsium og francium.
jordalkalimetaller (gruppe 2): beryllium, magnesium, calcium, strontium, barium og radium.
Repræsentative anliggender, ud over grundstofferne i gruppe 1 og 2, er: aluminium, gallium, indium, thallium, nion, tin, bly, flerovium, bismuth, muscovium og livermorium.
Ydre overgangsmetaller er de grundstoffer, der optager den centrale del af det periodiske system:
- Gruppe 3: skandium og yttrium.
- Gruppe 4: titanium, zirconium, hafnium og rutherfordium.
- Gruppe 5: vanadium, niobium, tantal og dubnium.
- Gruppe 6: chrom, molybdæn, wolfram og seaborgium.
- Gruppe 7: mangan, technetium, rhenium og bohrium.
- Gruppe 8: jern, ruthenium, osmium og hassium.
- Gruppe 9: kobolt, rhodium, iridium og meitnerium.
- Gruppe 10: nikkel, palladium, platin, darmstadium.
- Gruppe 11: kobber, sølv, guld og røntgen.
- Gruppe 12: zink, cadmium, kviksølv og copernicium.
Interne overgangsmetaller er de grundstoffer, der er en del af gruppe 3 og svarer til grundstofferne i lanthanid- og actinidrækken.
Lanthanidserien består af lanthan, cerium, praseodym, neodym, promethium, samarium, europium, gadolinium, terbium, dysprosium, holmium, erbium, thulium, ytterbium og lutetium.
Actinid-serien indeholder grundstofferne actinium, thorium, protactinium, uranium, neptunium, plutonium, americium, curium, berkelium, californium, einsteinium, fermium, mendelevium, nobelium og laurence.
Læs mere om alkalimetaller.
ikke-metaller
Ikke-metaller er placeret i højre del af det periodiske system og har modsatte egenskaber til metaller, for eksempel:
- De har ikke et skinnende udseende;
- De er ikke gode ledere af elektricitet og varme, så de bruges som isolatorer;
- De har lave koge- og smeltepunkter, så mange findes i naturen i flydende tilstand.
Du ikke-metalliske elementer i det periodiske system er: brint, nitrogen, oxygen, kulstof, fosfor, selen, svovl, halogener og ædelgasser.
Du halogener er de grundstoffer, der hører til gruppe 17: fluor, klor, brom, jod, astatin, tenessine og ædelgasfamilien.
Du ædelgasser er de grundstoffer, der hører til gruppe 18: helium, neon, argon, krypton, xenon, radon, oganesson.
Lær mere om ædelgasser og halogener.
halvmetaller
Halvmetallerne eller metalloiderne er: bor, silicium, germanium, arsen, antimon, tellur og polonium. Disse elementer har egenskaber, der er mellemliggende mellem metaller og ikke-metaller.
Læs også om periodiske tabel familier.
Repræsentative og overgangselementer
En anden måde at klassificere elementer på er ved at opdele dem i repræsentative og overgangselementer i henhold til elektronisk fordeling af atomet.
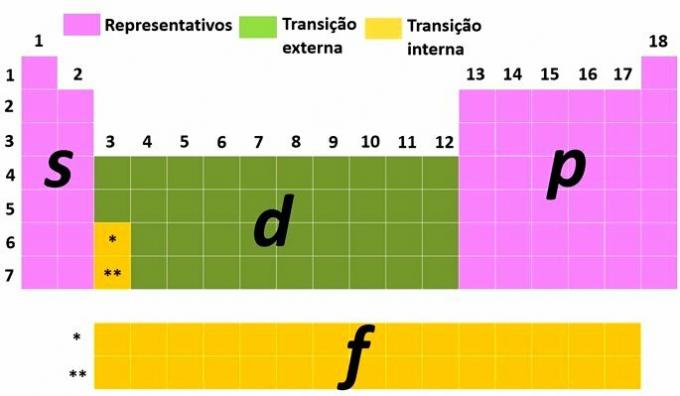
Du repræsentative elementer er dem, der har den elektroniske konfiguration, der slutter med det mest energiske underniveau i s (gruppe 1 og 2) eller til (gruppe 13, 14, 15, 16, 17 og 18).

Du overgangselementer er adskilt i ekstern overgang, med de grundstoffer, der har den mest energiske elektron i underniveauet d og de af indre overgang, hvor den mest energiske elektron er i et underniveau f.

Få mere viden om indholdet:
- periodiske egenskaber
- Periodiske øvelser
- Øvelser om organisering af det periodiske system


