Alkoholer kan undergå oxidation, når de udsættes for et oxidationsmiddel, såsom en vandig opløsning af kaliumdichromat (K2Cr2O7) eller kaliumpermanganat (KMnO4) i et surt medium.
Et spirende oxygen [O] i midten vil angribe kulstoffet, der er knyttet til alkoholens funktionelle gruppe (hydroxyl- OH), der danner en meget ustabil forbindelse, kaldet tvillingediol, som har to hydroxylgrupper knyttet til samme kulstof. Da det er ustabilt, frigiver denne forbindelse vand og giver anledning til et nyt produkt.
Dette produkt vil afhænge af typen af alkohol, der er blevet oxideret, om det er primær, sekundær, tertiær eller methanol.
Kort fortalt har vi:
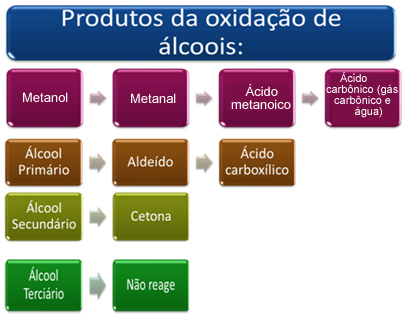
Se hvert enkelt tilfælde nedenfor:
- Methanol (H3C─ OH):
Methanol er den eneste alkohol, der har tre hydrogenatomer bundet til kulstof, der vil gennemgå oxidation. I dette tilfælde, da der er tre punkter på molekylet, som en begyndende oxygen kan angribe, vil der forekomme tre successive oxidationer, som vist i diagrammet nedenfor:
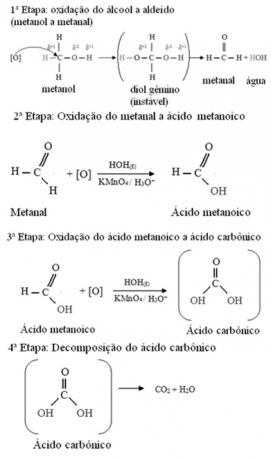
- Primære alkoholer:
I disse forbindelser er hydroxyl-carbonet kun bundet til et carbonatom, det vil sige, at de to andre ligander er hydrogener, og der er to steder, hvor den begyndende ilt kan angribe.
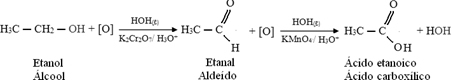
Først vil der være dannelse af et aldehyd, som vist nedenfor:
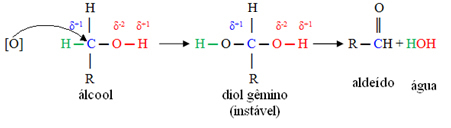
Men oxidationen fortsætter, fordi de reagenser, der bruges til at oxidere alkohol, er stærkere end dem, der bruges til at oxidere et aldehyd. Derefter angriber en anden begyndende oxygen carbonylcarbonet og producerer en carboxylsyre.
Det følgende er et eksempel, oxidation af ethanol, først til ethanal og derefter til ethansyre (eddikesyre). Denne totale reaktion er omdannelsen af vin til eddike.
Stop ikke nu... Der er mere efter reklamen ;)
Delvis oxidation af ethanol til ethanal opstår, når en alkoholiker tager en engangsalkotest. Inde i denne enhed er der en fast blanding af kaliumdichromat og silica i et surt medium, hvor følgende reaktion forekommer:
K2Cr2O7(aq) + 4H2KUN4(aq) + 3 CH3CH2åh(g) → Kr2(KUN4)3(aq) + 7 om morgenen2O(1) + 3 CH3CHO(g) + K2KUN4(aq)
orangeethanol (farveløs)grønethanal (farveløs)
Bemærk, at der udover oxidationen af ethanol (alkohol) til ethanal (aldehyd) sker en samtidig reduktion af dichromat, som er orange, til chrom (III) eller endda chrom (II), som er grønt. Ændringen i farve vil indikere, at personen har mere alkohol i blodet end tilladt.
- Sekundære alkoholer:
Det er forbindelser, hvori hydroxylcarbonet er bundet til to andre carbonatomer og kun et brintatom. Derfor vil der kun være ét sted i molekylet, hvor den begyndende ilt kan angribe, og der vil kun blive dannet én type produkt, som altid vil være en keton:
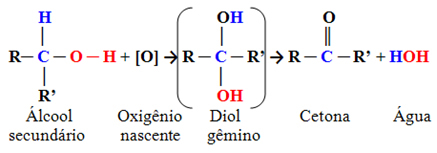
Da carbonylcarbonet i en keton ikke har noget hydrogen bundet direkte til sig, er der ikke længere nogen mulighed for yderligere oxidation. Derfor stopper reaktionen ved ketonen.
- Tertiære alkoholer:
Tertiære alkoholer er dem, hvor carbonet, der har -OH-gruppen, laver tre bindinger med andre carbonatomer. Da de ikke binder sig til hydrogener, er der ingen mening på molekylet, der kan angribes af ilt, der er i vækst. På grund af dette faktum undergår tertiære alkoholer ikke oxidation.
* Kilde og forfatter til billedet: CostaPPPR.
Af Jennifer Fogaça
Uddannet i kemi
Vil du referere til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Oxidation af alkoholer"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm. Tilgået den 27. juli 2021.
Kemi

Hvordan alkometeret virker, alkoholkoncentration, alkometer, reaktioner, der involverer ethylalkohol, typer af alkometer, kaliumdichromat, brændselscelle, katalysator, elektronfrigivelse, eddikesyre, brint, kons