Elektronisk fordeling refererer til, hvordan elektroner er fordelt i de lag eller energiniveauer, der omgiver atomets kerne.
Ifølge Rutherford-Böhr atommodellen har atomerne af kendte kemiske grundstoffer højst syv elektroniske lag, som øger energien fra indersiden til ydersiden af kernen (1 – 2 – 3 – 4 – 5 – 6 – 7). Disse syv lag kan også betegnes med de respektive bogstaver K – L – M – N – O – P – Q, hvor K er det første, er tættere på kernen og har den laveste energi. På den anden side er Q-laget det syvende, idet det er længst væk fra kernen og det med den højeste energi.
Da hvert atom har et atomnummer (mængden af protoner i kernen) og et forskelligt antal elektroner, elektronlag af hvert atom har forskellige energier, der holder elektroner med denne energi fast besluttet.
Mind Map: Elektronisk distribution

* For at downloade tankekortet i PDF, Klik her!
Bemærk nedenfor nogle atomer og elektroner fordelt i deres elektroniske lag:

Hydrogen, helium, beryllium og oxygenatom
Bemærk, at fordelingen af de fire atomer i beryllium er: 2 – 2, og fordelingen af oxygen er 2 – 6. Kun gennem disse eksempler er det muligt at se, at elektronisk distribution følger en ordre. For eksempel kan K (1)-skallen maksimalt have to elektroner.
Nedenfor har vi en tabel, der specificerer den maksimale mængde elektroner, der kan fordeles i hvert elektronisk lag:
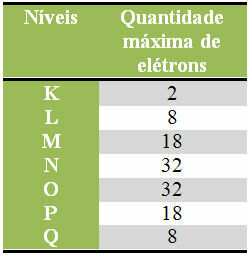
Maksimalt antal elektroner i elektroniske niveauer
Man skal også huske, at den sidste skal, der skal fyldes, den såkaldte valensskal, må højst have otte elektroner. Så hvis du fordelte elektronerne og så, at den sidste skal havde en mængde større end 8, men mindre at 18 så kun skulle efterlade 8 elektroner i den skal og tilføje resten i den næste skal plus ydre.
Stop ikke nu... Der er mere efter reklamen ;)
Overvej for eksempel den elektroniske fordeling af calciumatomet. Ser vi på det periodiske system, ser vi, at det har et atomnummer lig med 20, hvorimod der i grundtilstanden er det samme antal elektroner. Så vi skal fordele 20 elektroner i deres elektronskaller. Se det nedenfor:
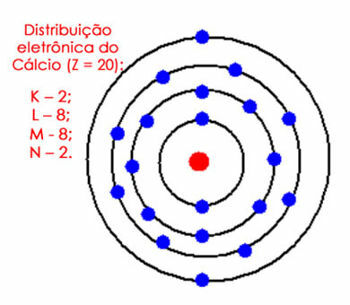
Elektronisk fordeling af calcium i atomet
Bemærk at M-skallen kan rumme op til 18 elektroner, men hvis vi putter de resterende elektroner i den, ville den have 10 elektroner, hvilket ikke kan ske i valensskallen. Så vi sætter de andre elektroner (2) i den næste skal, som er N.
Men hvis mængden af elektroner i den sidste skal er mellem 18 og 32, efterlader du 18 elektroner og sender resten videre til de ydre skaller. Se et andet eksempel:
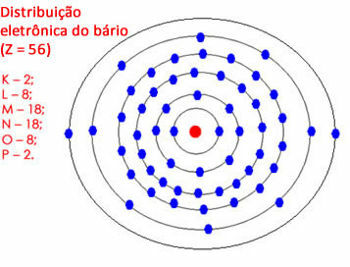
Elektronisk fordeling af barium i atomet
Bemærk, at "N"-skallen maksimalt kan indeholde 32 elektroner, men her ville den have 28. Så vi efterlader 18 elektroner og sender resten videre til den næste skal. Men "O"-skallen ville have 10 elektroner, så vi efterlod 8 og fordelte de andre 2 resterende elektroner til "P"-skallen.
Der er dog en nemmere måde at udføre denne elektroniske fordeling af et atoms elektroner på. Det er gennem Pauling diagram (da det blev skabt af videnskabsmanden Linus Carl Pauling (1901-1994)), også kendt som elektronisk distributionsdiagram eller endnu, Diagram over energiniveauer. Dette diagram ser således ud:
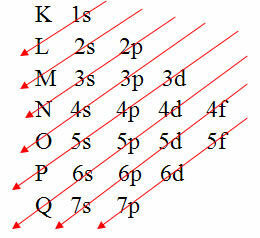
Den grafiske repræsentation af den elektroniske distribution er givet af Pauling-diagrammet
For at forstå, hvordan de elektroniske fordelinger af elektroner og ioner er lavet i dette diagram, skal du læse teksterne nedenfor:
* elektronfordeling;
* elektronisk ion distribution.
* Billedkredit fra Linus Pauling: Nobelprize.org
** Mind Map af Me. Diogo Lopes
Af Jennifer Fogaça
Uddannet i kemi
Vil du referere til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Hvad er elektronisk distribution?"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-distribuicao-eletronica.htm. Tilgået den 27. juli 2021.
Kemi

Niels Bohr, Bohrs atom, atomfysik, stabilt atom, atommodel, planetsystem, lag af elektrosfæren, energiniveauer, elektronskaller, elektronenergi, Rutherford atommodel, exciteret tilstandsatom.

